大多数化工生产都有催化剂的参与。
(1)化工生产使用催化剂的目的是 。
(2)研究表明氧化铜可催化过氧化氢分解。
①用如图1所示装置和药品制取氧气,反应的化学方程式为 。

②如图1中收集氧气的方法是向 排空气法。为了检验氧气是否收集满,将 放在集气瓶口。
③反应结束后,弃去试管中的上层清液,再向试管中加入过量稀硫酸,充分振荡,可观察到的现象 。
④为了制取较大量氧气,并便于多次添加过氧化氢溶液,请从如图2中选择合适的仪器或装置,重组一套制取装置,需要用到的是 (填标号)。
(3)下列设想有可能通过找到合适的催化剂来实现的是 (填标号)。
A.利用太阳光将水分解生产H2
B.将空气中的He分解生产H2
C.常温下Cu从硫酸镁溶液中置换出Mg
D.使一定质量CH4完全燃烧放出的热量变多
叠氮酸(HN3)常温下是一种无色液体,其水溶液具有酸性,可与NaOH溶液反应得到叠氮化钠(NaN3)。某些汽车安全气囊中装有叠氮化钠。
(1)叠氮酸在水溶液中解离出H+和 (填化学符号)。
(2)叠氮酸与NaOH溶液的反应属于 (填反应类型)。
(3)叠氮化钠受热分解时产生两种单质,该反应的化学方程式为 。
请将下列实验报告补充完整。
实验内容 |
现象 |
说明、解释或结论 |
(1)用高锰酸钾制取氧气。 连接仪器,检查装置气密性。用 (填仪器名称)取少量高锰酸钾装入试管中,并在试管口放一团棉花,固定好装置;加热试管,用排水法收集O2. |
当观察到 时,开始收集气体。 |
收集O2之前,将集气瓶内空气完全排净的方法是 。产生O2的化学方程式为 。 |
(2)酸与碱发生中和反应。 i.取少量稀NaOH溶液于试管中,滴入2滴酚酞溶液,再逐滴加入稀盐酸,边滴边振荡,至溶液的颜色恰好变为无色。 ii.往上述无色溶液中再滴入1滴稀NaOH溶液,观察现象。 |
步骤ii中观察到 。 |
步骤i中“边滴边振荡“的目的是 。 |
合理利用化石燃料资源,是人类不断探索的课题。某城市家用燃料的使用经历了如图所示的过程,并将逐步向理想燃料发展。

(注:括号中的物质是对应燃料的主要成分)
(1)CH4、C3H8两种物质中,氢元素的质量分数较大的是 (填化学式)。
(2)倡导“家用燃料低碳化”的意义是 。
(3)一定条件下,仅用一个置换反应即可制得CO和H2,反应的化学方程式为 。
(4)随着全球能源使用量的增长,化石燃料等不可再生能源将日趋枯竭。请提出一个缓解能源危机的设想: 。
科学使用化学物质,可以保障人体健康。
(1)某同学的部分体液的pH如图所示。
①图中碱性最强的体液是 。
②该同学胃酸(主要成分为盐酸)过多,可服用胃舒平[主要成分为Al(OH)3]治疗,其原理是 (用化学方程式表示)。
(2)某84消毒液产品的部分说明如下表。
84消毒液 [产品特点]主要成分为次氯酸钠(NaClO),有效氯的质量分数为5.1%~6.9%。 [餐具消毒]用有效氯的质量分数为0.04%的消毒液浸泡,20min后用生活饮用水冲净。 [注意事项]①外用消毒剂,须稀释后使用。 ②不得将本产品与酸性产品(如洁厕类清洁产品)同时使用。 |
①依据表中信息,将有效氯的质量分数为6.0%的84消毒液与水按质量比为1: 进行稀释,即可用于餐具消毒。
②洁厕灵(主要成分为盐酸)与84消毒液混合会产生有毒的氯气(Cl2)。请将该反应的化学方程式补充完整:2HCl+NaClO═ +Cl2↑+H2O

燃烧与人类生产、生活有着密切的关系。
(1)下列成语的原意与燃烧不相关的是 (填标号)。
A.卧薪尝胆
B.釜底抽薪
C.火上浇油
D.煽风点火
(2)古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”指高温条件下碳酸钙转化为生石灰。
①“煤饼烧石成灰”的过程中,能量转化的主要方式是 。
②“石”转化为“灰”的反应属于 (填基本反应类型)。
③“灰”遇水成浆,该反应的化学方程式为 。
(3)室内起火时,如果急于打开门窗,火反而会烧得更旺。原因是 。
硫酸亚铁晶体是重要的化学试剂。传统制备方法是用铁屑与稀硫酸反应,因铁屑中含有硫、磷等杂质,与稀硫酸反应会产生刺鼻、呛人的有毒气体。某科技小组改用铁屑与硫酸铜溶液反应制备硫酸亚铁晶体,流程如图:

(1)步骤①中反应的化学方程式为 。
(2)操作Ⅰ的名称是 。步骤②涉及到蒸发,蒸发时必需的仪器有铁架台(含铁圈)、酒精灯、玻璃棒、 。
(3)用硫酸铜溶液代替稀硫酸制备硫酸亚铁晶体,优点是 。
如图是实验室中常见装置。回答下列问题。
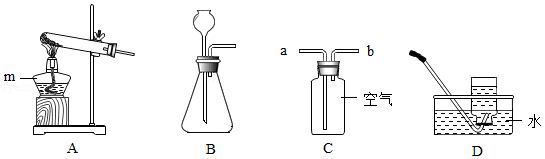
(1)装置A中仪器m的名称是 。
(2)用过氧化氢溶液制取氧气的化学方程式为 ,发生装置是 (填字母序号)。
(3)用装置C收集CO2气体时,气体应从 (填“a”或“b”)端通入。
(4)下列气体中,只能用装置D而不能用装置C收集的是 (填数字序号)。
①H2 ②N2 ③O2
阅读下列科技短文,回答问题。
废旧塑料制品和橡胶轮胎等含碳废物如何变废为宝,是众多科学家和工程师努力的目标。
研究人员开发出一种用超临界水处理含碳废物的新技术。超临界水是将水加热到超过374℃并加压到超过219个大气压,使水处于气、液相互交融的状态。
在超临界水的环境中,含碳废物中的有机物转化为氢气、甲烷和二氧化碳等气体;而无机物保留在残余物中,随后被去除。由于该过程中不使用氧气且温度相对较低,因此不会形成有害气体。
(1)文中涉及到的有机合成材料有 (填1种即可)。
(2)下列说法正确的是 (填字母序号)。
A.超临界水与液态水具有相同的物理和化学性质
B.将气态水升温或加压一定使水分子间距离变小
C.超临界水是由液态水和气态水组成的混合物
D.用超临界水处理含碳废物的方法比焚烧法更环保
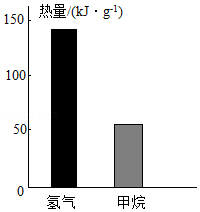
(3)氢气和甲烷都是清洁能源,写出甲烷完全燃烧时反应的化学方程式 。充分燃烧1g氢气或甲烷释放的热量如图所示,与甲烷相比,氢气作为燃料的优点是 ;而日常生活中使用的燃料,更多的是以甲烷为主要成分的天然气,原因是 (写出1点即可)。
补全实验报告。
装置及操作 |
现象 |
解释或结论 |
|
|
(1)向1中滴加 溶液 |
铁片上附着红色固体,溶液颜色变浅 |
Fe的金属活动性比Cu的强 |
(2)向2中滴加盐酸 |
固体减少,得到黄色溶液 |
化学方程式:
|
|
(3)向3中滴加足量盐酸 |
|
Ca(OH)2能与盐酸反应 |
|
下列是两个关于水的实验。

(1)实验1,反应的化学方程式为 。
(2)下列说法正确的是 (填序号)。
A.实验1,试管a中得到的气体能燃烧
B.实验1,反应前后原子的种类、个数均改变
C.实验2,水变化前后分子的种类不变
A.氧气的制取与性质 |
B.二氧化碳的制取与性质 |
|
|
(1)①中反应的化学方程式为 。
(2)②中观察到的现象是 。
从氯碱工业产生的盐泥中回收BaSO4,其主要工艺流程如图。
已知:①盐泥的主要成分为BaSO4、NaCl、Mg(OH)2和CaCO3。
②BaSO4难溶于水,不与盐酸反应。

(1)除去NaCl,利用的性质是 。
(2)酸溶槽中发生中和反应的化学方程式为 。
(3)过滤器中分离出来的固体是 。
2019年是门捷列夫元素周期表诞生150周年。某拓展小组模仿门捷列夫用扑克牌寻找元素规律的方法,对部分元素进行排列,位置如图所示。

(1)根据规律,图中钠元素扑克牌应放入的位置是 (填序号)。
(2)拓展小组用同样方法将其它元素排入相应的位置,并从表中选出几种元素,与钠元素组成了一种能和稀硫酸反应的盐。请写出该盐与稀硫酸反应的化学方程式 。