H2SO4是一种重要的化工原料。
(1)H2SO4溶液的pH 7(填“>”、“<”或“=”),请写出用pH试纸测定稀硫酸pH的正确方法 ;
(2)浓硫酸有吸水性,常用作某些气体的干燥剂,下列气体不能用浓硫酸干燥的是 (填写序号);
①H2
②CO2
③NH3
④HCl
(3)实验室常用亚硫酸钠固体(Na2SO3)和70%左右的硫酸溶液发生复分解反应制取SO2,请写出该反应的化学方程式: ;
(4)向160g含有H2SO4和CuSO4的混合溶液中逐滴加入NaOH溶液至过量,产生的沉淀质量与加入NaOH溶液质量的关系如图所示,请写出b点对应溶液的溶质 (填写化学式),原混合溶液中CuSO4的质量分数是 。

郴州东江湖,储水量大,水质优良,一直保持地表水一类水标准,被引入到多地作为居民饮用水。请回答下列问题:
(1)天然水中含有许多杂质,可以利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是 。
(2)以下防治水污染的措施中,你认为可行的是 (填写字母编号)。
A.禁止使用农药和化肥
B.应用新技术、新工艺减少污染物的产生
C.抑制水中所有动植物的生长
D.工业废水经净化处理达标后再排放
(3)水是一种常见的溶剂,同时也参与很多化学反应,如反应:Al2S3+6H2O═2Al(OH)3+3X↑,其中X的化学式为 ,Mg3N2也能与水发生上述类似的反应,请写出反应的化学方程式 。
根据下列实验装置图回答问题。

(1)仪器a的名称是 。
(2)实验室用过氧化氢溶液和二氧化锰制氧气时,应选择的气体发生装置是 (填字母),反应的化学方程式是 。
(3)用C装置收集二氧化碳时,检验二氧化碳已经收集满的方法是 。
(4)当气体从m口进入时,利用C装置还可以进行许多实验。下列实验设计方案中,不可行的是 (填序号)。
①C中盛澄清石灰水时,可以检验实验室制出的二氧化碳气体
②C中盛烧碱溶液时,可以除去一氧化碳中的二氧化碳气体
③C中盛浓硫酸时,可以除去氧气中的水蒸气
④C中盛适量冷水并放入一小块白磷时,可以验证可燃物燃烧的条件
小红和同学们完成了实验室制取氧气和验证氧气性质的实验,并进行了相关问题的思考。请结合图文信息完成下列任务。

(1)图1:仪器a的名称是 ,给试管预热的操作是 ,发生反应的化学方程式是 。
(2)图2:当气体从b端进c端出时,可收集到的一种气体是 (写名称)。
(3)图3:点燃系在螺旋状细铁丝底端的火柴,待 时,插入集气瓶中。
碳捕捉与封存技术
“碳捕捉与封存”是我国的一项先进技术(如图所示)。
我国能源消耗的70%来自于煤炭。每秒有100吨煤在燃烧,年消耗量超过30亿吨。如果任由煤炭资源在诸多领域利用,将对大气、河流、土地产生污染,温室效应增强。为实现节能减排、绿色环保,我国政府举全国之力,积极倡导并大力发展新的绿色经济。比如:电厂中的煤在极高的温度下充分燃烧,会产生大量CO2,每年的排放量大约1600万吨,达用“碳捕捉与封存”技术,这些CO2将不会进入大气。被封存的CO2有许多用途,如用于食品保鲜、气体肥料、冷藏食物、物品灭火等,以此来消除资源的巨大浪费。我国正以超世界一流的目光发展经济,完善环保体制。
阅读文本,完成下列任务:
(1)“碳捕捉与封存”技术有利于控制 的加剧。
(2)煤在极高的温度下充分燃烧,主要发生反应的化学方程式为 。
(3)将分离聚集的CO2压入地下的过程中,分子间隔会 。
(4)将CO2封入蓄水层中发生反应的化学方程式为 。
(5)被封存起来的CO2用于冷藏食物的原理是 。

请结合如图实验装置,回答问题:

(1)写出标号①仪器的名称 。
(2)写出实验室用高锰酸钾制取氧气的化学方程式 ,可选择装置 (填序号)作为气体发生装置,但在该装置中还需要补充的是 。
(3)实验室常用大理石和稀盐酸制取二氧化碳气体,写出反应的化学方程式 ,收集气体应选用装置 (填序号);若将收集到的二氧化碳气体,沿烧杯内壁慢慢倒入装置F中,可以观察到的现象是 ,说明二氧化碳具有 的物理性质。
通过近一年的学习,同学们一定深刻感受到化学就在身边,人类的衣、食、住、行都离不开化学,它使我们的生活变得更加绚丽多彩。请回答下列问题:
(1)你身上的衣服牢固耐穿、易洗快干、抗皱性好,是因为衣料大多都由 (填“合成纤维”或“天然纤维”)制成。
(2)自2018年以来,宁夏多地区启动深度净化黄河水替换地下水源供水,保障城乡居民饮水安全。黄河水自取水站经过沉淀、过滤、吸附、杀菌消毒,达到国家生活饮用水标准后,输送至千家万户。小刚通过 ,判断自来水仍然是硬水。饮用前,可 将其软化。
(3)你住的房屋建造时所用的各种材料也和化学有关。例如,用石灰浆粉刷过的墙壁,一段时间后,变得既白又坚固,其原理是 (用化学方程式表示)。
(4)“共享电动车”方便市民绿色出行,有效缓解了城市交通压力,减少了大气污染,成为现代城市的又一道靓丽“风景”。为防止电动车钢制车架与空气中的 等接触而生锈,通常在车架表面进行喷漆处理。
教材中用图1实验来验证硫能在氧气燃烧,某化学兴趣小组对该实验进行了改进,改进后的实验装置如图2,请完成实验过程中的相关问题。
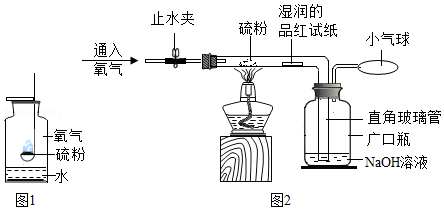
(1)根据图2进行实验,操作过程与现象记录如下:
①连接仪器,并在玻璃管中放入湿润的品红试纸及适量硫粉,向广口瓶中加入足量NaOH溶液。
②关闭止水夹,点燃酒精灯,加热,观察到硫粉熔化,并产生微弱的淡蓝色火焰。
③打开止水夹,通入氧气,观察到的现象:a. ,b.品红试纸褪色,c.小气球变大。
④硫粉完全反应后,熄灭酒精灯,继续通入氧气,排尽玻璃管中的SO2;待玻璃管冷却至室温时,关闭止水夹,撤下通入氧气的装置,然后应 ,并同时轻轻振荡广口瓶。
(2)问题讨论:
①图1实验设计中的不足之处是 。
②硫在氧气中燃烧更剧烈是因为 。
③反应过程中,玻璃管内湿润的品红试纸褪色,若改放干燥的品红试纸却不褪色,说明使品红试纸褪色的物质是 (提示:SO2与CO2的性质有相似之处)。
④广口瓶中吸收SO2的化学方程式为 。
实验室制取气体常用如图装置,请根据如图回答问题。
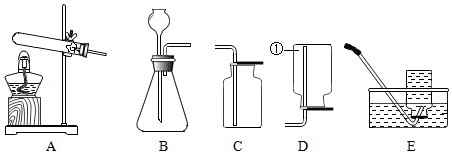
(1)写出图中标号仪器的名称:① 。
(2)实验室制取氢气的化学方程式为 ,若实验室用装置B制氢气,长颈漏斗的下端管口伸入液面下是为了防止 ,氢气的收集装置可选用 。氢气是一种高能燃料,点燃氢气前需要 。
(3)实验室将装置A和C组合,可制取的气体是 。
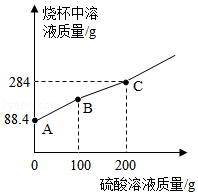
现有盛88.4g Na2CO3和NaOH混合溶液的大烧杯,向其中滴加质量分数为9.8%的H2SO4溶液,充分搅拌,烧杯中溶液的质量与滴加H2SO4溶液的质量关系如图所示,回答下列问题:
(1)写出AB段发生反应的化学方程式 。
(2)BC段可以观察到大烧杯的溶液中有气泡产生,则生成气体的质量为 g。
(3)B点时,大烧杯中的溶液pH 7(填“>”、“=”或“<”)。
(4)C点时,所得溶液为不饱和溶液。求溶液中溶质的质量分数。(写出计算过程)
气体制备、收集是初中化学的重要知识。请结合如图回答有关问题。

(1)写出图中仪器a的名称: 。
(2)实验室用氯酸钾和二氧化锰制取氧气,应选择的发生装置为 (填字母),写出该反应的化学方程式: 。
(3)用装置C代替装置B制取二氧化碳的优点是 ;用D装置收集二氧化碳,则气体应从 (填"①"或"②")端进入。

(4)用质软的塑料瓶收集满两瓶二氧化碳气体。向其中一瓶加入约 体积的水(如图F所示),立即旋紧瓶盖,振荡。观察塑料瓶最终的现象: ;用注射器向另一瓶(瓶口用橡胶塞塞紧)气体中注入约 体积的水(如图G所示),振荡。观察塑料瓶最终的现象: ,产生该现象的原因: 。
如图是初中化学实验室制取气体的常用装置图,请回答下列问题:
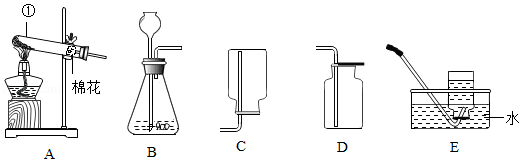
(1)仪器①的名称是 ;
(2)实验室制取二氧化碳选择的发生和收集装置是 (填写装置下方的字母);
(3)若用高锰酸钾制取氧气应选用的发生装置是 (填写装置下方的字母),写出该反应的化学方程式 ,检验氧气的方法是 ,排水法收集氧气不纯的原因是 (答一点即可)。
如图2为某钙片的商品标签,为测定钙片中钙元素的质量分数(假设钙片中其他物质不含钙元素,且不溶于水,也不与任何物质发生反应),某化学兴趣小组取20片钙片,进行如下实验:

(1)上述实验过程中发生反应的化学方程式为 。
(2)根据已知条件列出求解所加的稀盐酸中溶质质量(x)的比例式 。
(3)用36.5%的浓盐酸配制100g上述稀盐酸,所需浓盐酸的质量为 。
(4)钙片中钙元素的质量分数为 。
(5)若向滤液中加入5.4g水,所得溶液中溶质的质量分数为 。
(6)工厂生产钙片时若需碳酸钙120t,理论上需含氧化钙84%的生石灰的质量为 。
某化学小组选用如图部分装置制取纯净、干燥的CO2。

(1)写出A中所发生反应的化学方程式 。
(2)若将a、b连接,B中溶液不变浑浊,这是因为CO2中混有哪种杂质? 。
(3)为达到实验目的,所选用装置的导管接口从左到右的正确连接顺序为: a接 、 接 、 接j。
(4)用F收集CO2,j为进气口。请将F中的玻璃导管补画完整。