吸烟有害健康。香烟的烟气中含有几百种对人体有害的物质,毒害作用很大的有一氧化碳、尼古丁和含有致癌物的焦油等。下列有关尼古丁(化学式为C10H14N2)的说法正确的是( )
A.尼古丁完全燃烧只生成CO2和H2O
B.162g尼古丁中氢元素质量为14g
C.尼古丁中碳、氢、氮元素的质量比为5:7:1
D.尼古丁中氮元素的质量分数最大
水是常用溶剂,某同学进行如图实验。
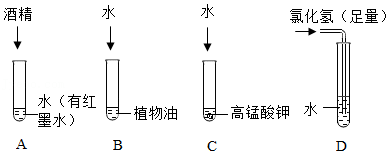
(1)倾斜A试管,沿内壁缓缓加入乙醇,不振荡,现象是 。
(2)实验可知,溶质状态可以是 。
(3)实验结束后,用洗涤剂洗净B试管,原理是 。
(4)C、D试管的废液倒入废液缸中产生了黄绿色气体,查阅资料可知:2KMnO4+16HCl(浓)═2KCl+2X+5Cl2↑+8H2O,X的化学式为 。
(5)询问老师得知用2NaOH+Cl2═NaCl+NaClO+H2O可处理Cl2。根据化学方程式计算,处理0.142g Cl2至少需NaOH的质量是多少?
中国承诺在2030年前实现碳达峰,2060年前实现碳中和。请回答下列问题。

(1)自然界中CO2的来源有 (任写一点),大气中的CO2过多会引起 效应增强。
(2)“碳捕捉和封存”技术是实现碳中和的重要途径之一。用NaOH溶液喷淋“捕捉”空气中的CO2,可达到消耗CO2的目的,写出该反应的化学方程式 。重庆合川实验基地通过如图1技术将CO2压入地下实现CO2的封存。此封存技术可行的依据是 。
(3)若CO2能合理利用,将会是一种重要的原料。
①CO2与H2在催化条件下反应生成甲醇。反应的化学方程式为CO2+3H2 X+H2O,X的化学式为 。
X+H2O,X的化学式为 。
②CO2可用于食品保鲜,实验测得气体中的CO2体积分数与溶液pH的关系如图2所示。
a.气体中CO2体积分数增大时,造成图示变化的主要原因是溶液中 的浓度增大(填化学式)。
b.智能化食品包装通过颜色变化显示包装内CO2气体含量的变化。举出一种可通过颜色变化用于该智能化包装的物质 。
古往今来,金属材料和制品在生产生活中应用广泛。
(1)三星堆遗址发掘现场出土了华丽的鸟型金饰片,金能被加工成超薄金箔,是因为金具有良好的 ;同时出土的铜头像、青铜神树等表面有锈迹,铜生锈的主要原理是:2Cu+H2O+O2+X═Cu2(OH)2CO3,X的化学式为 。
(2)向氧化铜和铁粉的混合物中加入一定量的稀硫酸,微热充分反应后冷却、过滤得到滤渣和滤液。
①在滤液中加入一枚洁净的铁钉,发现铁钉表面无任何变化,则滤液中一定没有的阳离子是 (填离子符号)。
②向滤渣中再滴入稀硫酸产生气泡,则滤渣中一定含有 (填名称)。
下列有关含碳化合物的说法,正确的是( )
A.一氧化碳和二氧化碳组成元素相同,则二者的化学性质一定相同
B.有机物中一定含有碳元素,则含有碳元素的碳酸氢钠一定属于有机物
C.二氧化碳能使澄清石灰水变浑浊,则澄清石灰水变浑浊一定是通入了二氧化碳
D.某物质在空气中燃烧生成了二氧化碳和水,则该物质一定含有碳、氢元素
防疫情,测体温。体温测量仪功不可没。
(1)传统型﹣﹣体温计。含汞体温计将在2026年起全面禁止生产,因为汞是人体中的 (选填“必需”或“有害”)元素。汞的元素符号是 。
(2)方便型﹣﹣额温枪。某种额温枪的红外温度传感器所用材料含有钽酸锂(LiTaO3)。钽酸锂中锂元素(Li)的化合价为+1价,则钽元素(Ta)的化合价为 价。在惰性气氛中制取钽的原理为:5Na+K2TaF7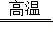 Ta+2KF+5R,则R的化学式为 。
Ta+2KF+5R,则R的化学式为 。
(3)快捷型﹣﹣红外热成像测温仪。该测温仪可实现远距离、多目标、非接触式测温,可用于快速筛查人群中的高温个体。
①该测温仪还可用于 。(填序号,双选)
A.测量物质溶解时的热量变化
B.分析赣江水质
C.探测炼铁高炉是否漏热
D.检测室内甲醛含量是否超标
②该测温仪外壳的塑料是热固性塑料。生活中检验热固性塑料的方法是 。
水是生命之源,是人类宝贵的自然资源。
Ⅰ.节约用水
(1)如图所示图标是我国“国家节水标志”的是 (填字母)。

Ⅱ.水的净化
天然水净化为自来水的主要流程如图所示:

(2)“沉降池”中可用明矾作混凝剂,其化学式为KAl(SO4)n•12H2O,n的值为 。
(3)“吸附池”中常用 (填物质名称)吸附色素和异味。
(4)“消毒池”中常用液氯作消毒剂,发生了反应:Cl2+H2O═HCl+HClO。若用自来水直接配制硝酸银溶液会产生氯化银白色沉淀。写出盐酸与硝酸银溶液反应的化学方程式: 。
Ⅲ.废水处理
(5)废水中氨氮(以NH3形式存在)含量过高,直接排放会导致水体富营养化。次氯酸(HClO)可除去废水中的NH3,发生的反应为:2NH3+3HClO═X+3HCl+3H2O。X的化学式为 。若废水碱性过强(pH>10),NH3的去除率会显著降低,原因是 。
氯化钠是生产、生活中的一种重要化合物,应用很广泛。
Ⅰ.图甲和图乙分别是钠原子和氯原子的原子结构示意图。

(1)图甲中的x= 。
(2)金属钠与氯气反应时,由图乙的结构可知,氯原子容易得到钠失去的1个电子,从而形成最外层有 个电子的相对稳定的氯离子,氯离子用化学符号表示为 。
Ⅱ.如表是氯化钠在不同温度下的溶解度数据。
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
37.3 |
37.8 |
(1)30℃时,将10g氯化钠加入到50g水中,充分搅拌后,所得到的氯化钠溶液属于
(填“饱和”或“不饱和”)溶液。
(2)医用盐水(溶质为NaCl)的溶质质量分数为0.9%,现有200mL该盐水(假定该溶液的密度为1g/mL),其中含NaCl的质量为 g。
(3)学生化学实验活动之一:配制50g质量分数为6%的氯化钠溶液,该实验需要的仪器有药匙、托盘天平、玻璃棒、胶头滴管、 (从下列图中选择写出名称)。

Ⅲ.工业上常用电解饱和食盐水的方法来制取氢氧化钠、氯气和氢气,其化学反应方程式可表示为:xNaCl+yH2O zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
zNaOH+wH2+vCl2↑,若w=v=1,那么x=y=z=
(填数字)。
将下列四种物质放入密闭容器中充分反应,测得反应前后各物质的质量如表。下列说法正确的是( )
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前质量/g |
1 |
10 |
27 |
4 |
| 反应后质量/g |
1 |
a |
0 |
23 |
| A. |
a的值是8 |
| B. |
甲物质一定是该反应的催化剂 |
| C. |
该反应属于分解反应 |
| D. |
反应过程中乙、丁的质量比是5:2 |
一定条件下,在密闭容器内发生某一化学反应,测得反应前后各物质的质量如表所示。
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前的质量/g |
3.2 |
16.8 |
0.8 |
0.1 |
| 反应后的质量/g |
x |
8.4 |
3.0 |
1.0 |
下列说法不正确的是( )
| A. |
x=8.5 |
| B. |
反应中生成丙与丁的质量比为3:1 |
| C. |
乙一定是化合物 |
| D. |
丙和丁的相对分子质量之比可能为22:9 |
大量实验证明,化学反应符合质量守恒定律。
(1)如图是铁钉与硫酸铜溶液反应的实验。
①反应一段时间,观察到的现象是 ;
②该反应的化学方程式是 ;
③溶液中减少的铜元素质量等于反应生成的 的质量。
(2)取足量的铁、锌,各加入相同质量相同溶质质量分数的稀盐酸,完全反应后,铁、锌均有剩余,下列说法正确的是 。
| A. |
生成氢气的质量相等 |
| B. |
生成的氯化亚铁和氯化锌的质量相等 |
| C. |
参加反应的铁和锌的质量相等 |
| D. |
参加反应的稀盐酸中HCl的质量相等 |
(3)经计算3g镁和100g质量分数7.3%的盐酸充分反应可生成氢气0.2g,但经实验测定,生成氢气的质量大于0.2g,则可能的原因是过量的镁与 发生反应。

我国力争在2060年前实现"碳中和"(二氧化碳的排放与吸收平衡,实现"零排放"),保护环境。实现"碳中和"通常可采取如下措施:
(1)碳减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:2B+6X  2B(OH) 3+3H 2↑,则X的化学式为 ,B(OH) 3中B的化合价为 。
2B(OH) 3+3H 2↑,则X的化学式为 ,B(OH) 3中B的化合价为 。
(2)碳"捕捉"与封存:碳"捕捉"可用氢氧化钠溶液吸收空气中的二氧化碳,该反应的化学方程式为 。
(3)碳转化:一定条件下,可将二氧化碳在催化剂表面转化成某种有机清洁燃料,其反应原理如图所示,该反应的化学方程式为 。

甲、乙、丙、丁四种物质混合后,在一定条件下充分反应,测得反应前后各物质的质量如表所示。关于此反应说法正确的是( )
| 物质 |
甲 |
乙 |
丙 |
丁 |
| 反应前质量/g |
70 |
15 |
6.25 |
8.75 |
| 反应后质量/g |
35 |
7.5 |
48.75 |
8.75 |
| A. |
丁一定是该反应的催化剂 |
| B. |
参加反应的甲和乙的质量之和一定等于生成的丙的质量 |
| C. |
甲一定是化合物,乙一定是单质 |
| D. |
该反应可能是分解反应 |
实验室用浓盐酸和二氧化锰来制取氯气,反应的化学方程式为:MnO 2+4HCl(浓)  X+Cl 2↑+2H 2O,则X的化学式为( )
X+Cl 2↑+2H 2O,则X的化学式为( )
| A. |
MnCl 2 |
B. |
ClO 2 |
C. |
MnCl 4 |
D. |
HClO |
阅读下面科普短文。
碳元素是人类接触和利用最早的元素之一。由碳元素组成的单质可分为无定形碳、过液态碳和晶形碳三大类,如图1。

石墨是制铅笔芯的原料之一,在16世纪被发现后,曾被误认为是含铅的物质。直到18世纪,化学家将石墨与KNO3共熔后产生CO2,才确定了它是含碳的物质。
碳纤维既有碳材料的固有本质特性,又有纺织纤维的柔软可加工性,综合性能优异。目前,我国已形成碳纤维生产、碳纤维复合材料成型,应用等产业链,碳纤维复合材料应用领域分布如图2。
科学界不断研发出新型碳材料,碳气凝胶就是其中一种。碳气凝胶具有优良的吸附性能,在环境净化中发挥重要作用。我国科研人员在不同温度下制备了三种碳气凝胶样品,比较其对CO2的选择性吸附性能。他们在不同压强下测定了上述样品对混合气体中CO2吸附的选择性值,实验结果如图3。图中选择性值越高,表明碳气凝胶对CO2的选择性吸附性能越好。
随着科学技术的发展,碳材料的潜能不断被激发,应用领域越来越广泛。
依据文章内容回答下列问题:
(1)金刚石属于 (填序号)。
A.无定形碳
B.过渡态碳
C.晶形碳
(2)石墨与KNO3共熔,能发生如下反应,配平该反应的化学方程式:5C+4KNO3
K2O+ N2↑+ CO2↑。
(3)由图2可知,我国碳纤维复合材料应用占比最高的领域是 。
(4)判断下列说法是否正确(填“对”或“错”)。
①石墨是一种含铅的物质 。
②碳材料其有广阔的应用和发展前景 。
(5)对比图3中三条曲线,得到的实验结论是 。