下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是:
| A.氢氧化铜和稀硫酸 | B.氢氧化钠和稀盐酸 |
| C.氢氧化钙溶液和少量二氧化碳 | D.氢氧化钾和硝酸钠 |
氧化镁在医药、建筑等行业应用广泛.硫酸镁还原热解制备高纯氧化镁是一种新的探索.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如下:
(1)MgCO3与稀硫酸反应的化学方程式为 ;
(2)加入H2O2氧化时,发生反应的化学方程式为(已经配平,X属于常见的化合物): ,则X的化学式为 ;
,则X的化学式为 ;
(3)NH3·H2O是氨水的主要成分,溶液显 性,加入氨水时,溶液的PH值 (填“增大”、“减少”或“不变”),当PH≈4时,会产生红褐色沉淀,则滤渣2 的成分是 (填化学式)。
(4)通常用PH试纸测定溶液的PH值,其操作方法是 。
(5)煅烧过程存在以下反应:木炭和硫酸镁在高温下除得到氧化镁外,还得两种气体,一种会造成酸雨,另一种大量排放则会引起温室效应。请写出该反应的化学方程式: 。
下列图象分别表示对应的四种操作过程,其中表示正确的图像是
| A.①加热氯酸钾和二氧化锰固体至质量不再减轻,固体中二氧化锰的质量 |
| B.②向pH=1的硫酸溶液中逐滴加入pH=13的氢氧化钠溶液 |
| C.③某温度下,向一定量的水中持续加入食盐并不断搅拌,所得溶液的质量分数 |
| D.④等质量的锌、铁与足量的同种稀硫酸反应,产生氢气的质量M与反应时间 |
小明同学在实验室中测定某酸性溶液的pH,他的实验操作如下:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测试液于pH试纸上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较
| A.偏低 | B.偏高 | C.不变 | D.无法判定 |
某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,利用数字化传感器测得烧杯中溶液pH的变化图像,如图所示。下列说法正确的是()
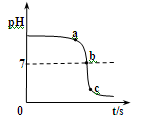
| A. | 图中c点所示溶液呈碱性 |
| B. | 图中a点所示溶液中,含有的溶质是 和 |
| C. | 该实验是将氢氧化钠溶液逐滴滴入到盛有硫酸的烧杯中 |
| D. | 由a点到b点的pH变化过程证明酸和碱发生了中和反应 |
推理是化学学习的一种方法,以下推理正确的是
| A. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 |
| B. | 碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的 一定大于7 |
| C. | 在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价 |
| D. |
稀有气体元素的原子最外层电子数为8(氦除外),因此微粒
 一定是稀有气体元素的原子 一定是稀有气体元素的原子
|
下列曲线能正确表达对应的反应或过程的是()

| A. | 向一定量的水中加入生石灰 | B. | 红磷在装有空气的密闭容器中燃烧 |
| C. | 向一定量的烧碱溶液中加入盐酸 | D. | 向饱和 溶液中加入 固体 |
下面图示为某些物品对应的pH范围,其中显弱碱性的是()

| A. | 小苏打 | B. | 杨梅 | C. | 栗子 | D. | 菠萝 |
化学与生活密切相关,下列叙述中正确的是
| A. | 胃酸过多的人应少饮葡萄汁(葡萄汁的 为3.5---4.5) |
| B. | 为了个人卫生,应全部使用一次性的木筷和餐盒 |
| C. | 人体缺锌会引起生长发育缓慢,因此锌元素摄入得越多越好 |
| D. | 铵态氮肥与草木灰混合使用可以明显提高肥效 |
下图体现了稀盐酸和氢氧化钠溶液反应的实质,请回答有关问题:
(1)在上图C、D中的圆圈内填入适当的化学式或离子符号:C中_______、_______,D中________;
(2)用化学方程式表示图中所体现的化学反应______________________________;
(3)以上变化的反应类型是_______________。
下列物质之间不能发生化学反应的是
| A. | 石灰水与稀盐酸 | B. | 铜与硝酸银溶液 |
| C. | 银与稀硫酸 | D. | 二氧化碳与水 |
测定人体内或排出的液体
,可以帮助人们了解身体的健康状况,人体内的一些体液近似
如下:
| 液体 |
胃液 |
胰液 |
胆汁 |
血浆 |
| 0.9-1.5 |
7.5-8.0 |
7.1-7.3 |
7.35-7.45 |
下列液体中,碱性最强的是
| A. |
胃液 |
B. |
胰液 |
C. |
胆汁 |
D. |
血浆 |
2015年苏州市初中化学实验操作考查内容为"溶液酸碱性的检验"。请根据实验回答下列问题。
(1)测得碳酸饮料的pH7(填"〈"或"="或"〉")。
(2)下列使用pH试纸的方法中,正确的是(填序号)。
| A. | 将pH试纸剪成几段使用 |
| B. | 将pH试纸直接插入待测液中 |
| C. | 将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上 |
| D. | 将pH试纸湿润后放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸上 |
E.读数时,在30秒内将pH试纸呈现的颜色与标准比色卡对照
(3)本次实验中滴管使用出现了如图6~图9所示的四种常见错误操作。请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法。
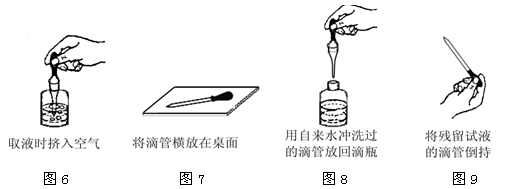
(4)使用白色点滴板完成实验有显色明显、便于对比、(填一项)等优点。
形成化学观念是化学学习的任务之.下列说法中,错误的是
| A.pH=0的溶液一定是中性溶液 |
| B.元素周期表中原子序数等于该元素原子核内的质子数 |
| C.化学变化的过程中常会伴随能量变化 |
| D.复分解反应前后各元素的化合价均未发生变化 |
(7分)中和反应是中学化学中重要的学习内容,其在日常生活和工农业生产中有广泛的应用。
(1)下图表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH的变化曲线。请从曲线图中获取信息,回答下列问题:
①图1图象表示盐酸和氢氧化钠溶液发生反应过程中溶液的pH变化。进行该反应的实验操作是按照图2中的 (填甲或乙)图所示进行。
②曲线上M点表示 。
③向烧杯中倾倒20g质量分数为4.00%的氢氧化钠溶液,滴入3滴酚酞试液,振荡,再逐滴滴入质量分数为3.65%的稀盐酸,边滴边振荡,直至溶液刚好变为色为止,共用去稀盐酸20g,则反应后溶液中溶质质量分数为 (结果精确到0.1%)。
(2)为证明中和反应是放热反应,某小组进行了如图所示的实验操作:
根据上图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应。乙同学认为:甲同学得出这个结论的依据不科学,理由是 。
(3)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、
D、E的五只烧杯中各装入36.5g溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g 20%的氢氧化钠溶液,最后测量其温度,数据记录如下:
实验结论:影响中和反应放出热量多少的因素 。
交流反思:反应后,烧杯内溶液pH最小的是 (填烧杯编号)。