化学是以实验为基础的科学。通过下列实验可以得出对应的结论,其中不合理的是
| A.甲实验中黄铜片(铜的合金)能在铜片上刻画出痕迹说明铜合金的硬度比铜大 |
| B.乙实验可以说明分子是运动的 |
| C.丙实验既可以说明二氧化碳易溶于水生成碳酸,又可说明二氧化碳显酸性 |
| D.丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
下列比较金属活动性强弱的实验设计、现象和结论均正确的是
| 选项 |
实验设计 |
现象 |
结论(金属的活动性) |
| A |
将铝丝放人硫酸铜溶液中 |
无现象 |
Cu>Al |
| B |
分别将相同形状的镁条和铝条点燃放入盛氧气的集气瓶中 |
镁条燃烧得更剧烈 |
Mg>Al |
| C |
分别将锌粉与铁丝放入相同浓度的稀盐酸中 |
锌粉产生气泡的速率比铁丝快 |
Zn>Fe |
| D |
分别将铁丝与铜丝放入相同浓度的稀盐酸中 |
铁丝表面产生气泡,铜丝无现象 |
Fe>Cu |
某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如下图所示的实验操作。其中可以达到实验目的的组合是( )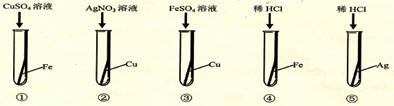
| A.②③ | B.②④ | C.④⑤ | D.①③ |
根据金属活动性顺序分析,下列描述或判断正确的是
| A.金属钾能与硫酸锌溶液发生化学反应得到金属锌 |
| B.金属铁与硫酸溶液反应后所得溶液的质量比原溶液的质量增大 |
| C.在常温下,铝比镁更容易与氧气发生化学反应 |
| D.金属铜与氯化银反应得到金属银 |
下列有关实验事实不能用金属活动性顺序解释的是
| A.铁能将铜从硫酸铜溶液中置换出来 |
| B.铝制品抗腐蚀能力比铁制品强 |
| C.不能用金属铜与稀硫酸反应制氢气 |
| D.相同条件下,镁和锌与稀硫酸反应的剧烈程度 |
有等质量的
两金属,相对原子质量
,将
放入质量分数为15%的稀硫酸中,
放入质量分数为15%的稀盐酸中,在反应中
均为正二价,产生氢气的质量随反应时间变化曲线如右图。下列说法正确的是()
| A. |
产生氢气的速率 |
B. |
反应后 一定都有剩余 |
C. |
消耗的稀硫酸和稀盐酸质量一定不相等 |
D. |
消耗 的质量一定小于 的质量 |
为从废铜屑中得到较纯的单质铜,某探究小组设计了如下方案。有关说法正确的是
| A.若X是铁,第③步反应还会生成氯化铁 |
| B.X还可以是Zn,但不能是Ag |
| C.仅用第②③步操作也能达到实验目的 |
| D.向第②步反应后的溶液中加入硝酸银溶液,若产生白色沉淀即证明稀盐酸过量 |
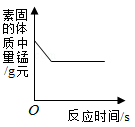
下列图像能正确反映对应变化关系的是
 |
 |
 |
 |
| A.一定质量的碳酸钠中不断加入盐酸 |
B.向一定质量的铜锌合金样品中不断加入稀硫酸 |
C.用酒精灯加热一定质量的高锰酸钾固体 |
D.向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液 |
A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应。相同条件下,C、D能与稀盐酸反应产生H2,且D比C反应剧烈。则四种金属的活动性由强到弱的顺序是( )
A.A、B、C、D B.B、A、C、D C.D、C、A、B D.D、C、B、A
对物质的性质进行比较归纳,有利于更好的学习化学。下列对物质性质的归纳中,正确的是
A.H2、O2、CH4都具有可燃性
B.H2、C、CO都能和CuO发生置换反应
C.石墨、木炭、活性炭都具有吸附性
D.Fe、Al、Cu都能和AgNO3溶液发生置换反应
为了验证铁、铜两种金属活动性大小,某同学设计了如图所示的实验,为了达到试验目的,溶液应该选择
| A.稀硫酸 | B.硫酸镁溶液 | C.氯化钠溶液 | D.植物油 |
现有一种固体粉末状样品,已知该样品由氧化铜和铁组成。取样品少许,加入一定量的稀硫酸,待反应停止后过滤,得到滤渣和滤液。向滤液中加入一根洁净的铁丝,铁丝表面无明显变化。关于该实验有如下说法,其中错误的有几个
① 该样品的颜色为黑色;
② 向样品中加入稀硫酸后,一定有气体生成,且液体颜色不变;
③ 滤渣中一定有铜,不一定有铁;
④ 滤液中含有硫酸铜和硫酸亚铁;
⑤ 滤液中溶质只有硫酸铁。
| A.2个 | B.3个 | C.4个 | D.5个 |
下列反应中属于置换反应的是
| A.CO+CuO △ Cu+CO2 | B.Ca(OH)2+CO2="=" CaCO3↓+H2O |
| C.SO2+2NaOH="=" Na2SO3+H2O | D.Zn+CuSO4===ZnSO4+Cu |
某同学探究金属单质的活动性时发现 、 都能跟稀硫酸反应,而 不能; 能在X的盐溶液中置换出 .则它们的金属活动性顺序为()
| A. | > > | B. | > > | C. | > > | D. | > > |