金属活动顺序在工农业生产和科学研究中有重要应用
(1)铝比较活泼,为什么铝制品却有较好的搞腐蚀性能?
(2)农业上不能用铁制容器配制波尔多液(含硫酸铜),请用化学方程式解释。
(3)探究实验:分别将不同量的锌粉加入一定量的
。混合溶液中,充分反应后过滤。以下是不同情况下对固体或滤液成分的探究。
①若向所得固体上滴加盐酸有气泡产生,则该固体含有金属为 。
②猜想:滤液中溶质为
,请分析猜想不合理的原因。
某金属冶炼厂的工业废渣中含有泥沙和某些单质,其中单质含有铜、锌和少部分硫。现欲回收铜和锌,并对硫进行处理,主要流程如下图所示:

(1)在废气
中,一定含有的有害气体是(填化学式)。操作①的操作名称是。
(2)溶液
中含有的溶质是(填化学式)。
(3)写出加入
后发生的化学方程式(写出其中之一即可)。
在硫酸铜溶液中加入一定量的锌粉和铁粉充分反应后,过滤可得到一些固体.向该固体中加入少量稀硫酸,可观察到有气体产生.下列对该固体的叙述正确的是
①一定有锌、②一定有铁、③一定有铜、④可能有锌、⑤可能有铁、⑥可能有铜.
| A.①、②、③ | B.②、③、④ | C.③、④、⑤ | D.①、②、⑥ |
某溶液含有Cu(NO3)2和AgNO3,现向其中加入一定量的锌粉,参加反应的锌的质量与溶液中金属离子种类的关系如图所示。下列说法不正确的是
| A.a~b间(不含两点)的溶液中金属离子为Zn2+、Ag+、Cu2+ |
| B.c~d间(不含两点)的溶液中金属离子为Zn2+、Cu2+ |
| C.当参加反应的锌的质量为m3时,溶液中金属离子为Zn2+ |
| D.当参加反应的锌的质量分别为m1、m2时,溶液中Cu(NO3)2的质量分数相等 |
(5分)Ti是一种重要的航天金属材料。某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究。过程如下:
【提出假设】a.Ti金属活动性比Al强。 b.Al金属活动性比Cu强。
【查阅资料】钛能与盐酸反应。
【实验设计】同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象。
【操作分析】三种金属加入盐酸前都先用砂布将表面擦光亮,其目的是 。
A.除去氧化膜,利于直接反应
B.使表面光亮,易观察现象
C.使反应金属温度相同,易反应
【实验现象】
| 金 属 |
Ti |
Al |
Cu |
| 与盐酸反应现象 |
反应缓慢 |
反应剧烈 |
无明显现象 |
【实验结论】(1)原假设中 不正确(填“a”、“b”或“a与b”)。
(2)三种金属的金属活动性由强至弱的顺序为 。
【结论应用】能否用铝制容器来盛装波尔多液(含硫酸铜), (填“能”或“否”);理由是 。
现有一种固体粉末状样品,已知该样品由氧化铜和铁组成。取样品少许,加入一定量的稀硫酸,待反应停止后过滤,得到滤渣和滤液。向滤液中加入一根洁净的铁丝,铁丝表面无明显变化。关于该实验有如下说法,其中错误的有几个
① 该样品的颜色为黑色;
② 向样品中加入稀硫酸后,一定有气体生成,且液体颜色不变;
③ 滤渣中一定有铜,不一定有铁;
④ 滤液中含有硫酸铜和硫酸亚铁;
⑤ 滤液中溶质只有硫酸铁。
| A.2个 | B.3个 | C.4个 | D.5个 |
向一定量硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图。下列说法正确的是
| A.a点所得固体为银和铁 |
| B.b点所得溶液中的溶质为硝酸银、硝酸亚铁和硝酸锌 |
| C.c点所得固体为银、铁和锌 |
| D.d点所得溶液中的溶质为硝酸锌 |
一定质量的锌、铁分别和等质量、等浓度的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法正确的是
| A.t1时,产生氢气的质量锌比铁小 |
| B.t1时,产生氢气的速率铁比锌大 |
| C.t2时,参加反应锌的质量与铁相同 |
| D.t2时,锌、铁消耗的盐酸质量相同 |
金属材料与人类的生产和生活密切相关。请回答:
(1)下列用品中,主要利用金属导电性的是(填字母)
A.铂金饰品 B.铁锅 C.铝导线
(2)为了验证铝、铜、银三种金属的活动性顺序,设计了下列四种方案,其中可行的是(填 序号)
①将铝、银分别浸入到硫酸铜溶液中
②将银分别浸入到硫酸铝、硫酸铜溶液中
③将铜、银分别浸入到硫酸铝溶液中
④将铜分别浸入到硫酸铝、硝酸银溶液中
(3)在氯化铜和氯化亚铁的混合溶液中加入一定质量的镁粉,充分反应后过滤,得到滤渣和滤液。
①滤液中一定含有的溶质是(填化学式);
②向滤渣中滴加稀盐酸,有气泡产生,则滤渣中一定含有的物质是(填化学式)。
(4)某钢铁厂每天需消耗4900t含
76%的赤铁矿石,该厂理论上可日产含
98%的生铁的质量是t。
某学生为了验证锌、铁、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Zn分别加入到FeSO4、CuSO4溶液中;④将Fe分别加入到ZnSO4、CuSO4溶液。其可行的是
| A.①或② | B.①或④ | C.②或③ | D.③或④ |
如图所示,在等臂杠杆的两端各系一只等质量等体积的铁球,这时杠杆平衡。然后将两球分别浸没在稀硫酸和硫酸铜溶液中片刻,下列说法正确的是
| A.左边烧杯中溶液质量减少 |
| B.杠杆向右倾斜 |
| C.杠杆仍保持平衡 |
| D.右边烧杯中溶液的质量增加 |
某兴趣小组的同学从实验室收集到一桶含有FeSO4、CuSO4的废液,他们想从中回收金属铜和硫酸亚铁晶体,设计了如下实验方案。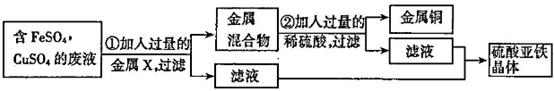
(1)写出步骤①中反应的化学方程式___________________。
(2)步骤②中,加入过量稀硫酸的目的是什么?____________________
(3)从滤液中获得硫酸亚铁晶体采用的方法是什么?____________________
将相同体积、相同溶质质量分数的稀盐酸,分别加入到等质量、颗粒大小相同的X、Y、Z三种较活泼金属中(金属完全反应〕,生成H2的质量与反应时间的关系如下图所示。下列说法中正确的是
| A.三种金属的活动性顺序为Y>X>Z |
| B.产生氢气的速率顺序为X>Y>Z |
| C.消耗稀盐酸的质量顺序为Z>Y>X |
| D.相对原子质量由大到小的顺序为X>Y>Z |
金属在生产和生活中有广泛的应。
(1)下列金属制品中,利用金属导电性的是 填字母序号)。
A.黄金首饰 B.铝蒸锅 C.铜导线
(2)铁制品在沙漠地区不易锈蚀的原因是 ;
(3)工业上用一氧化碳和赤铁矿(Fe2O3)炼铁反应的化学方程式为 ;
(4)某厂排放的废水中含有硫酸铜,将废水处理可得到铜(产品F)和铁红(氧化铁,产品G)两种产品.过程如下图所示(废水中的其他物质不参与反应):
过程①中发生反应的化学方程式为_______________ 。
A-G七种物质中含铁元素的有 (填字母代号)
把 三种金属分别放入稀盐酸中, 溶解并有气泡产生, 不反应,取过量 放入 和 的混合溶液中充分反应后过滤,经检验,滤渣中只有 .则 三种金属的活动性由强到弱的顺序是()
| A. | B. | C. | D. |