下列说法中正确的是( )
A.质量相等的氧化铁和四氧化三铁中,氧元素的质量比为80:87
B.碳酸钠和氯化钠的固体混合物22.3g,其中含氧元素4.8g,则该混合物中氯元素的质量为7.1g
C.某氮的氧化物中,氮、氧元素的质量比为7:12,则该氧化物的化学式为N2O5
D.某过氧化氢溶液中氢元素与氧元素的质量比为2:17,向38g该溶液中加入1g二氧化锰,充分反应后,生成2g氧气
(1)右图是某品牌牙膏标签的部分内容,请用化学用语填空:

①磷元素的符号 ;
②二氧化硅的化学式 ;
③硝酸根离子 ;
④2个氧原子 。
(2)为减少龋齿,制造口香糖时常用木糖醇(C5H12O5)代替蔗糖。一个木糖醇分子中有______个原子,木糖醇的相对分子质量为 ,其中碳、氢、氧元素的质量比为 ,15.2g木糖醇中碳元素的质量为______g。
葡萄糖(化学式为C6H12O6)在生物学领域具有重要地位,是活细胞的能量来源和新陈代谢中间产物,即生物的主要供能物质.植物可通过光合作用产生葡萄糖.
计算葡萄糖的相对分子质量
计算葡萄糖中各元素的质量比
计算葡萄糖中碳元素的质量分数
计算葡萄糖中各元素的原子个数比.
亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)的化合价为
| A.+3 | B.+2 | C.+5 | D.+4 |
2011年科学家发现了一种化学式为N(NO2)3的新型火箭燃料。下列关于N(NO2)3的说法不正确的是( )
A.N(NO2)3由两种元素组成
B.1个N(NO2)3分子由4个N原子、6个O原子构成
C.N(NO2)3的相对分子质量是152
D.N(NO2)3中N、O元素的质量比为2:3
人体缺乏维生素C(简写“Vc”)会患坏血病.右图所示为某种“维生素C”说明书的一部分,请回答:

(1)“Vc”中碳、氢、氧三种元素质量比为
(2)若正常成人每天对“Vc”的最低需要量为60mg:当这些“Vc”完全来自右图的“维生素C”时,则每次服用“维生素C”至少 片.
下列元素的化合价不正确的是
A.K2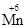 O4 O4 |
B.Ca( O)2 O)2 |
C. 60 60 |
D.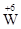 O3 O3 |
一定质量的某有机化合物完全燃烧,生成2.2gCO2和1.8gH2O,另取3.2g该有机化合物在O2中完全燃烧,消耗4.8gO2,该有机化合物的化学式可能是( )
A.C2H4B.CH4OC.CH4D.C2H4O
天然气广泛应用于生产生活,其主要成分是甲烷(CH4)。
Ⅰ.天然气是重要的能源
(1)天然气属于 (填“可再生”或”不可再生”)能源。
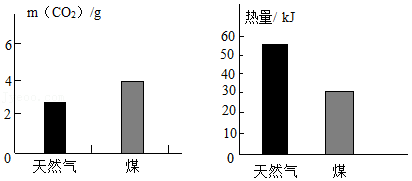
(2)室温下,充分燃烧1g天然气和1g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有 。
(3)甲烷可直接应用于燃料电池,电池工作时的能量转化方式为 。
Ⅱ.天然气是重要的化工原料
(4)甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2。该反应的化学方程式为 。
(5)甲烷无氧催化重整可获得碳氢化合物X,X的相对分子质量为106,且碳、氢元素的质量比为48:5,则X的化学式为 。
甲醇是一种无色、有特殊香味、易挥发的液体。已知甲醇由碳、氢、氧三种元素组成,其中氢元素的质量分数为12.5%,氧元素的质量分数为50%;一个甲醇分子中含有1个氧原子。
回答下列问题:
(1)甲醇的相对分子质量是 ;
(2)一个甲醇分子中含氢原子的个数是 。
氢气的储存是科学研究热点之一。X是一种储存氢气的材料,取11.2g X在O 2中完全燃烧后只生成8.0g CuO、8.0g MgO。
(1)上述燃烧过程中消耗O 2的质量为 克。
(2)通过计算求X中各元素的原子个数比。(写出计算过程)
按要求填空:
(1)溶洞里形态各异的钟乳石的形成过程可简单理解为:石灰岩长时间缓慢的“溶解”在水中,水在滴落时又缓慢的生长出钟乳。钟乳石生长的化学方程式为 ,其反应类型为 。
(2)汽车尾气中含有多种氮的氧化物和一氧化碳,对空气有污染作用。有人设计在尾气处加装高效催化剂,将其转化成无污染的一种单质和一种化合物。则生成的化合物的化学式为 ,反应中化合价降低的元素符号是 。
(3)侯德榜是我国杰出的化学家,他发明的联合制碱法大大提高了原料的利用率。联合制碱的主要反应原理:向饱和的食盐溶液通入过量的氨气(易溶于水的碱性气体)和二氧化碳气体,反应后分离出碳酸氢钠。反应方程式为:NaCl(饱和)+NH3+H2O+CO2=NaHCO3+NH4Cl
向饱和的食盐溶液是先通入氨气还是二氧化碳? (填化学式)。该反应属于复分解反应,该反应能够发生的依据是 。
(4)已知某铁的氧化物可表示为FexOy=aFeO•bFe2O3.经测:15.2克的某铁的氧化物中铁的质量为11.2克。则x:y= ,a:b= (均填最小整数比)。
白酒中溶质的主要成分是酒精(C2H5OH),下列说法正确的是( )
A.酒精中碳、氢、氧元素的质量比为2:6:1
B.酒精的相对分子质量为46g
C.酒精属于有机物
D.酒精是由2个碳原子、6个氢原子和1个氧原子构成的
科学家近日揭示了一种冰的新固态阶段,这是迄今所知道的密度最小的冰.这种新形态被称为“冰ⅩⅥ”,是目前发现的冰的第16个固态阶段,它有着像笼子一样的结构.下列关于这种“冰ⅩⅥ”的说法正确的是
| A.物理性质与普通冰完全相同 | B.分子间没有间隔 |
| C.氢、氧元素的质量比为1:8 | D.水分子不再运动 |
空气是人类最宝贵的自然资源。空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应.图1是以空气和其他必要的原料合成氮肥(NH4HCO3)的流程.请按要求回答下列问题:

(1)步骤①中可利用氮气和氧气的 不同分离出氮气和氧气。
(2)写出步骤②中发生反应的化学式表达式 。
(3)图2是化肥碳酸氢铵包装袋上的部分说明:碳酸氢铵具有的性质是 (填字母).
A.易溶于水 B.有挥发性 C.受热易分解
(4)这种化肥含氮量是否达到16%,化肥中碳酸氢铵的含量是多少?带着这些问题,兴趣小组的同学取了一些化肥样品,进入实验室。
【查找资料】①碱石灰能够吸收水和CO2,但是不吸收NH3。
②浓硫酸能吸收NH3但是不吸收CO2。
③氨气溶于水形成氨水
【性质探究】该同学设计了如下的实验装置:

①用A装置给碳酸氢铵加热,装药品前,必须进行的一步操作是 。
②取适量碳酸氢铵加入试管,连接A、C、E装置,加热,E中的现象是 。
③连接A、B装置,继续加热,观察到试管口的现象是 ,B中的现象是 。
④碳酸氢铵在受热时发生反应的化学式表达式是 。
【含量分析】将装置A、C、D依次连接,加入20g化肥样品,加热至A中固体完全消失。
她称量装置D的质量如表:
| 实验前D装置的质量 |
149g |
| 实验后D装置的质量 |
152.4g |
⑤由此分析得知:反应中产生氨气的质量为 g。
⑥通过反应的表达式可以知道:氨气中氮元素全部来自于碳酸氢铵(假设杂质中不含氮元素),请计算此化肥含氮元素质量分数为 。
⑦请计算此化肥中碳酸氢铵的纯度 。
⑧ 千克的硝酸铵(NH4NO3)和这袋化肥的含氮元素质量相等.