如图是铈元素在元素周期表中的信息以及A、B、C、D四种粒子的结构示意图,请根据图示回答。

(1)铈元素的原子序数是 。
(2)A、B、C、D四种粒子中易失去电子的是 (填字母)。
(3)B、C属于不同种元素的原因是 。
(4)A、B、C、D四种粒子中具有相对稳定结构的是 (填字母)。
科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据如图所示按要求回答问题:

(1)图(甲)是氯元素在元素周期表中的部分信息,氯元素的相对原子质量是 。
(2)图(乙)是某原子的结构示意图,则X的数值是 ,该原子形成的阳离子符号是 ,该元素与氯元素组成的化合物的化学式是 。
(3)图(丙)是某化学反应的微观示意图,请写出该反应的化学方程式 。
图1是铝元素在元素周期表中的相关信息,图2是几种微粒的结构示意图。
回答下列问题:
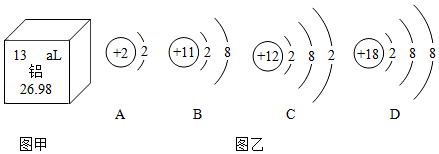
(1)铝的相对原子质量为 。
(2)图2中,B所对应的元素位于元素周期表的第 周期。
(3)铝元素和镁元素的本质区别是 。
(4)图2中,属于相对稳定结构的原子是 (填字母序号)。
如图是元素周期表的一部分。
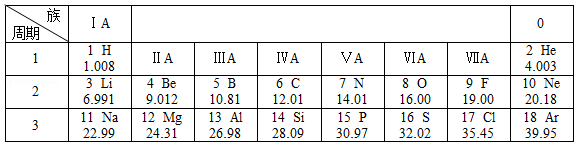
(1)写出空气中含量最多元素的符号 。
(2)如图是A、B、C三种粒子的结构示意图,其中属于同种元素的是 (填序号),A粒子与第二周期 元素的原子化学性质相似。
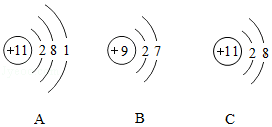
(3)第8号元素的原子在化学反应中易 (填“得到”或“失去”)电子,则第8号元素和第13号元素形成的化合物的化学式是 。
(4)我国科学家张青莲教授主持测定的铟等多种元素的相对原子质量已成为国际标准。关于相对原子质量,下列叙述错误的是 (填序号)。
A.相对原子质量与原子质量没有什么差别
B.由于原子的质量太小,使用不方便,所以采用相对原子质量
C.两种原子的质量之比等于它们的相对原子质量之比
D.采用相对原子质量后,就增大了原子的质量
联合国将2019年定为国际化学元素周期表年。下图是元素周期表中1~18号元素的原子结构示意图,请回答下列问题:
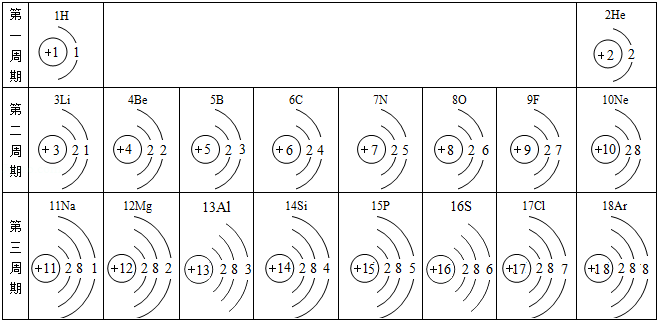
(1)原子序数为9的元素属于 (填“金属”或“非金属”)元素。
(2)具有相似化学性质的元素是 (填数字序号)。
①He、Mg ②O、S ③H、Na ④Cl、Ar
(3)元素M是第三周期中的一种元素,与氯元素形成的化合物的化学式为MCl3,则M的元素符号为 。
(4)同周期元素,随原子序数的增加,各元素的原子 依次增加
铝是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。
(1)人类冶炼和使用金属铝的时间较晚,可能是因为 (填字母)。
a.地壳中铝元素含量少
b.冶炼铝的技术要求高
(2)用铝锂合金制造“神舟号”航天飞船的一些部件,主要是利用其强度高、耐腐蚀和 (写一条)等性质。高温下,铝与Li2O反应可置换出金属锂,写出该反应的化学方程式: 。
(3)用砂纸去除铝片表面的氧化膜。将其浸入硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质析出,并有气泡产生,经检验气体为氢气。
①写出生成红色物质的化学方程式: 。
②硫酸铜溶液中的阳离子有 (填离子符号)。
(4)原子簇是若干个原子的聚集体,有望开发成新材料。某铝原子簇由13个铝原子构成,其最外层电子数的总和为40时相对稳定。写出该稳定铝原子簇的微粒符号: 。
[铝原子的结构示意图为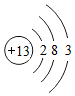 ]
]
2019年为“元素周期表年”,元素周期表是学习和研究化学的重要工具。
(1)原子序数为1~18的元素在元素周期表中的位置如下表所示(图1)。
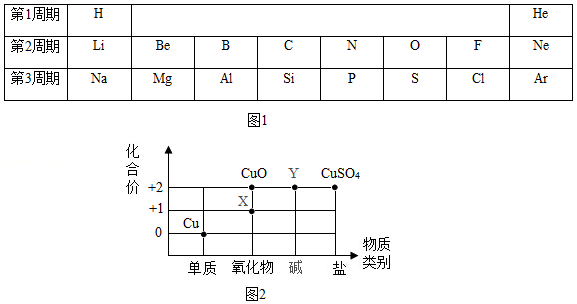
①Al属于 (填“金属”或“非金属”)元素,其原子的核电荷数为 。
②Na原子的结构示意图为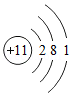 ,则钠离子的核外电子数为 。
,则钠离子的核外电子数为 。
③周期表中磷元素的有关信息为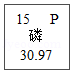 ,图中“30.97”所表示的含义是 。
,图中“30.97”所表示的含义是 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图(图2)。
①写出物质X的化学式: 。
②写出由物质Y转化为CuSO4的化学反应方程式: 。
华为公司作为我国高新科技的代表,一直致力于核心技术的研发,其自主研制的“麒麟”芯片已达到世界领先水平,该芯片的主要材料为高纯度的单质硅。请回答以下与硅有关的问题:
(1)如图是硅元素在元素周期表中的相关信息及其原子结构示意图。硅元素属于 (填“金属”或“非金属”)元素,硅原子的最外层上有 个电子;
(2)工业上制粗硅原理:二氧化硅与碳单质在高温条件下生成单质硅和一种可燃性气体物质,请写出该反应的化学方程式: 。
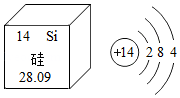
如图中A、B、C、D为四种元素原子的结构示意图。请回答下列问题:
(1)A、C两种原子相互结合形成的化合物的化学式为 (任写一种)。
(2)D中x= 。
(3)写出B、C两种原子形成的化合物BC2的名称 。
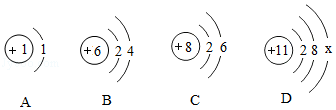
学习化学要建立元素观、粒子观、变化观和分类观,请用所学化学知识回答下列问题: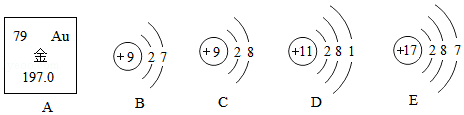
(1)从图A中可知,金的相对原子质量为 。
(2)B、C、D、E所示粒子共表示 种元素,其中 (填序号)与E化学性质相似。
2020年6月23日,长征三号乙运载火箭将北斗三号最后一颗组网卫星成功送入预定轨道,我国北斗导航地位将进一步提升。从化学视角回答下列问题:
(1)卫星制造使用了黄金、钛合金,其中用作天线的是 。使用黄金制作卫星的电子元件,利用了金的什么化学性质? (填序号)。
A.光泽好
B.耐磨、易加工
C.容易导电
D.很难被氧化
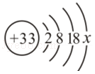
(2)卫星的太阳能电池帆板用先进的砷化镓主板和铝合金边框制成,砷(As)原子的结构示意图如图,其中x= 。铝合金比纯铝具有的优势是 (写出1条即可)。
(3)运载火箭用偏二甲肼(C2H8N2)作燃料,N2O4作氧化剂。偏二甲肼中C、H、N的质量比为 (填最简整数比)。火箭发射时,燃料与氧化剂剧烈反应放出大量的热,并生成对空气无污染的两种氧化物和一种单质,这种单质的化学式为 ,两种氧化物中相对分子质量较大的是 。
镁是一种常见的金属,请回答下列问题。
(1)组成和结构:
①从宏观看,镁是由 组成的。
②从微观看,据如图分析,镁位于元素周期表中第 周期,在化学反应中容易 (填“得到”或“失去”)电子形成镁离子。
(2)性质和变化:
①镁具有可燃性,在空气中燃烧的化学方程式是 。
②向镁条中滴加稀盐酸,产生大量气泡,此反应是一个 (填“放热”或“吸热”)反应。
③把一定量的镁放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,滤液为无色,则滤液中的溶质是 (填化学式,下同),滤渣的组成可能是 。

请用化学用语填空:
(1)保持过氧化氢化学性质的最小粒子是 。
(2)某粒子的结构示意图为 ,该粒子的符号是 。
,该粒子的符号是 。
眉山市岷江河畔的东坡湿地公园,环境优美,是市民休闲的场所。请用所学的化学知识回答下列问题:
(1)走进湿地公园,花香四溢,从微观上解释是因为 。
(2)经环保部门鉴定,湿地公园的空气质量优,空气中基本不含SO 2、NO 2、 等有害气体。
(3)湿地公园的湖水清澈见底,用化学用语表示4个水分子 。
(4)我们可以滴加 来鉴别该公园中的湖水是硬水还是软水。湖水中含有Na +、Mg 2+、Cl ﹣等离子,请画出其中Mg 2+的结构示意图 。