已知A~E分别是铁、氢氧化钙、盐酸、碳酸钠、氯化铜中的一种,A与B反应能生成气体,E的溶液呈蓝色。它们相互之间的关系如图所示,“—”表示两种物质之间可以相互反应。请回答下列问题:
(1)E物质的化学式为 ;
(2)B与D反应的实验现象是 ;
(3)B和C反应的实质是 ;
(4)写出A与C反应的化学方程式 ,其基本反应类型是 。

重庆多地曾出现过盐井,从天然盐井中获取粗盐(含泥沙、CaCl2、MgCl2、Na2SO4等杂质)。为了除去以上杂质得到精盐,小明设计如下实验:
【提示】杂质含量较少,不考虑微溶物形成沉淀。
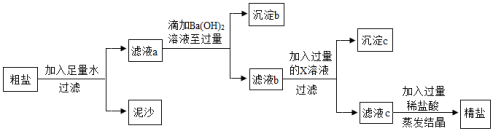
(1)过滤操作中用到的玻璃仪器有烧杯、玻璃棒和 。
(2)沉淀b所含物质为Mg(OH)2和 。
(3)物质X是 。
(4)滤液c中加入稀盐酸后发生中和反应的化学方程式为 。
(5)为了证明滴加的Ba(OH)2溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的有 。
A.Ba(OH)2
B.K2CO3
C.Na2SO4
D.KCl
实验室以某石灰石(含少量Fe2O3)为原料制备高纯CaCO3的步骤如下。
溶解 向石灰石样品中加入适量盐酸,至反应完全。
除铁 加入氨水调节pH,然后加入适量Ca(OH)2,充分反应后过滤。
沉淀 向滤液中补充氨水,通入CO2,反应一段时间。
分离 过滤、洗涤、干燥得高纯CaCO3。
(1)溶解时,CaCO3、Fe2O3分别与盐酸反应的化学方程式为 、 。判断样品已完全反应的实验现象是 。
(2)除铁时,选用Ca(OH)2而不选用NaOH,其主要原因是Ca(OH)2价格低且来源广、 、 ;过滤所得滤渣的主要成分为 。
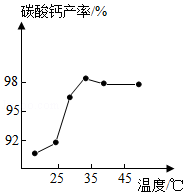
(3)沉淀时,其他条件相同,反应温度对CaCO3产率的影响如图。高于35℃时,CaCO3产率下降的主要原因是 、 (4)分离时,若向过滤所得滤液中加入 (填化学式)并加热,则可回收NH3。
(5)该实验中可以循环利用的物质有H2O和 。
(6)石灰厂煅烧石灰石生产CaO,若要得到28t CaO,则至少需要含CaCO3 90%的石灰石多少吨?(写出计算过程,保留一位小数。)