规范操作是科学实验成功的关键,下列操作正确的是( )
| A. |
|
B. |
|
| C. |
|
D. |
|
用所给实验器材(规格和数量不限),就能顺利完成相应实验的是( )
| 选项 |
相应实验 |
实验器材(省略夹持装置) |
| A |
硫酸铜晶体的制备和生长 |
烧杯、玻璃棒、蒸发皿、量筒 |
| B |
分离氯化钾和二氧化锰的混合物 |
烧杯、玻璃棒、胶头滴管、滤纸 |
| C |
用固体氯化钠配制5%的溶液 |
烧杯、玻璃棒、胶头滴管、量筒 |
| D |
用pH试纸测定溶液的酸碱性强弱 |
烧杯、玻璃棒、pH试纸、标准比色卡 |
| A. |
A |
B. |
B |
C. |
C |
D. |
D |
下列课外实验与物质的化学性质无关的是( )
A.用石墨做导电实验
B.用灼烧法区分棉纤维与羊毛纤维
C.用白糖、小苏打、柠檬酸等自制汽水
D.用紫甘蓝的酒精浸取液检验苹果汁与石灰水的酸碱性
某溶液能使紫色石蕊试液变蓝,下列说法不正确的是( )
A.该溶液呈碱性
B.可将pH试纸放入溶液中,测其pH
C.该溶液可能是碱溶液
D.向该溶液中滴加盐酸,溶液的pH变小
下列实验操作正确的是( )
A.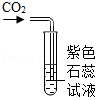 检验CO2B.
检验CO2B.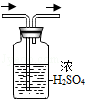 干燥H2
干燥H2
C.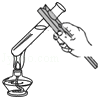 加热试管里的液体D.
加热试管里的液体D.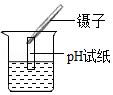 检测待测溶液的pH
检测待测溶液的pH
下列实验操作符合规范要求,能达到目的是( )
A.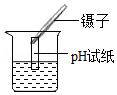 测定溶液的pH
测定溶液的pH
B. 证明MnO2的催化作用
证明MnO2的催化作用
C. 证明CO2已集满
证明CO2已集满
D. 测定空气中O2的含量
测定空气中O2的含量
甲、乙两种物质的溶解度曲线如图所示,下列叙述错误的是【 】
| A.t1℃时,甲的溶解度小于乙的溶解度 |
| B.t1℃时,加入甲物质,可使不饱和的甲溶液变成饱和 |
| C.t2℃时,甲或乙两种物质饱和溶液中溶质与溶剂的比是W:100 |
| D.将甲、乙饱和溶液的温度从t2℃降到t1℃时,乙先析出晶体 |
下列说法正确的是( )
| A.用50g溶质质量分数为10%的NaCl溶液配制溶质质量分数为5%的NaCl溶液需要加水20g |
| B.气体的溶解度与温度、压强和水的用量有关 |
| C.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 |
| D.汽油作溶剂可以去除衣物上的油污 |
下列叙述中,正确的是( )
| A.复分解反应的实质是参加反应的物质间的离子交换 |
| B.将pH试纸放入待测液中,测溶液的pH |
| C.洗洁精去除餐具上的油污是溶解的过程 |
| D.利用木炭燃烧消耗掉密闭容器中的氧气以间接测定空气中氧气的含量 |
下列说法正确的是( )
| A.在相同温度下同一物质的饱和溶液与不饱和溶液所含溶质的质量一定不相等 |
| B.某KNO3溶液在室温下蒸发5g水析出ag晶体,再蒸发5g水又析出bg晶体,则a与b一定相等 |
| C.一定质量的NaOH溶液含溶质a克,再加入a克NaOH固体,溶解后所得溶液中溶质的质量分数为原溶液的2倍 |
| D.将a克NaOH溶液加入a克的水,所得溶液的溶质质量分数是原溶液的一半 |
下列有关溶液的说法符合实际的是
| A.将澄清的饱和石灰水加热,有白色浑浊出现 |
| B.二氧化碳通入滴有紫色石蕊试液的蒸馏水中,溶液变蓝 |
| C.溶液一定是无色透明的液体 |
| D.20℃时S(NaCl)为36g,将30g氯化钠放入50g水中充分搅拌后溶质质量分数为37.5% |
溶液与我们的生活息息相关。下列有关溶液的说法不正确的是
| A.配置5%的医用葡萄糖溶液的一般步骤是计算、称量、溶解 |
| B.氢氧化钠溶液能导电是因为溶液中含有较多自由移动的离子 |
| C.硝酸钾的饱和溶液通过降温可以变成硝酸钾的不饱和溶液 |
| D.消除路面上的积雪可以撒些盐,这样可以使雪较快地融化 |
洗涤在生活、生产中不可缺少。下列洗涤方法中利用了乳化原理的是
| A.用汽油洗去手上的油污 | B.用洗洁精洗去餐具上的油污 |
| C.用酒精洗去试管中的碘 | D.用稀盐酸洗去铁制品表面的铁锈 |
下列关于溶液的说法中正确的是( )
| A.所有的溶液都可以通过升高温度由饱和变成不饱和溶液 |
| B.浓溶液一定是饱和溶液 |
| C.洗洁精清洗餐具上的油污是乳化现象 |
| D.20℃时,NaCl的溶解度是36克,此时饱和溶液中溶质的质量分数是36% |
下列有关溶液的说法中正确的是
| A.溶液中各部分的组成不同 |
| B.餐具上的油污可利用洗涤剂的乳化功能将其洗去 |
| C.把氢氧化钠固体放入盛有少量水的试管里,溶液温度没有明显变化 |
| D.将氯化钠、蔗糖分别溶于水后,溶质均以分子形式存在 |