我市某化工厂排放的尾气中除含CO2外,还可能含有CO等气体。为确认CO气体是否存在,实验小组利用下列装置进行了检验,请回答下列问题:
(1)在实验时,上述装置的连接顺序是:A→B→C→B。其中A装置的作用是 ,第一次B装置的作用为 。
(2)若CO气体存在,则装置C中实验现象为 ,反应的化学方程式为 。
(3)从环境保护的角度考虑,你认为该实验的设计应如何改进?请写出一种改进方法: 。
工业上将赤铁矿炼成铁是一个复杂的过程,炼铁高炉中发生的主要反应有( )
①C+O2 CO2②Fe2O3+3H2
CO2②Fe2O3+3H2 2Fe+3H2O
2Fe+3H2O
③Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
④2Fe2O3+3C 4Fe+3CO2↑
4Fe+3CO2↑
⑤CO2+C 2CO
2CO
| A.②③⑤ | B.①③⑤ | C.①④⑤ | D.②③ |
下列与金属有关的说法正确的是( )
| A.生铁和钢都是铁的合金 |
| B.废旧电池可以随意丢弃,不会对环境造成污染 |
| C.银的导电性比铜强,所以一般用银作电线 |
| D.铁矿石在地壳中含量最丰富,可以随意开采 |
日常生活中的一些铁制品经常会被锈蚀。下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌
②在铁制品表面涂油脂
③保留铁件表面的铁锈作保护层
④在铁器表面刷油漆
⑤自行车脏了用清水冲洗
⑥用废酸液冲洗铁制污水管道
⑦切完咸菜后,尽快将菜刀洗净擦干
| A.②⑤ | B.③⑤⑥ | C.①③⑦ | D.②⑥⑦ |
早在春秋战国时期,我国就开始生产和使用铁器。公元1世纪时,铁在我国已经被广泛使用。工业炼铁的主要设备——高炉。
请回答下列问题:
(1)铁在地壳中的含量在所有金属元素中居第________位。
(2)试写出赤铁矿(Fe2O3)与CO反应的化学方程式_________________________
_____________________________________。
(3)铁矿石在高炉中冶炼后,得到含较多碳、硫、磷、硅等的生铁。生铁的含碳量范围为_________________。
(4)生铁经过进一步冶炼可得到钢,全世界每年被腐蚀损失的钢铁约占全年总产量的十分之一。请列举一种生产、生活中防止钢铁生锈的方法:__________。
竖炉冶铁工艺流程如图所示。 
回答下列问题:
(1)该工艺流程中,甲烷的作用是_______________________,冶炼出的铁水属于__________________(填“纯净物”或“混合物”)。
(2)用化学方程式表示还原反应室内炼铁的原理_________________。(写一个)
(3)该工艺流程中,可循环利用的物质是_____________。
如图所示,在盛水的试管中放一根洁净的铁钉,用带U形管的胶塞塞紧,U形管内水面处在同一高度。数天后观察到U形管内的水面( )
| A.a比b高 |
| B.b比a高 |
| C.一样高 |
| D.U形管中的水从b管全部溢出 |
钢铁是人类生活和生产中非常重要的材料,但全世界每年都有约四分之一的钢铁因生锈损失。某化学课外小组对钢铁制品锈蚀的条件进行了如下探究,设计了如图所示的实验,据此回答下列有关问题:
(1)一周后观察到编号为_________的试管中的铁钉锈蚀严重。
(2)常温下,铁锈蚀是铁跟______和_______(用化学式表示)等物质相互作用的结果。
(3)如何防止家庭中常用的铁制品生锈?简单易行的方法是 (列举一种方法即可)。
某同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图。经过一周观察:试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。
(1)通过探究发现:铁生锈是铁与 共同存在时发生化学反应的过程。
(2)A中加入的蒸馏水要事先煮沸,其目的是 ;
(3)通过探究,请你写出防止铁制品生锈的一种措施 。
炼铁高炉中发生了下列反应:
①高温下一氧化碳将铁矿石还原为铁
②高温煅烧石灰石
③灼热的焦炭和二氧化碳反应
④焦炭充分燃烧
其中属于化合反应的是( )
| A.①和④ | B.②和③ | C.③和④ | D.只有④ |
用赤铁矿(主要成分Fe2O3)为原料,炼铁的主要反应的化学方程式是____________________________________.在这一反应中,铁元素的化合价由____________价变为____________价。
试选用“>”或“<”或“=”填空。
(1)空气中气体成分的体积分数:氧气 稀有气体;
(2)通常状况下的液体体积:100mL酒精与100mL水混合 200mL。
(3)室温下,1g硝酸钾饱和溶液中加入1g硝酸钾固体能得到溶液的质量 2g
(4)相同的两段细铁丝生锈的速率:用蒸馏水浸过的铁丝 用食盐水浸过的铁丝
(5)1g硫粉在1g氧气中完全燃烧后生成二氧化硫的质量 2g
(6)熔点:武德合金 其组成金属
下列说法正确的是
| A.天然水经过沉降、过滤、吸附、消毒,得到的是纯水 |
| B.空气中各种气体各自具有特定的组成,性质各不相同,用途也差异明显 |
| C.工业炼铁中焦炭的作用是提供热量并产生CO2 |
| D.工业生产过程中形成的废金属对环境无污染,可以随意丢弃 |
“对比实验”是化学学习中行之有效的思维方法。某化学学习小组的同学在学完相关的化学知识后,走进实验室做了如下实验,请你参与并回答下列问题。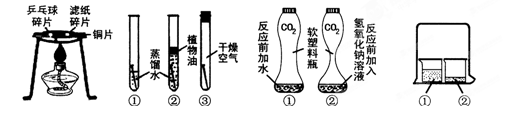
| A.燃烧的条件 | B.铁钉生锈的条件 | C.证明CO2与NaOH反应 | D.分子运动的现象 |
(1)通过实验A,可以说明燃烧的条件之一是 ,实验中使用铜片,是利用了铜的 性(填一条物理性质)。
(2)对于实验B,一段时间后观察到试管①中的铁钉明显锈蚀,由此得出:铁生锈的主要条件是铁与水和 直接接触。若用稀硫酸来除去铁制品表面的铁锈, (填“能”或“不能”)长时间浸在稀硫酸溶液中,理由是 (用化学方程式表示)。
(3)实验C是利用体积相同并充满CO2的软塑料瓶、等量的水(瓶①)和NaOH溶液(瓶②)进行实验,根据塑料瓶变瘪的程度证明CO2与NaOH溶液中的溶质确实发生了反应,这一反应的化学方程式为 。
(4)实验D的烧杯②中呈现的现象能说明分子是不断运动的。当烧杯①中液体是浓氨水时烧杯②中的酚酞溶液由无色变为 色;当烧杯①中液体换成浓盐酸,且烧杯②中液体换成滴有酚酞的NaOH溶液时,一段时间后,溶液颜色的变化是 。其中盐酸与NaOH反应的化学方程式 。
结合下列有关铁的实验,回答有关问题:
(1)铁丝在氧气中燃烧的实验:
点燃系在螺旋状细铁丝底端的火柴,待火柴将要燃尽时,插入盛有氧气的集气瓶中,观察现象.这根火柴的作用是 ;为了防止集气瓶底炸裂,应采取的方法是 。
(2)如图是探究铁钉锈蚀条件的实验:
①A中植物油的作用是 ;
②一段时间后,B中铁钉没有锈蚀,而C中铁钉锈蚀,通过B、C对比说明铁钉锈蚀的条件之一是 。