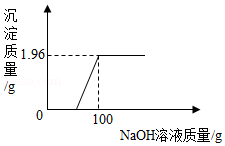
某化工厂排放的废水中含有H2SO4和CuSO4两种污染物。为测定废水中两种污染物的含量,给该化工厂提供污水处理的参考,某化学小组进行了以下实验:取该废水100g,向其中加入溶质质量分数为10%的NaOH溶液,测得生成沉淀的质量与加入NaOH溶液的质量关系如图所示,回答下列问题(写出计算过程):
(1)100g废水中含CuSO4的质量为多少?
(2)废水中H2SO4的质量分数为多少?
生铁和钢都是由铁和碳组成的合金,生铁中碳的含量为2%~4.3%,钢中碳的含量为 0.03%~2%,为测定某种铁合金中碳的含量,小王同学取一定质量的合金样品盛放在烧杯中,并向其中逐滴加入稀盐酸至恰好完全反应,实验数据如下表所示:
烧杯质量 |
样品的质量 |
稀盐酸的质量 |
烧杯+剩余物的总质量 |
50g |
5.8g |
94.6g |
150.2g |
注:碳既不溶于水也不与稀盐酸发生反应。
请根据相关信息完成下列计算:
(1)恰好完全反应时,生成氢气的质量为 g;
(2)样品中碳的质量分数 (计算结果保留到0.1%);
(3)反应后得到的溶液中溶质的质量分数(计算结果保留到0.1%)。
某实验小组同学做中和反应实验时,向80g质量分数为10%的氢氧化钠溶液中逐滴加入稀硫酸,当恰好完全反应时,共用去稀硫酸62g。请你计算:
(1)氢氧化钠溶液中溶质的质量为 g。
(2)反应后所得溶液中溶质的质量分数?
向54.5g某物质质量分数的盐酸溶液中加入4g氢氧化钠固体恰好完全反应,求所得溶液中溶质的质量分数。
我国化学家侯德榜创立了侯氏制碱法,为世界制碱工业作出了突出贡献。在实际生产的产品碳酸钠中会混有少量的氯化钠,现有该样品混合物20.4g,将其放入一洁净的烧杯中,向其中逐滴滴入7.3%的稀盐酸,放出气体质量与滴加稀盐酸质量的关系如图所示。请回答下列问题:
(1)当滴加稀盐酸至图中B点时,烧杯中溶液的pH 7(填"<"">"或"=");
(2)该样品混合物中碳酸钠的质量 g;
(3)当滴加稀盐酸至图中A点时,烧杯中所得溶液为不饱和溶液,请计算此时溶液中的溶质质量分数。(写出计算过程,计算结果保留至0.1%)。

向CaCl2和HCl的混合溶液中逐滴加入Na2CO3溶液,生成沉淀的质量变化与加入Na2CO3溶液质量关系如图所示,请回答问题:
(1)生成沉淀质量为 g。
(2)求所用Na2CO3溶液的溶质质量分数(计算结果保留一位小数)

取一定量氯化镁溶液于烧杯中,将100g的氢氧化钠溶液平均分成五次加入烧杯中。在化学反应过程中对烧杯中的溶液和沉淀进行了多次过滤并称量。加入的氢氧化钠溶液和生成沉淀的质量关系记录如下表。
| 实验次数 |
第1次 |
第2次 |
第3次 |
第4次 |
第5次 |
| 加入的氢氧化钠溶液质量/g |
20 |
20 |
20 |
20 |
20 |
| 沉淀总质量/g |
2.9 |
5.8 |
8.7 |
11.6 |
11.6 |
分析上表中的数据,完成下列问题:
(1)第 次加完氢氧化钠溶液时,氯化镁和氢氧化钠恰好完全反应,此时生成沉淀质量为 g。
(2)恰好完全反应时,称量所得氯化钠溶液质量为168.4g,求原氯化镁溶液中溶质的质量分数(请写出计算过程)。
为了测定一瓶标签被腐蚀的稀硫酸中溶质的质量分数,桢桢同学用小烧杯取了16g10%的NaOH溶液,并向其中逐滴加入该稀硫酸,反应过程中溶液的pH与滴入稀硫酸的质量关系如图所示,计算:
(1)该稀硫酸的溶质的质量分数。
(2)当滴入稀硫酸质量为4g时烧杯内溶液中钠元素的质量(写出简单的计算过程)

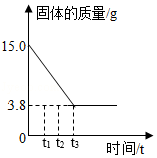
取15g某铁样品(杂质不溶于水也不与酸反应)放入烧杯中,逐渐加入一定质量的稀盐酸至不再产生气泡,烧杯中固体的质量随反应时间的关系如图所示。过滤后向所得滤液中加入143.2g水,测得溶液的溶质质量分数为10%,计算:
(1)该样品中铁的质量。
(2)所用稀盐酸的溶质质量分数。
氢化钙(CaH2)是种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是 (填写化学式)。
为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
【提出猜想】猜想一:NaOH:猜想二:NaOH和Na2CO3;
猜想三: ; 猜想四:NaOH、Na2CO3、Ca(OH)2
经过分析,大家一致认为上述猜想 不需要验证,肯定是错误的,原因是 (用化学方程式表示)。
【实验探究】
方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到有白色沉淀产生。
【讨论交流】根据实验现象,得出猜想 是正确的。请解释方案一中无明显现象的原因是 。
【拓展探究】上述小组同学将5g氢化钙样品(所含杂质不参与反应也不溶于水)加入到50g碳酸钠溶液中,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
(1)样品中CaH2的质量分数为 。
(2)原碳酸钠溶液中溶质的质量为 。
(3)反应后溶液中溶质的质量分数为 。(计算结果保留一位小数)
今年“五•一”假期,小丽随爸爸到乡下省亲,期间看到许多漂亮的大理石。于是她带了一些回来,想去学校实验室测定这些大理石中CaCO3的含量。她称取了20克大理石样品置于烧杯中,然后将250g稀盐酸分成五等份,依次加入烧杯充分反应,记录有关实验数据如下表所示(大理石中其他成分均不溶于水,也不参与化学反应)。
加入次数 |
一 |
二 |
三 |
四 |
五 |
加入稀盐酸的质量/g |
50 |
50 |
50 |
50 |
50 |
烧杯中剩余固体的质量/g |
15 |
10 |
5 |
5 |
m |
试求:(1)m的值应为 ;
(2)实验中大理石样品所含CaCO3的质量分数?
(3)实验中所用稀盐酸的溶质质量分数?
钙是人体中的常量元素,缺钙时可通过食用保健药剂来增加摄入量。某品牌补钙药剂主要含酸酸钙,为了测定该品牌补钙药剂中CaCO 3的质量分数,取该补钙剂制成的粉末20g,逐滴滴入稀盐酸(补钙剂中其他成分不与盐酸反应),得到数据如图所示,请根据有关信息回答问题:
(1)该补钙剂刚好完全反应时产生气体的质量为 。
(2)该品牌补钙药剂中CaCO 3的质量分数是 。
(3)求该盐酸中溶质的质量分数。(写出计算过程)

取NaOH和NaCl的混合物3.63克放入烧杯中,加水溶解配制成70克溶液。向该溶液滴加溶质质量分数为7.3%的稀盐酸,测得溶液pH与滴入稀盐酸的质量关系如图所示。
(1)当滴入稀盐酸的质量为11.2克时,溶液的pH 7(填“>”、“<”或“=”);此时溶液中的溶质是 (填化学式)。
(2)当pH=7时,计算该溶液中溶质的质量分数。(写出计算过程)

小明同学在完成实验室制取CO2后,对回收的盐酸和CaCl2混合溶液(不考虑其它杂质)进行以下实验:取200g该溶液于烧杯中,向其中滴加溶质质量分数为10.6%的Na2CO3溶液,滴入Na2CO3溶液与生成沉淀的质量关系如图所示。
(1)生成沉淀的质量为 g?
(2)回收液中HCl的质量分数是多少?
(3)当Na2CO3溶液与CaCl2溶液恰好完全反应时,溶液中溶质的质量是多少?
