甲、乙两种物质的溶解度曲线如图所示。叙述正确的是
| A.依据溶解度曲线可判断,甲的溶解度比乙的大 |
| B.将甲、乙的饱和溶液从t2℃降到t1℃,析出甲的质量大 |
| C.将t2℃时甲的饱和溶液变为不饱和溶液,可采取降温方法 |
| D.t1℃时,甲和乙的饱和溶液各100 g,其溶质的质量一定相等 |
为了测定在一定温度时某固体物质的溶解度,待测液必须是该温度下该物质的( )
| A.浓溶液 | B.稀溶液 | C.不饱和溶液 | D.饱和溶液 |
以下说法正确的是( )
| A.溶液一定是均一、无色、稳定的 | B.均一、稳定的液体一定是溶液 |
| C.溶液的溶质一定是固体 | D.溶液一定是混合物 |
如图是A、B、C三种物质的溶解度曲线,下列分析不正确的是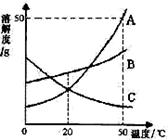
A.50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶剂的质 量比为1:2
C.将C的饱和溶液变为不饱和溶液,采用降温的方法
D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A=C
实验室中的操作类似“海水晒盐”原理的是
| A.溶解 | B.蒸发 | C.过滤 | D.搅拌 |
如图是X、Y、Z三种固体的溶解度曲线,下列有关说法中错误的是( )
| A.Z的溶解度随温度的升高而降低 |
| B.t1℃时,Z的溶解度大于X的溶解度 |
| C.t2℃时,X和Y两者的饱和溶液中溶质 |
| D.t3℃时,X的饱和溶液中溶质的质量大于溶剂的质量 |
下列有关化学知识的说法正确的是( )
| A.铁丝浸没在水中比暴露在潮湿的空气中更容易生锈 |
| B.凡是含有碳元素的化合物都是有机物 |
| C.大多数固体物质的溶解度随温度的升高而增大 |
| D.可燃物只要达到着火点就能燃烧 |
如图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是( )
| A.30 ℃时,氯化铵、硫酸钠的溶解度相同 |
| B.氯化铵的溶解度随温度的升高而增大 |
| C.将50 ℃时硫酸钠的饱和溶液降低温度,始终有晶体析出 |
| D.将60 ℃时硫酸钠的饱和溶液降温至40 ℃,溶质的质量分数不变 |
一定温度下,向图1烧杯中加入一定量的水,现象如图2,则所得溶液与原溶液相比,一定正确的是
| A.所得溶液是饱和溶液 | B.所得溶液颜色变浅 |
| C.溶质的质量增加 | D.溶质溶解度变大 |
物质M在不同温度下的溶解度数据如下表所示,以下说法正确的是( )
| 温度(℃) |
0 |
20 |
40 |
60 |
80 |
| 溶解度(g) |
13.6 |
16.3 |
20.0 |
25.0 |
39.2 |
A.0℃时,15.6gM溶于120g水中形成饱和溶液
B.20℃时,M形成饱和溶液的溶质质量分数是16.3%
C.80℃时,M的饱和溶液139.2g降温至40℃,析出晶体的质量大于20.0g
D.若要配制300.0g20.0%的M的饱和溶液,对应温度必须是60℃
能比较出室温下白糖和食盐溶解性大小的一组实验是
A.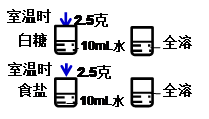 |
B. |
C.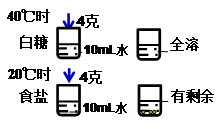 |
D. |
右图为甲、乙两种物质(均不含结晶水)的溶解度曲线,下列说法不正确的是
| A.t2℃时甲物质的溶解度大于乙物质的溶解度 |
| B.甲中含有少量的乙,可以用冷却热饱和溶液的方法提纯甲 |
| C.t1℃时,甲、乙的饱和溶液中溶质的质量分数都是30% |
| D.t2℃时,将等质量的甲、乙的饱和溶液分别降温至t1℃,所得甲溶液质量比乙溶液质量小 |
【改编】下列生活中的现象,与气体的溶解性无关的是
| A.打开雪碧瓶盖,有大量气泡溢出 ,喝下去后容易打嗝 |
| B.雪糕拿出冰箱后,包装纸上出现小水珠 |
| C.夏天下雨前气压过低时,鱼会浮起来 |
| D.潜水员进行长时间深度潜水后,需在高压氧仓过渡才能上岸 |
一定温度下,饱和食盐水露置在空气中一段时间后,有少量晶体析出,是因为
| A.氯化钠溶解度变小 | B.溶质的质量分数变小 |
| C.溶剂质量减小 | D.溶液变成不饱和溶液 |
甲、乙、丙三种不含结晶水的固体物质的溶解度曲线如图
所示,下列说法中正确的是
| A.20℃时,溶解度:甲>乙>丙 |
| B.50℃时,在100g水中放入33.3g乙,充分搅拌后所得溶液中溶质的质量分数为33.3% |
| C.若要从甲溶液(含有少量乙)中提取甲,最好采用蒸发结晶的方法 |
| D.50℃时甲、乙、丙的饱和溶液中溶质的质量分数:甲>乙>丙 |