下图为氯化铵和硫酸钠的溶解度曲线。下列说法中不正确的是
| A.30℃时,氯化铵、硫酸钠的溶解度相同 |
| B.氯化铵的溶解度随温度的升高而增大 |
| C.将50℃时硫酸钠的饱和溶液降低温度,始终有晶体析 |
| D.将60℃时硫酸钠的饱和溶液降温至40℃,溶质的质量分数不变 |
依据下图,下列说法不正确的是( )

| A. | 将硫酸钠或氯化铵的不饱和溶液转变为饱和溶液,均可采取添加溶质或蒸发溶剂的方法。 |
| B. | 升高温度,氯化铵和硫酸钠的溶解度都增大 |
| C. | 时,氯化铵饱和溶液与硫酸钠饱和溶液的溶质质量分数相等。 |
| D. | 时,将氯化铵和硫酸钠两种饱和溶液分别冷却到 时,硫酸钠溶液中无晶体析出。 |
(10福建省晋江12.)溶解度曲线为我们定量描述物质的溶解性强弱提供了便利。请你根据下图的溶解度曲线判断下列说法,其中正确的是
| A.20℃时,甲物质的溶解度大于乙物质的溶解度 |
| B.40℃时,两种物质的溶解度相等 |
| C.60℃时,将80g甲物质放入100g水中,所得溶液的质量为180g |
| D.60℃时,将等质量的甲、乙两种物质的饱和溶液降温到20℃,析出晶体较多的是乙 |
图为A、B两种物质的溶解度曲线。
(1)曲线上Q点表示 ;
(2)在20℃时两种物质的饱和溶液中溶质的质量分数为A B(选填“﹥”、“﹦”、“﹤” )各为 ;(精确到0.1%)
(3)30℃时,将10gA物质加入到盛有100g水的烧杯中,充分搅拌,得到不饱和溶液,若再加入A物质 g或降温到 ℃,都能恰好形成饱和溶液。
下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
| 温度(℃) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
90 |
100 |
| KNO3 |
13.3 |
20.9 |
32 |
45.8 |
64 |
85.5 |
110 |
138 |
169 |
202 |
246 |
| NaCl |
35.7 |
35.8 |
36 |
36.3 |
36.6 |
37 |
37.3 |
37.8 |
38.4 |
39 |
39.8 |
①以上两种物质溶解度的变化受温度影响较小的是________。
②30℃时,KNO3的溶解度是________g/100g水。
③KNO3溶液中含有少量NaCl时,可通过________的方法提纯。
④对③析出的晶体和剩余溶液描述正确的是________(填写编号)。
Ⅰ、剩余溶液一定是KNO3饱和溶液 Ⅱ、剩余溶液一定是NaCl不饱和溶液
Ⅲ、上述方法可以将两者完全分离 Ⅳ、析出的晶体中只含有KNO3
⑤在一定温度下,将含69gKNO3、18gNaCl的混合物完全溶解在50g水中。改变温度使KNO3析出,NaCl不析出,则温度T(℃)的范围是________(硝酸钾和氯化钠溶解度互不影响)。
下图是A、B、C三种物质的溶解度曲线,下列说法不正确的是
A.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过冷却热饱和溶液的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和
D.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是( )

| A. |
t 1℃时a、c两物质溶液中溶质的质量分数相等 |
| B. |
t 2℃时,物质a的100g饱和溶液中含有25g物质a |
| C. |
t 2℃时,分别将a、b、c的饱和溶液降温至t 1℃,溶质质量分数关系是b>a=c |
| D. |
t 2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g |
将20.0g稀盐酸逐滴加入到10.0g溶质质量分数为4.0%的氢氧化钠溶液中,边滴加边搅拌,随着稀盐酸的滴加,溶液的pH变化情况如图所示,溶液的温度变化如表所示(不考虑反应过程中热量散失)
| 反应时间(s) |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 溶液温度(℃) |
20.5 |
20.6 |
20.7 |
20.8 |
20.9 |
20.8 |
20.7 |
(1)当稀盐酸与氢氧化钠溶液恰好完全反应时,溶液的温度是 ℃
(2)计算稀盐酸中溶质的质量分数(精确到0.1%)

如图表示M、N两种物质的饱和溶液的溶质质量分数随温度变化的曲线。现分别向50克M、80克N固体中各加入150克水,并加热至完全溶解,同时各蒸发掉50克水,冷却至t℃,下列分析正确的是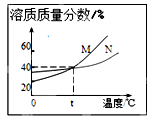
| A.M、N两溶液的溶质质量分数相等 |
| B.只有N析出晶体 |
| C.M、N均有晶体析出 |
| D.M、N两溶液都是饱和溶液。 |
如图是
、
、
三种固体物质的溶解度曲线,下列分析不正确的是
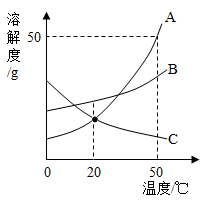
| A. |
50℃时,三种物质的溶解度由大到小的顺序是 |
| B. |
50℃时,把50 放入50 水中形成75 的饱和溶液 |
| C. |
20℃时, 和 两种物质的溶解度相等 |
| D. |
分别将三种物质的饱和溶液从50℃降至20℃时,所得溶液溶质质量分数大小关系是 |
下列关于溶液的叙述正确的是
| A.汽油洗衣服上的油污是利用了乳化作用 |
| B.硝酸铵固体溶于水时仅发生扩散吸热的过程 |
| C.某物质的不饱和溶液变为饱和溶液后溶质质量分数可能不变 |
| D.“波尔多液”是无色、透明、均一稳定的混合物 |
如图是a、b、c三种固体物质的溶解度曲线

(1)在t1℃时,a、b、c三种物质中,溶解度最大的是 ;
(2)t1℃时,将30g a物质放入100g水中,充分搅拌,所形成的溶液是 溶液(填“饱和”或“不饱和”);溶液中溶质的质量分数是 (精确到0.1%);此时若将温度由t1℃升至t2℃,还应再加入a物质 g,才能变成饱和溶液。
(3)从a、c的饱和溶液中提取a,应采用方法是 (填“冷却结晶”或“蒸发溶剂”)。
除杂(括号内为杂质)方法错误的是
| A.N2(O2)通过灼热的铜网 | B.KNO3(NaCl)溶解、蒸发浓缩后降温结晶 |
| C.CaO(CaCO3)加水后过滤 | D.CO2 (CO) 通过灼热的氧化铜 |
在20℃时,向质量均为50g的5份水中分别加入一定质量的氯化钾固体,然后搅拌至完全溶解得到溶液(如有不溶解的氯化钾,则过滤除去).加入氯化钾的质量与所得溶液的质量见下表.
| 实验编号 |
1 |
2 |
3 |
4 |
5 |
| 加入氯化钾的质量/g |
5 |
10 |
15 |
20 |
25 |
| 溶液的质量/g |
55 |
60 |
65 |
67 |
67 |
(1)在20℃时,实验3所得的溶液中溶质与溶剂质量之比为_________;
(2)在20℃时,实验5所得的溶液中溶质的质量为_________g;
(3)在20℃时,实验1所得的溶液为不饱和溶液,可以通过________________的方法使它变为饱和溶液;
(4)在20℃时,所得溶液的溶质质量分数:实验3____ 实验4____ 实验5(用“﹤”或“﹥”或“=”填空)
下图是a、b两种固体物质的溶解度曲线。下列说法正确的是
| A.b物质的溶解度大于a物质的溶解度 |
| B.t1℃时,a、b两种物质的溶解度相等 |
| C.t2℃时,100克b物质的溶液中含有80克b物质 |
| D.将t2℃时接近饱和的a溶液变为饱和溶液,可采用升高温度的方法 |