将50℃的硝酸钠饱和溶液降温到20℃,有晶体析出(晶体中不含水)。下列有关量中没有发生改变的是()
| A. | 硝酸钠的溶解度 | B. | 溶液中溶质的质量 |
| C. | 溶液中溶剂的质量 | D. | 溶液中溶质的质量分数 |
将60℃饱和的硝酸钾溶液降温至20℃,没有发生变化的是
| A.溶液的质量 | B.溶液里溶质的质量 |
| C.溶液里溶剂的质量 | D.溶液里溶质的质量分数 |
t℃时,某物质的溶解度为10 g,则t℃时该物质的饱和溶液中,溶质、溶剂、饱和溶液间的质量比为
| A.1∶9∶10 | B.1∶10∶11 |
| C.9∶1∶10 | D.10∶1∶11 |
以下是KCl的部分溶解度数据,下列说法中正确的是
| 温度(℃) |
0 |
20 |
40 |
60 |
| 溶解度(g/100g水) |
27.6 |
34.0 |
40.0 |
45.5 |
A.KCl饱和溶液中不能再溶解其他物质
B.20℃时,100 g KCl饱和溶液中含KCl 34.0 g
C.20℃的KCl溶液的浓度一定小于 40℃的KCl饱和溶液的浓度
D.60℃时,将一定质量分数KCl溶液降温到40℃,一定有晶体析出
如图是甲、乙、丙三种物质的溶解度曲线,将甲、乙、丙三种物质tl℃时的饱和溶液升温至t2℃,所得溶液的溶质质量分数关系正确的是
| A.甲>乙>丙 | B.甲=乙=丙 | C.甲=乙>丙 | D.丙>甲=乙 |
如图为a、b、c三种物质(均不含结晶水)的溶解度曲线。
①t1℃时c物质的溶解度是 (38) ;
②P点的含义是 (39) ;
③t2℃时,向60g的水中加入35g a物质,充分搅拌,所得溶液的质量是 (40) g;
④t1℃时,相同质量的a、b、c三种物质的饱和溶液中所含溶剂的质量最少的是 (41) (填“a”或“b”或“c”);
⑤欲将b物质的不饱和溶液变为饱和溶液,下列说法正确的是 (42) (填序号)。
Ⅰ.溶液中溶质的质量一定增加
Ⅱ.溶质b的质量分数可能增大
Ⅲ.溶液的质量可能不变
Ⅳ.可倾倒出一些水
下图是是甲、乙两种固体物质的溶解度曲线,请你回答下列问题:
(1) ℃时,甲、乙两种物质的溶解度相等;
(2)若固体甲中含有少量乙时,可用 方法提纯甲(填“蒸发结晶”或“冷却结晶”);
(3)溶解度受温度影响比较大的物质是 ;
(4)t2℃时,用等质量的甲、乙两种物质配制甲、乙的饱和溶液需要水的质量:甲 乙(填“>”“<”或“=”)
硝酸钾的溶解度如下表所示,有关叙述正确的是
| 温度(℃) |
20 |
30 |
40 |
50 |
60 |
| 溶解度(g/100g水) |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
A.20℃时,可配成50g35%的硝酸钾饱和溶液
B.30℃和50℃时,等质量的硝酸钾饱和溶液,所含水的体积,前者大于后者
C.40℃时,50g硝酸钾饱和溶液降温至20℃,析出固体的质量为32.3g
D.60℃时,50g硝酸钾饱和溶液中,溶质与溶剂的质量比为11:21
下图是常见固体物质的溶解度曲线,根据图示回答:
(1)A、B、C三种物质可能是气体的是 。
(2)将t1℃140g A的饱和溶液升温至t2℃时,可用图上的 点表示,此时溶液是 (填“饱和”或“不饱和”)状态,然后再加入A物质40g,可用曲线上的 点表示。t2℃时A、B、C三种物质饱和溶液的质量分数由大到小的顺序是 。
(3)若将d点对应的温度下A、B、C三种物质的饱和溶液降温至t1℃,没有晶体析出的是 物质。
如图是甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线,回答下列问题:
(1)t1℃时,甲物质的溶解度 (填“>”“<”或“=”)丙物质的溶解度;
(2)将丙的不饱和溶液变为饱和溶液的方法是 ;
(3)t2℃时,将一定质量的甲物质加入到100g水中完全溶解,再降温到t1℃,析出甲物质15g,则t2℃时,加入甲物质的质量为 g;
(4)将t3℃时甲、乙、丙三种物质的饱和溶液降温到t1℃,所得溶液中溶质的质量分数由大到小的顺序为 。

溶液与人类的生活息息相关。
(1)下列少量物质分别放入水中,充分搅拌,能得到溶液的是 (填序号)。
A.面粉
B.硝酸钾
C.泥沙
D.花生油
(2)下表是氯化钠和氯化钾在不同温度时的溶解度。
温度/℃ |
0 |
20 |
40 |
60 |
80 |
|
溶解度 |
NaCl |
35.7 |
36.0 |
36.6 |
37.3 |
38.4 |
KCl |
27.6 |
34.0 |
40.0 |
45.5 |
51.1 |
|
①20℃时,氯化钠的溶解度为 g。
②20℃时,将20g氯化钠固体加入到50g水中,充分溶解,所得氯化钠溶液的质量为
g。
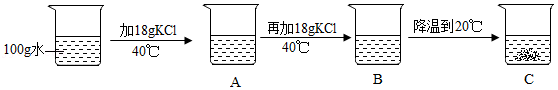
③某同学进行实验如图所示,得到相应的A、B、C三种溶液,C中析出的氯化钾固体质量为 g。
打开啤酒瓶盖时,你会发现啤酒会自动喷出,喝了啤酒后又常常会打嗝,这说明气体溶解性与外界的压强和温度有关,下列关于气体溶解度说法不正确的是
| A.压强减少,气体溶解度增大 | B.压强减小,气体溶解度减小 |
| C.温度升高,气体溶解度减小 | D.温度降低,气体溶解度增大 |
20℃时,在两只各盛有50克水的烧杯中,分别加入30克氯化钠和蔗糖固体,搅拌使其充分溶解,结果如图所示。下列说法正确的是()

| A. | 两烧杯中的溶液质量相等 | B. | 20℃时两者的溶解度相等 |
| C. | 氯化钠溶液一定是饱和溶液 | D. | 蔗糖溶液一定是饱和溶液 |
下图是甲、乙、丙三种物质(均不含结晶水)的溶解度曲线。现有t2℃时甲、乙、丙三种物质的饱和溶液(无固体存在)。下列说法正确的是
| A.三种物质溶解度大小依次为:乙>丙>甲 |
| B.将温度由t2℃降到t1℃时,析出甲的质量比乙多 |
| C.若甲中含有少量杂质乙,可采用降温结晶的方法进行提纯 |
| D.将温度由t2℃降到t1℃,所得溶液中溶质的质量分数由大到小的顺序为:乙>丙=甲 |
下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
| 温度/℃ |
0 |
20 |
40 |
60 |
80 |
100 |
|
| 溶解度/g |
Ca(OH)2 |
0.19 |
0.17 |
0.14[ |
0.12[ |
0.09 |
0.08 |
| NaOH |
31 |
91 |
111 |
129 |
313 |
336 |
|
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,下图中能表示NaOH溶解度曲线的是 (填A或B)。

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②升高温度,③降低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰。
其中措施正确的是 。
A.②④⑥ B.③④ C.①③⑤⑥ D.①②⑤⑥
(3)20℃时,191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为 。
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后得到的溶液(乙溶液),此时溶液中溶质的质量分数乙 甲(填“>”、“<”或“=”)。
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是 。
(6)20℃时,欲测定NaOH溶液的pH,若先将pH试纸用蒸馏水润湿,再进行测定,则所测溶液的pH (填“偏大”、“偏小”或“不受影响”)。