根据如图所示溶解度曲线判断,下列说法正确的是( )

A.28℃时,将40g KNO3溶于100g水得到饱和溶液
B.将43℃的Na2CO3饱和溶液升高10℃,有晶体析出
C.三种物质的饱和溶液由40℃降温至23℃,所得溶液中溶质质量:m(NaCl)=m(KNO3)>m(Na2CO3)
D.除去KNO3中混有的Na2CO3,可在40℃配成饱和溶液,再降温结晶、过滤
甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )

A.温度为T1℃时,100g甲、乙的饱和溶液,温度降到T0℃时,两溶液的质量仍然相等
B.温度为T1℃时,甲和乙各30g分别加入100g水中,均形成饱和溶液
C.温度为T2℃时,在100g水中加入50g乙,形成的是不饱和溶液
D.甲的溶解度大于乙
根据图示实验、部分记录和溶解度曲线,判断下列说法正确的是( )
A.无法判断a中溶液是否为饱和溶液
B.c中溶液溶质的质量分数为33.3%
C.b中溶液在加热过程中始终为饱和溶液
D.常用冷却热的饱和溶液的方法获得氯化钠晶体
(1)水与人类的生活密切相关。
①硬水给生活和生产带来许多麻烦,一般可用 来区分硬水和软水。
②可利用活性炭吸附水中的异味和色素,活性炭的吸附性属于 (填“物理”或“化学”)性质。
(2)下表是KNO3和Ca(OH)2在不同温度时的溶解度。回答有关问题:
温度/℃ |
10 |
20 |
30 |
40 |
50 |
60 |
|
溶解度/g |
KNO3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110.0 |
Ca(OH)2 |
0.19 |
0.17 |
0.16 |
0.14 |
0.13 |
0.11 |
|
①两种物质中,溶解度随温度升高而减小的是 。
②60℃时,按图示操作:
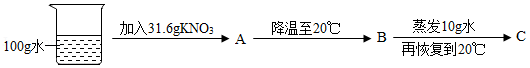
A中的溶液是 (填“饱和”或“不饱和”)溶液。
C中析出固体的质量是 g。
③如图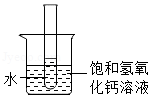 ,向烧杯中加入一定量的硝酸铵固体,此时试管中氢氧化钙溶液的溶质质量分数将 (填“变大”不变”或“变小”)。
,向烧杯中加入一定量的硝酸铵固体,此时试管中氢氧化钙溶液的溶质质量分数将 (填“变大”不变”或“变小”)。
推理是学习化学的一种重要思维方式。以下推理正确的是( )
A.氧化物中含有氧元素,则含有氧元素的物质一定是氧化物
B.铝表面的氧化铝薄膜起到保护作用,则铁的表面的铁锈也起保护作用
C.蔗糖的饱和溶液不能再溶解蔗糖,也一定不能再溶解其他物质
D.点燃氢气和氧气的混合物可能发生爆炸,则点燃可燃性气体和氧气的混合物都可能发生爆炸
如图是四种物质的溶解度曲线,下列说法中正确的是( )

| A. |
20℃时,分别配制四种物质的饱和溶液,硫酸铵需要水的质量最少 |
| B. |
40℃时,向硫酸铵饱和溶液中加入适量氯化钾固体会析出硫酸钾晶体 |
| C. |
氯化钾饱和溶液的溶质质量分数一定小于氯化铵饱和溶液的溶质质量分数 |
| D. |
用30克硫酸钾固体最多可配制150克80℃的硫酸钾饱和溶液 |
为M、N两种固体物质的溶解度曲线,据图回答:
(1)b点表示的意义是 。
(2)t2℃时,将M溶液的状态由a点转化到b点,可采用的方法是 和 。
(3)将t1℃时,M和N的饱和溶液各100g降温至t0℃,过滤,得到滤液m和滤液n。关于m和n的说法正确的是 (填序号)。
A.都是饱和溶液 B.溶液质量:m<n C.溶剂质量:m<n
D.溶质质量:m=n E.溶质的质量分数:m=n

水是宝贵的自然资源,日常生活、工农业生产和科学实验都离不开水。
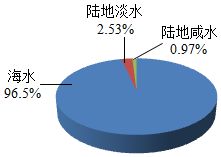
(1)图中的海水属于 (填“纯净物”或“混合物”)。
(2)如图所示,利用海水提取粗盐的过程中,析出晶体后的母液是氯化钠的 (填“饱和”或“不饱和”)溶液。
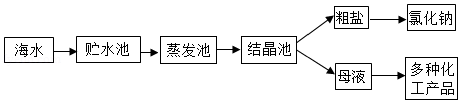
(3)河水是重要的陆地淡水资源,经处理后可用作城市生活用水,自来水厂净水的过程中不包括下列哪种净水方法 (填字母序号)。
A、沉淀 B、过滤 C、蒸馏 D、吸附
(4)生活中,人们常用 来检验水样品是硬水还是软水。
已知NH4Cl、KNO3在不同温度时的溶解度
温度/℃ |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
70 |
80 |
|
溶解度/g |
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
55.2 |
60.2 |
65.6 |
KNO3 |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
85.5 |
110 |
138 |
169 |
|
请回答下列问题:
(1)在35℃时,KNO3的溶解度 NH4Cl的溶解度。(填“>”或“=”或“<”)
(2)若KNO3固体中含有少量NH4Cl固体,可采用 获得KNO3晶体。(填“蒸发结晶”或“降温结晶”)
(3)25℃时,将15克KNO3固体溶解在50克水中,所得溶液为 。(填“饱和溶液”或“不饱和溶液”)
(4)20℃时,饱和NH4Cl溶液溶质质量分数为 。(精确到0.1%)
如图为KNO3、NaCl两种固体物质的溶解度曲线,请回答下列问题:

(1)10℃时KNO3的溶解度 (填“<“、“=“或“>”)NaCl的溶解度。
(2)80℃时140g KNO3溶于100g水中形成的溶液是 (填“饱和”或“不饱和”)溶液。
(3)如图所示进行实验,再现结晶过程:

本实验条件下,影响析出晶体质量多少的主要因素是 、 。
如图是A、B、C三种固体物质的溶解度曲线。
(1)P点表示的含义是 。
(2)t1℃时,将35gA物质加入到50g水中,形成 (填“饱和”或“不饱和”)溶液。
(3)B中混有少量的A,提纯B的方法是 。
(4)将等质量的A、B、C三种固体物质分别配成t3℃时的饱和溶液,所得溶液的质量最多的是 。
(5)将t1℃时A、B、C三种物质的饱和溶液升温到t3℃时,所得溶液的溶质质量分数由大到小的关系是 。

如图是硝酸钾的溶解度曲线,回答下列问题。
1)硝酸钾的溶解度随温度的升高而 。
(2)20℃时,100g硝酸钾饱和溶液中含硝酸钾的质量 (填“大于”、“等于”或“小于”)31.6g。
(3)图中点A所对应的是该温度下硝酸钾的 (填“饱和”或“不饱和”)溶液。

如图为a、b、c三种不含结晶水的固体物质在水中的溶解度曲请回答下列问题:
(1)t1℃时,a、b、c三种物质溶解度由大到小的顺序为 。
(2)当b中混有少量a时,提纯b的方法是 。
(3)t4℃时,将等质量的a、b、c三种饱和溶液降温到t3℃时,所得溶液中,溶剂质量由大到小的顺序为 。
(4)t4℃时,在三个装有50g水的烧杯中分别加入a、b、c三种物质各20g,能形成不饱和溶液的是 ,再降温到t2℃时,所得三种溶液的溶质质量分数大小关系为 。

T1℃时,将等质量的KNO3、KCl分别加入到各盛有100.0g水的两个烧杯中,充分搅拌后恢复到T1℃,现象如图1、2所示。下列说法正确的是( )

A.甲中加入的固体是KNO3
B.甲中溶液可能是该溶质的饱和溶液,乙中上层清液一定是该溶质的饱和溶液
C.将甲、乙中的物质混合,充分搅拌,一定有固体剩余
D.若将甲、乙的温度从T1℃升高到T2℃,两溶液中的溶质质量分数相等