化学小组的同学利用如图仪器和装置完成以下实验。

(1)制取氧气。
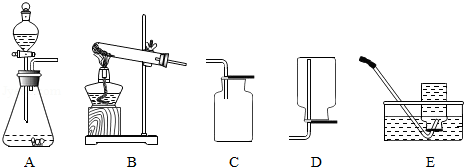
①指出图中标号仪器的名称:X 。
②高锰酸钾和过氧化氢溶液均可用于实验室制取氧气。加热高锰酸钾制取氧气,可选用的发生装置是 (填字母序号,下同),收集装置是 。
③选用B作为发生装置,用过氧化氢和二氧化锰制取氧气。该反应的化学方程式是 。实验时的主要操作步骤有:a.向分液漏斗中加入过氧化氢溶液;b.收集气体;c.检查装置的气密性;d.向锥形瓶中加入二氧化锰;e.组装仪器。以上步骤正确的操作顺序是 (填字母序号)。
(2)制取二氧化碳。用大理石与稀盐酸反应制取二氧化碳的化学方程式是 。反应后的废液中如果含有稀盐酸不能直接排放,以免污染环境。请你选择下列试剂设计一种实验方案,检验废液中是否含有稀盐酸。
可供选择的试剂;石灰石、硝酸银溶液、紫色石蕊试液、氢氧化钠溶液
| 实验操作 |
现象与结论 |
|
|
|
如图是实验室制取气体的常见装置。请回答下列问题:

(1)仪器①的名称是 。
(2)用A和F装置制取氧气,反应的化学方程式是 。向气体发生装置内装入药品前应进行的操作是 。实验过程中发现收集的气体不纯,原因可能是 (写出一点即可)。
(3)制取二氧化碳的发生装置可选用B或C.使用B装置时,长颈漏斗末端管口应伸入液面以下,原因是 。与B相比,C装置的优点是 (答一点即可)。若用G装置收集二氧化碳,检验二氧化碳收集满的方法是 。
化学是一门以实验为基础的自然科学,化学实验和科学探究离不开装置。
| 制取气体的常用装置 |
|
|
|
| 收集气体的常用装置 |
|
|
|
| 干燥气体的常用装置 |
|
|
此格空白 |
(1)制取气体时,首先要对发生装置进行气密性的检查,确保装置不漏气。检查装置C气密性的方法是:首先将导管的末端浸在水中,然后用双手紧握试管,一会儿发现导管末端 ,松开双手后,导管末端液面上升,形成一段稳定的水柱,说明装置的气密性良好。
(2)收集气体的方法主要决定于气体的性质。装置F所示的收集方法是 ,被收集气体的密度 空气的密度(填"大于"、"等于"或"小于");如果用D装置收集某种气体,发现 时,证明气体已集满。
(3)实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳气体,所选装置正确的连接顺序是 → → (填装置编号)。
(4)从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法就是利用过氧化氢在二氧化锰做催化剂的条件下分解,其主要操作步骤有:①检查装置的气密性;②组装仪器;③向漏斗中注入过氧化氢溶液;④向锥形瓶中放入二氧化锰;⑤收集气体。正确的操作顺序是 (填序号)。
a.①②③④⑤
b.①④②③⑤
c.②①④③⑤
d.②③④①⑤
(5)写出用高锰酸钾加热制取氧气的化学方程式 。
利用如图装置进行气体的制取实验,请回答下列问题:
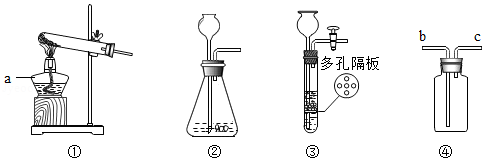
(1)写出标号a仪器的名称: .
(2)用氯酸钾制取氧气的化学方程式 ,选择④装置收集氧气,气体从 (填字母)端进入.若改用排水法收集,实验结束后先撤导气管后熄灭酒精灯,目的是防止 .
(3)实验室用大理石和 (填写药品名称)反应制取二氧化碳.与②相比,③作为发生装置的优点是 ,在装置④中盛放 可用于干燥二氧化碳气体.
如图是初中化学实验室制取气体的常用装置图,请回答下列问题: 
(1)仪器a的用途是 ;
(2)写出装置B制取氧气的化学方程式 。装置B中试管口略向下倾斜的目的是 ,若用C装置收集氧气,当 时开始收集;
(3)实验室制取二氧化碳选择的发生装置是 (填写装置下方的字母)。若用F装置收集二氧化碳气体,检验气体收集满的操作方法是 。
请结合图回答问题:
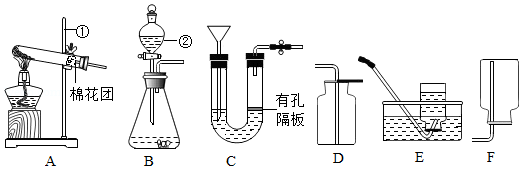
(1)仪器名称:① ,② 。
(2)用高锰酸钾制取氧气,可选用的发生装置是 (选填序号),该反应的化学方程式为 。用E装置收集氧气完毕后,应先 (选填"从水中取出导气管"或"熄灭酒精灯")。
(3)实验室制取CO 2,反应的化学方程式为 ,为方便控制反应的发生和停止,应选择的发生装置是 (选填序号),可用D装置收集CO 2的理由是 。
(4)NH 4Cl溶液与NaNO 2溶液混合共热可制取氮气,氮气和氢气在一定条件下可生成氨气。如图是实验室制氮气并模拟合成氨的装置。
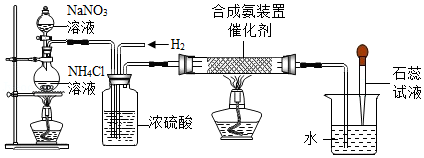
①合成氨时参加反应的氮气和氢气的质量比为 。
②实验中烧杯内导管口有气泡,还可观察到 现象。
实验利用如图所示装置进行相关实验,请回答问题

(1)写出标有序号①仪器的名称 。
(2)实验室用高锰酸钾制取并收集氧气可选择的装置组合是 。写出该反应的化学方程式 。用此方法制取氧气的实验步骤有:①在试管中加入药品并固定好装置:②把导管移出水面;③点燃酒精灯加热,当气泡连续均匀冒出时开始收集;④熄灭酒精灯;⑤检查装置的气密性。下列排序正确的是 。
A.①⑤③②④
B.⑤①③②④
C.①⑤③④②
D.⑤①③④②
(3)实验室制取二氧化碳的药品是 。图F是某同学利用塑料瓶和其他用品设计的二氧化碳的发生装置,该设计与B装置比较除了废物利用的优点外,请另写出一个优点 。
某兴趣小组围绕"实验室制取氧气"进行了一系列探究活动:
(1)药品选择:下列物质中不能作为实验室制取氧气反应物的是 (填字母).
A.水 B.过氧化氢 C.氯化钾(KMnO 4)
原因是 .
(2)装置连接,所需的一些实验装置如图1所示:
仪器a的名称是 ;选择气体收集方法时,气体的下列性质:A.颜色 B.可燃性 C.溶解性 D.密度,必须考虑的是 (填字母);要制取并收集一瓶干燥的氧气,所选装置的连接顺序为 (填装置字母序号).
(3)气体检验:如图2甲装置中带火星的木条很难复燃,乙装置中带火星的木条较易复燃,原因是 .
(4)实验探究:如图3所示,向三支试管中分别滴加浓度相同的三种溶液,观察可见:实验①中无明显现象,实验②中产生气泡,实验③中产生气泡更快,据悉你能得出的结论是 .
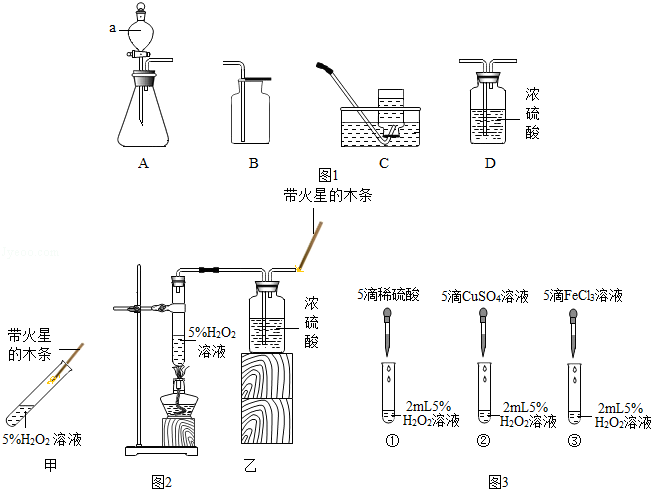
华雪同学在老师的指导下从图中选择装置在实验室进行氧气的制备实验。

(1)华雪同学首先选择装置A和E用加热高锰酸钾的方法制取氧气。
①装置A和E的导管口之间要用 连接。(填实验用品)
②不用D装置收集氧气的原因是 。
③当反应不再进行时停止加热,待试管冷却后洗涤试管,可看到溶解残留固体的洗涤用水呈现绿色(已知MnO 2不溶于水),说明 (填离子符号)在溶液中呈绿色。
(2)华雪同学然后选择装置B和C用分解过氧化氢的方法制取氧气。
①写出仪器a的名称: 。
②实验证明MnO 2、CuSO 4溶液、FeCl 3溶液等对过氧化氢的分解具有催化作用。已知FeCl 3在水中可解离处Fe 3+和Cl ﹣,请设计实验证明:FeCl 3溶液中对H 2O 2的分解真正起催化作用的是FeCl 3溶液中的Fe 3+. 。
实验室常用如图的一些装置制备气体,请回答下列问题:

(1)写出图中仪器a的名称: ;
(2)写出实验室用氯酸钾制O 2的化学方程式: ;如用装置B、C制备氧气,收集完氧气后,应先进行的操作是 ;
(3)实验室制备CO 2时,选用的发生装置是 ,收集装置是 .
某兴趣小组根据下列装置进行试验,请你参与并回答:

(1)②仪器的名称是 .
(2)若用A装置制取氧气,则①中可观察到的现象是 (任答一点);若用E装置收集气体,观察到 时才能收集.
(3)写出用B装置制取二氧化碳气体的化学方程式 .
(4)写出检验氧气是否收集满的方法 .
(5)已知氢气密度比空气小,很难溶于水,常用金属锌和稀硫酸反应制取.若实验室要制取少量氢气最好选择发生装置 (填序号,下同)和收集装置 .
根据如图所示的实验回答问题:
(1)甲实验中仪器a的名称是 ;停止加热时,要先将导管移出水面,再熄灭酒精灯,原因是 .
(2)乙实验验证了硫酸铵的物理性质: (答一条即可);化学性质: .
(3)配制50g10%的氯化钠溶液,量取水的操作如图丙所示,其他操作都正确,所配溶液中氯化钠的质量分数 (选填">"、"="或"<")10%.

进行氧气制取与性质检验的实验。
(1)以过氧化氢溶液为原料制取并收集氧气,应选用的装置是 (选填序号)。
(2)实验中,用装有一定量水的集气瓶进行排水法收集氧气,能使带火星木条复燃,那么使带火星的木条复燃的氧气体积分数的最低值是多少呢?进一步展开探究。
第一组实验:5只容积均为100毫升的集气瓶,分别装入一定体积的水,再用排水法收集氧气,恰好把5只集气瓶中的水排去,将带火星的木条依次伸入5只集气瓶中,记录实验现象。
以相同方法完成第二组实验,两组实验的数据和现象见下表,(已知空气中氧气的体积分数为21%)
|
第一组 |
第二组 |
||||||||
集气瓶编号 |
A |
B |
C |
D |
E |
A |
B |
C |
D |
E |
集气前装入集气瓶内水的体积(毫升) |
10 |
20 |
30 |
40 |
50 |
31 |
33 |
35 |
37 |
39 |
带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
很亮 |
很亮 |
复燃 |
复燃 |
复燃 |
①第一组实验D瓶,集气结束时氧气的体积分数为 %。
②经计算,第二组实验C瓶的氧气体积分数为48.65%,由此得出“使带火星的木条复燃的氧气体积分数的最低值只能是48.65%”的结论,对此结论和过程进行评价: 。
实验室制取、收集、干燥气体的常用装置如图所示。请回答下列问题:
(1)实验室制取二氧化碳所选用的收集装置是 ,反应的化学方程式是 。
(2)若用高锰酸钾制取氧气,并用排水法收集,实验操作步骤如下:①点燃酒精灯并收集气体②熄灭酒精灯③加入药品并固定仪器④检查装置的气密性⑤从水槽中撤出导管。正确的操作顺序是 (填字母)。
A.③④①②⑤
B.④③①②⑤
C.④③①⑤②
D.①②③④⑤
(3)若要除去氧气中混有的水蒸气,气体应从F装置的 端进入。