分析处理图表中的信息是学习化学的一种重要方法,如表是NH 4Cl和KNO 3在不同温度时的溶解度数据:
| 温度/℃ |
10 |
30 |
50 |
70 |
|
| 溶解度/g |
NH 4Cl |
33.3 |
41.4 |
50.4 |
55.2 |
| KNO 3 |
20.9 |
45.8 |
85.5 |
110 |
|
根据上述数据,回答下列问题:
(1)从上表可知,50℃时,NH 4Cl的溶解度为 g.
(2)NH 4Cl和KNO 3的溶解度受温度影响比较大的物质是 (填化学式).
(3)欲配制质量分数为10%的KNO 3溶液,需要的玻璃仪器有烧杯、量筒、胶头滴管和 .
(4)烧杯中A中是60℃时,含有100g水的NH 4Cl不饱和溶液,经过如图1的变化过程
(在整个过程中,不考虑水分的蒸发),则C烧杯中溶液的质量为 g 
(5)某同学欲验证NH 4Cl固体溶于水时吸收热量,设计如图2实验,通过观察到 现象得以验证.
A.a端液面高于b端液面
B.a端液面低于b端液面.
酸、碱、盐在生产生活中具有广泛的用途.
(l)制作“叶脉书签”需用到10%的氢氧化钠溶液.现配制50g质量分数为10%的氢氧化钠溶液.
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为 g.
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要 .
③下列操作正确的是 (填字母).
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为lg/cm3)配制50g质量分数为10%的氢氧化钠溶液,需20%的氢氧化钠溶液的质量为 g;配制时应选用 mL的量筒量取水(填“10”或“50”).
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种.为确定该固体粉末的成分,进行了如下实验:
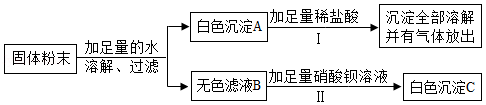
回答下列问题:
①反应I 的化学方程式为 .
②白色沉淀C是 (填化学式).
③原固体粉末中一定不含 (填化学式).
溶液在日常生活、工农业生产和科学研究中具有广泛的用途。
(1)生理盐水是医疗上常用的一种溶液,其溶质是 (填化学式)
(2) 在盛有水的烧杯中加入以下某种物质, 形成溶液的过程中温度上升。 这种物质是 (填字母)。
A.氯化钠 B.硝酸铵 C.氢氧化钠
(3)某同学在实验室用氯化钠固体和蒸馏水配制50g质量分数为6%的氯化钠溶液时,涉及以下实验步骤:
①溶解 ②称量和量取③计算④装入试剂瓶贴好标签。
配制上述溶液正确的实验步骤顺序是 (填序号)
(4)某注射用药液的配制方法如下:
①把1.0g药品溶于水配制成4.0mL溶液a;
②取0.1mL溶液a,加水稀释至1.0mL,得溶液b;
③取0.1mL溶液b,加水稀释至1.0mL,得溶液c;
④取0.4mL溶液c,加水稀释至1.0mL,得溶液d。
由于在整个配制过程中药液很稀,其密度都可近似看做1g/cm 3.则最终得到的药液(溶液d)中溶质的质量分数为 。
如图是实验室制取气体的有关装置图,据图回答下列问题:

(1)写出图中标号仪器的名称:X ,Y 。
22,应选用的发生装置为 (填装置序号,下同),收集装置为 2,则反应的化学方程式为 。
(3)小海同学在装置B中加入15%的过氧化氢溶液和二氧化锰制取氧气。
①若用F装置收集氧气,氧气应从 (填“a”或“b”)端通入。
②实验中发现不能得到平稳的氧气流。小涛同学提出可以从两个方面加以改进:
一是将制取的装置B换为上图中的装置 ;
二是将过氧化氢溶液加水稀释。如果把50g溶质质量分数为15%的过氧化氢溶液稀释成溶质质量分数为10%的溶液,需加水的质量为 克。
实验技能是学习化学和进行探究活动的基础和保证。
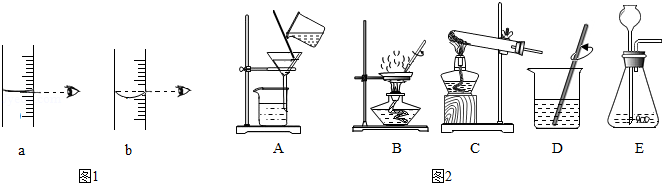
(1)实验室配制50g质量分数为6%的NaCl溶液,用到的玻璃仪器除试剂瓶、量筒、胶头滴管外,还需要 。量取读数时,如图视线角度正确的是 (填序号)。
(2)请根据如图装置或操作回答相关问题。
①选取图2中的序号,表示粗盐提纯的正确操作顺序为 。操作B的名称是 ,该操作中当 时,应停止加热。
②实验室用高锰酸钾固体制取氧气时,可选用的发生装置是 (填序号)。
某同学欲配制一定溶质质量分数的NaCl溶液,他准备了下列实验仪器。
请填空:
(1)配制时可按下列实验步骤进行:
计算→称量→量取→ 。
(2)称量时,NaCl固体粉末应放在托盘天平 (填"左盘"或"右盘")的纸片上。
(3)配制过程中为促进NaCl的溶解,还需要的一种玻璃仪器是 (填仪器名称)。
(4)量取一定体积的水,除了用量筒外,还需要用 (填仪器名称)。

实验室配制饱和澄清石灰水和质量分数为10%的氢氧化钠溶液,并进行有关实验。
下表是20℃时部分物质的溶解度数据。
物质 |
Ca(OH)2 |
NaOH |
CaCO3 |
Ca(HCO3)2 |
Na2CO3 |
NaHCO3 |
溶解度/g |
0.16 |
109 |
0.0065 |
16.6 |
21.8 |
9.6 |
(1)配制溶液。其中配制100g 10%氢氧化钠溶液的基本步骤是:
称取氢氧化钠固体﹣量取水﹣溶解﹣装瓶﹣贴标签。
①称取氢氧化钠固体的质量 g。
②已知水的密度为1g/cm3,用100mL量筒量取所需的水,画出水的液面。
③装瓶后贴标签,在标签上填写: 。
(2)进行性质探究实验,20℃时,根据数据回答下列问题:
①向饱和澄清石灰水中通入CO2直至过量,先生成CaCO3,再转化为Ca(HCO3)2,可观察到的现象是 。
②向10%氢氧化钠溶液中通入CO2直至过量,先生成Na2CO3,再转化为NaHCO3,可观察到的现象是 。
③理论上吸收4.4gCO2,需饱和澄清石灰水的质量至少为 g,或需10%氢氧化钠溶液的质量至少为 g.(计算结果精确到个位)

在农业生产上,常用质量分数为16%的氯化钠溶液选种。现要配制该氯化钠溶液100kg,需要氯化钠固体和水的质量各是多少?
学习了酸、碱、盐有关知识后,小明在实验室称量氢氧化钠固体,配制了溶质质量分数为10%的氢氧化钠溶液,进行以下探究:

(1)若图Ⅰ中游码标尺读数为1.8,则他称取的氢氧化钠质量是 g.
(2)图Ⅱ中反应的化学方程式是 .
(3)图Ⅲ中玻璃棒的作用是 ,当出现较多固体时,应 .
(1)要配制50g溶质质量分数为11%的氯化钠溶液,需要水的体积为 mL(水的密度是1g•mL﹣1);
(2)下列配制氯化钠溶液的过程图组顺序有误且不全,请将⑦框内所缺的实验步骤图用文字补全在横线上 ;

(3)小明同学按(1)和(2)的正确实验步骤配制好溶液后,发现所配制的氯化钠溶液溶质的质量分数小于11%,造成溶质质量分数偏小的原因可能是 (填序号).
A.称量时药品和砝码放反了 B.量取水时仰视量筒读数
C.所取用的氯化钠含有杂质 D.称量好的溶质倒入烧杯时有部分洒出
(4)金属与酸反应的剧烈程度反映了金属活动性的强弱.把形状、大小相同的纯金属
A、B、C、D同时放入装有足量稀盐酸的烧杯中,以下卡通图形象地表现了此实验现象,由图2可知,活动性最强的金属是 (填字母代号).
(5)请你写出锌与稀盐酸反应的化学方程式: .
(6)图3所示,将一支充满二氧化碳气体的试管倒插入氢氧化钠溶液中,一段时间后试管内液面上升了,请用化学方程式表示所发生的化学反应为: .

如图是初中化学中的一些常用实验仪器或装置:

(1)实验室用高锰酸钾制取氧气的化学方程式是 ,常用来收集氧气的装置是 (填字母序号).
(2)小李要配制50g质量分数为10%的NaCl溶液,并装入试剂瓶备用.
①要完成该实验,如图中还缺少的仪器是 (填名称).
②该实验过程中,玻璃棒的作用是 .
(3)用试纸测定溶液pH值的方法是:将小片pH试纸放在洁净的玻璃片上, ,与标准比色片比较,读出pH,若pH试纸事先用水湿润,测出的食醋pH值 (填“偏大”、“偏小”或“没有影响”).
室温为25℃时,某小组用无水氯化铜粉末制备氯化铜大晶体,制备过程如下:
步骤I:查阅资料,得到氯化铜溶解度数据如下
| 温度(℃) |
0 |
20 |
25 |
40 |
50 |
60 |
80 |
| 溶解度(g) |
69.2 |
74.5 |
76.4 |
81.8 |
85.5 |
89.4 |
98.0 |
步骤Ⅱ:配制少量CuCl 2热饱和溶液,冷却结晶,得到晶种。
步骤Ⅲ:把晶种悬挂在新配制的CuCl 2热饱和溶液中,室温下静置数天,形成大晶体。
步骤Ⅳ:取出大晶体,处理剩余的溶液(母液)。
根据以上信息,回答下列问题:
(1)用20mL蒸馏水(密度约为1g/mL)配制50℃的氯化铜饱和溶液。
①计算需称取CuCl 2的质量是 g。
②将称取的CuCl 2固体和20mL水倒入烧杯中, (填操作名称),直至固体完全溶解。
(2)母液中Cu 2+属于重金属离子,随意排放将导致环境污染。下列方法可用于母液处理的是 。
A.收集母液于敞口容器中,用报纸包住容器口,待水分自然蒸干后保存所得固体
B.向母液中加入适量AgNO 3,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
C.向母液中加入适量NaOH,充分反应后过滤,滤渣干燥保存,滤液倒入下水道
(3)若用铁粉置换出母液中的铜,100g母液需要铁粉的质量至少是 g(只列计算式,已知CuCl 2的相对分子质量为135)。
以下实验室配制一定溶质质量分数的氯化钠溶液的流程示意图.
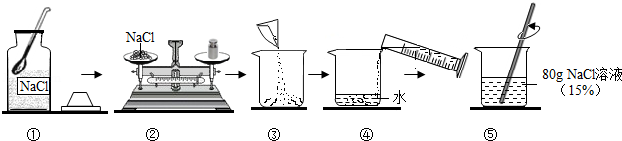
请根据示意图回答.
(1)托盘天平左盘中固体氯化钠的质量为 g,量筒中水的体积为 mL;
(2)上述溶液取10g加水40g进行稀释,所得氯化钠溶液的溶质质量分数是 .
溶液在生产、生活中起着十分重要的作用。请回答下列问题:
(1)可以作为溶质的是 。
A.只有固体 B.只有液体 C.只有气体 D.气体、液体、固体都可以
(2)配制100g质量分数为16%的氯化钠溶液,所需氯化钠的质量为 ,水的体积为 mL (水的密度近似看作1g/cm 3)。
(3)甲、乙两种不含结晶水的固体物质的溶解度曲线如图1.t 1℃时,甲物质的溶解度是 。t 2℃时,若从甲和乙两种物质的饱和溶液中析出等质量的固体,须蒸发掉较多水的是 (填"甲"或"乙")物质的饱和溶液。

(4)按图2所示装置,将液体X注入装有固体y的试管中,会导致U形管中右端液面升高。则可能的组合是 。
| 选项 |
x |
y |
| A |
水 |
氧化钙 |
| B |
水 |
硝酸铵 |
| C |
浓硫酸 |
水 |
| D |
稀盐酸 |
镁 |