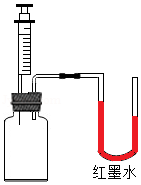
某兴趣小组做了如下实验:
①在止水夹K1、K2处于关闭状态时,将针筒A中溶液挤入试管B中,接着打开止水夹K1,发现D中的部分溶液被吸入试管B中,充分反应后,试管B留下的溶液也显红色;
②打开止水夹K2,风哨振动鸣叫,C中的部分溶液被吸入B和D中,反应后B、D中溶液都变为无色。
回答:
(1)步骤①中,充分反应后,试管B里的CO2最终转化为 (填化学式)和水。
(2)解释步骤②中“风哨振动鸣叫”的原因 。
(3)实验开始时C、D中两种溶液中溶质质量分数大小关系为:a% b%(选填“>”“=”“<”)
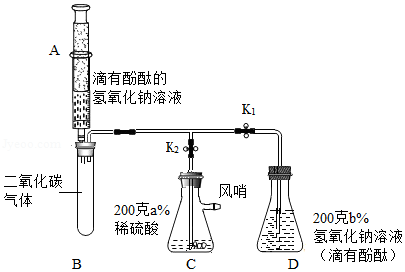
某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计实验探究:
[提出问题]甲烷燃烧后生成哪些物质?
[查阅资料]①含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;②白色无水CuSO4粉末遇水变蓝色;③CO与人体内的血红蛋白结合,会造成人中毒缺氧。
[猜想与假设]猜想一:CO2、H2O;猜想二:CO、H2O;猜想三:CO2、CO、H2O
[实验探究]将甲烷在一定量的纯净氧气中燃烧的产物依次通过如图装置(部分夹持、固定装置省略)进行验证:
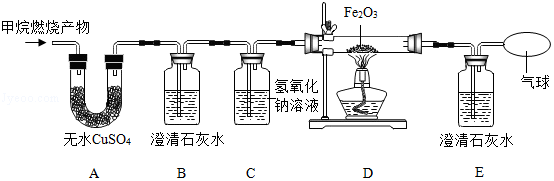
(1)实验过程中观察到A中白色粉末变为蓝色,B、E中澄清石灰水变浑浊,D中红棕色粉末变成黑色,由此推断猜想 成立。
(2)实验过程中B装置的作用是 ;该反应的化学方程式是 。
(3)D装置中发生反应的化学方程式是 。
(4)实验过程中用纯净O2而不用空气的原因是 。
(5)实验过程中B、C装置的顺序不能颠倒,原因是 。
[反思与交流]日常生活中,使用含碳燃料定要注意通风,防止 中毒。
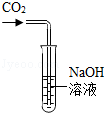
某化学兴趣小组在探究氢氧化钠的化学性质时,将二氧化碳通入盛有氢氧化钠溶液的大试管中,如图所示,结果同学们没有观察到明显现象,于是他们展开了如下探究。
探究一:二氧化碳是否与氢氧化钠溶液发生了化学反应?
取少量大试管中的液体,滴加足量的稀盐酸,观察到 ,证明二氧化碳与氢氧化钠发生了反应。
探究二:反应后大试管中溶液所含溶质的成分是什么?
[查阅资料]
1、CO2与碳酸钠溶液反应:Na2CO3+CO2+H2O═2NaHCO3
2、NaHCO3溶液呈碱性,能与NaOH反应,且与澄清石灰水反应生成白色沉淀
3、BaC12溶液呈中性,与Na2CO3反应生成白色沉淀,与NaHCO3不发生反应
小组成员经过分析讨论,一致认为溶质的成分为Na2CO3、NaHCO3、NaOH中的一种成几种。
[猜想假设]
猜想一:NaOH、Na2CO3
猜想二:Na2CO3
猜想三:
猜想四:NaHCO3
[实验探究]
序号 |
实验操作 |
实验现象 |
① |
取一定量大试管中的溶液于试管中,加入足量的BaCl2溶液 |
产生白色沉 |
② |
过滤 |
/ |
③ |
取一定量的滤液于试管中,加入澄清石灰水 |
没有明显现象 |
④ |
取一定量的滤液于另一支试管中,滴加适量酚酞溶液 |
|
[实验结论]
根据观察到的实验现象得出猜想 成立。
[实验反思]
化学反应是否发生,可以借助反应过程中伴随的实验现象来判断:也可以借生成物的性质来判断。
某化学兴趣小组用实验室常用药品(或溶液)对“NaOH溶液与稀盐酸是否恰好完全反应”进行探究。
[知识卡片]:氯化钠溶液显中性,氯化铜易溶于水。
[实验探究]:
(1)方案Ⅰ:某同学先向试管中加入约2mLNaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液恰好变为无色。
①实验结论 。
②从微观的角度分析,该反应的实质是 。
③在滴入稀盐酸的过程中,若观察到有少量气泡出现。请分析产生气泡的可能原因 (用化学方程式表示)。
(2)方案Ⅱ:
实验步骤 |
实验现象 |
结论 |
取2mLNaOH溶液于试管中,滴入一定量的稀盐酸,振荡后加入镁条 |
若 |
稀盐酸过量 |
若没有明显现象 |
NaOH溶液与稀盐酸恰好完全反应 |
[实验反思]:
(3)另有同学提出方案Ⅱ不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。
(4)除以上方案外,下列哪些物质单独使用,也能证明“NaOH 溶液与稀盐酸是否恰好完全反应” (填序号)。
A.铜片 B.pH试纸 C.氧化铜 D.紫色石蕊试液
某同学在学习了氢氧化钠的性质后发现,将二氧化碳通入氢氧化钠溶液中,没有观察到明显的现象,对反应是否发生产生了疑问?为此他进行了下列探究活动。
[提出问题]①二氧化碳与氢氧化钠溶液是否发生反应?②若发生反应,则可能生成什么产物?
[查阅资料]①将二氧化碳缓慢的通入氢氧化钠溶液中,先后发生如下反应:2NaOH+CO2═Na2CO3+H2O Na2CO3+H2O+CO2═2NaHCO3
②NaHCO3溶液呈碱性,能使酚酞试液变红,Ba(HCO3)2易溶于水。
[实验探究]
实验Ⅰ:将二氧化碳气体缓慢的通入一定量的氢氧化钠溶液。
实验Ⅱ:取Ⅰ中溶液少许与试管中,滴加2~3滴酚酞试液,溶液变红。
实验Ⅲ:再分别取Ⅰ中溶液少许于A、B两支试管中,向试管A中滴加足量的稀盐酸,有气泡产生,向试管B中滴加氯化钡溶液,有白色沉淀生成。
实验Ⅳ:为了进一步确定溶质的成分,将Ⅰ中剩余溶液低温蒸干,得到白色固体,取白色固体与试管中加热,将产生的气体通入足量的澄清石灰水,澄清石灰水变浑浊。
[实验分析与结论]
实验Ⅱ中:该同学 (填“能”或“不能”) 确定二氧化碳与氢氧化钠溶液发生了反应。
实验Ⅲ中:写出产生白色沉淀的化学方程式 ,由实验Ⅲ得出的结论是 ;
实验Ⅳ中:涉及的化学反应方程式为 ,CO2+Ca(OH)2=CaCO3↓+H2O.综上所述实验探究可知,实验Ⅰ所得溶液中溶质的成分为 ;
[反思交流]
通常检验二氧化碳时,常选用澄清石灰水,而不用氢氧化钠溶液的原因是 。
新型洗涤剂过氧碳酸钠(Na 2CO 4)固体,能瞬间清除衣服上的汗渍、果汁渍等顽固污渍。它与水反应生成碳酸钠和其他化合物,某学习小组对产生的其他化合物进行探究。
实验1:溶解样品。取适量洗涤剂样品于烧杯中,加入适量蒸馏水,使之完全溶解,有气泡产生并形成无色溶液a。产生的气体能使带火星的木条复燃。
[提出问题]过氧碳酸钠与水反应生成的其他化合物是什么?
[猜想与假设]猜想一:H 2O 2
猜想二:NaOH
猜想三:H 2O 2、NaOH
猜想一、二、三除了遵循质量守恒定律外,猜想H 2O 2的其他理由是 。
实验2:验证
| 实验步骤 |
实验现象 |
分析与结论 |
| ①取适量溶液a于小烧杯中,加入稍过量的氯化钙溶液,过滤,得到清液b |
产生白色沉淀 |
加入稍过量氯化钙的目的是 。 |
| ②取适量清液b于试管中,加入过量二氧化锰,振荡 |
|
证明过氧碳酸钠与水反应有H 2O 2生成 |
| ③将步骤②所得混合物静置,取少量清液于试管中,滴加氯化铁溶液 |
无明显现象 |
|
[实验结论]猜想 正确。写出过氧碳酸钠与水反应的化学方程式: 。
[反思与评价]该洗涤剂保存时应密封、防潮。
同学们对“二氧化碳溶于水是否与水反应”进行实验探究。请参与探究并回答下列问题。
[探究目的]二氧化碳溶于水是否与水反应
[探究思路]
(1)判断物质间是否发生化学反应的根本依据是 ,观察到的可以作为判断依据的宏观实验现象有 ;
(2)CO2溶于水无明显现象, (填“能”或“不能”)用观察的方法判断是否发生反应;
(3)“实验”的方法探究物质间是否反应的实验设计依据是:生成物和反应物的性质差异。
[提出猜想]
猜想一:二氧化碳溶于水不与水反应;
猜想二: 。
[实验设计]用四朵石蕊溶液染成紫色的干燥纸花设计如下实验:
序号 |
实验设计 |
① |
向第一朵纸花喷稀醋酸 |
② |
? |
③ |
将第三朵纸花直接放入盛有二氧化碳的集气瓶中 |
④ |
将第四朵纸花喷水后放入盛有二氧化碳的集气瓶中 |
(1)“实验设计①”中的稀醋酸还可用 (填物质名称)代替;
(2)“实验设计②”的具体内容是 ;
(3)“实验设计③”的目的是 。
[进行实验]观察记录实验现象,进行实验探究。
[实验结论]猜想二成立,支持猜想二成立的实验现象是 。
[反思交流]
(1)实验探究“无明显实验现象时是否发生化学反应”的核心思路有 (填字母序号);
A.设计对比实验
B.控制实验条件
C.获取事实证据
D.逻辑推理判断
(2)将稀盐酸加入氢氧化钠溶液中没有明显实验现象,判断两者混合是否发生化学反应的具体方法是 (任写1条)。
已知:Na2O为白色,Na2O2为淡黄色;Na2O+H2O=2NaOH.某兴趣小组对钠和铜的单质及其化合物的性质进行了如下实验探究。
①将铜片置于铁架台的铁圈上,用酒精灯加热,观察到铜片表面变黑;
②趁热将钠置于铜片表面,钠剧烈燃烧,有淡黄色物质生成,将此淡黄色物质转移到试管中待用,再用蒸馏水冲洗铜片,观察到铜片上钠燃烧处出现了光亮的铜斑;
③向盛装淡黄色物质的试管中滴加蒸馏水,观察到冒气泡,将带火星的木条伸入试管,木条复燃。
回答下列问题:
(1)步骤①产生的黑色物质是 ,步骤②淡黄色产物中氧元素的化合价为 价。
(2)步骤②中产生铜斑反应的另一产物,进一步与氧气反应也转化为淡黄色物质,则产生铜斑反应的化学方程式为 。
(3)步骤③产生的气体物质为 。
(4)猜想步骤③还可能有一种常见物质 (填化学式)生成,向反应后的溶液中滴加 溶液(可供选择的试剂:H2SO4、CuSO4、KOH、Na2CO3),观察到 的现象时,即证明了你的猜想。
蚊虫叮咬时能在人的皮肤内分泌出蚁酸刺激皮肤,课外小组同学决定对蚁酸进行探究。
[查阅资料]
1、蚁酸化学名称叫甲酸,化学式为HCOOH
2、蚁酸在一定条件下会分解生成两种氧化物
3、白色无水硫酸铜粉末遇水变蓝
[提出问题]蚁酸的酸碱性及分解产物是什么?
[猜想与假设]
猜想①:蚁酸的分解产物是水和二氧化碳;
猜想②:蚁酸的分解产物是水和一氧化碳;
猜想③:蚁酸的分解产物是一氧化碳和二氧化碳。
经讨论,小组同学认为猜想③是错误的,理由是 。
[实验探究]
1、探究蚁酸的酸碱性。
用pH试纸测得蚁酸溶液的pH值 7(填“>、<或=”),证明蚁酸溶液呈酸性。
2、探究蚁酸分解的两种产物。
为了确认蚁酸分解的所有产物,小组同学设计实验,将蚁酸分解的产物通入如图所示的实验装置,并观察现象。

[现象与结论]
实验中观察到A中无水硫酸铜变蓝,B中澄清石灰水未变浑浊,D中黑色粉末逐渐变红,E中澄清的石灰水变浑浊。
(1)写出E中发生的反应的化学方程式 ;
(2)通过对实验现象的分析,上述猜想 正确。
[实验反思]
(3)从环保的角度考虑,上述实验装置设计上存在的不足之处是 。
[拓展应用]
(4)人们被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒,下列物质中你会选择的物质是 。
A.NaOH溶液 B.食醋 C.食盐水 D.肥皂水
某学习小组的同学在整理归纳反应规律时发现,有些化学反应发生时没有伴随明显的现象,他们就此进行了以下探究。
[提出问题]
怎样证明NaOH溶液分别与CO2及稀盐酸发生了反应?
[分析讨论]
同学们讨论后认为,可以用两种思路探究上述反应是否发生。
思路Ⅰ:验证有 ;思路Ⅱ:验证反应物减少或消失。
[实验探究]同学们分两组分别设计方案进行探究。
组别 |
第一组 |
第二组 |
实验示意图 |
|
|
[实验结论]
(1)第一组同学将充满CO2气体的试管倒扣在NaOH溶液中,观察到试管内液面升高,认为NaOH溶液与CO2发生了反应。但有同学指出,还应进行CO2与 反应的对比实验才能得出这一结论。
(2)第二组的小文同学向丙中滴入无色酚酞溶液后,观察到溶液颜色 ,得出NaOH溶液与稀盐酸发生了反应的结论。小亮同学向丁中滴入AgNO3溶液后,观察到有白色沉淀生成,由此他认为NaOH溶液与稀盐酸反应生成了NaCl.你认为小亮的结论是 的(填“合理”或“不合理”)。
(3)第二组同学进一步讨论后认为,如果将乙中的溶液蒸发结晶,再将得到的晶体溶于水,若在室温下测得该溶液的pH (填“>”、“<”或“=”)7时,则能证明有NaCl生成。
[拓展应用]第一组同学向反应后的溶液中加入某无色溶液,观察到有白色沉淀生成,也得出了NaOH溶液与CO2发生了反应的结论。生成白色沉淀的化学方程式为 (只写一个)。
实验室常用下列装置制取气体,请你根据所学知识回答下列问题。
(1)仪器a的名称是 。
(2)实验室用氯酸钾制取氧气时,选用的发生装置是 (填字母序号)。若改用图1装置收集氧气,则气体应从 端进(填“a”或“b”)。
(3)实验小组同学取一定浓度的盐酸与石灰石反应制取气体,反应的化学方程式为 ;将生成的气体通入澄清石灰水中,未见变浑浊。为探究其原因,小组同学讨论后做出如下猜想:
[作出猜想]A.石灰水已经完全变质;B.气体中有挥发出来的HCl气体
[实验探究]
小组同学设计了如下实验来验证。请你帮助完成实验,填写以下表格:
实验步骤 |
实验现象 |
实验结论 |
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡 |
|
猜想A不成立 |
②将生成的气体通入 溶液中 |
产生白色沉淀 |
气体中有HCl猜想B成立 |
[查阅资料]
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O=2NaHCO3
[拓展延伸] 如果用上述原料制取一瓶干燥纯净的二氧化碳气体,所选仪器的连接顺序为B→ → →C(填字母序号)。
某同学用相同的两个玻璃罩探究蜡烛(主要含碳、氢元素)在其中的燃烧情况。
实验Ⅰ:如图甲,将三个盛有等量澄清石灰水的敞口容器编号,并等距离固定在铁丝上。在铁丝两侧点燃高、低两支蜡烛,立即用玻璃罩扣上,使铁丝处于正中位置。三个容器内石灰水变浑浊所需的时间如表格所示。
容器编号 |
1 |
2 |
3 |
时间/秒 |
3.2 |
5.0 |
11.1 |
实验Ⅱ:如图乙,将三支温度计的玻璃泡分别置于玻璃罩内的不同位置。点燃蜡烛,一段时间后,观察到B的示数明显增大,A、C示数增大不明显。
(1)根据表中数据,推测实验Ⅰ中,先熄灭的是 (填“高”或“低”)蜡烛。
(2)通过上述实验,解释1号容器内澄清石灰水先变浑浊的原因 。
(3)结合实验及相关知识分析,高层楼房着火时,一般情况下,合理的做法有 (可多选)。
A.排队乘电梯依次撤离
B.向着火楼层的上方撤离
C.用湿毛巾捂住口鼻,弯腰跑离火场
D.若火势不大,可用灭火器材将火扑灭
在一次实践活动中,某小组同学对游泳馆内清澈湛蓝的池水产生了浓厚的兴趣,他们对池水呈现蓝色的原因、溶质成分、池水处理方法和对环境的影响,展开了连续性问题探究。
活动一:查阅相关资料,寻找池水呈现蓝色的原因。
[查阅资料]水对蓝光的反射作用使水呈现蓝色,水越深蓝色越深。
[交流讨论]光反射引起池水呈现蓝色,从微观角度分析,水分子本身 改变。有同学质疑:池水呈现蓝色可能加入了硫酸铜。
活动二:检验泳池水中是否加入硫酸铜。
实验步骤 |
实验现象 |
实验结论 |
1.取少量泳池水于试管中,滴加几滴 |
有蓝色沉淀产生 |
池水中含有Cu2+ |
2.另取少量泳池水于试管中,满加足量稀盐酸,无明显现象,再滴加几滴 |
产生白色沉淀 |
池水中含有的离子是 (用符号表示) |
[实验小结]泳池水中含有硫酸铜。步骤1发生反应的化学方程式为 。
[实验调查]同学们咨询了泳馆的管理人员,得知:
①池水是定期净化再利用的。
②池水中硫酸铜起到抑制藻类繁殖等作用。
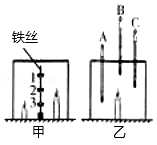
活动三:设计泳池水净化模拟实验装置(如图)。
[进行实验]小组同学取一定量的泳池污水于水槽中,再加入适量的絮凝剂(聚合氯化铝),10分钟后,打开水泵使水循环,在此过程中石英砂的作用是 。
[归纳提升]①为保证净化后的池水安全、卫生,还应增加的一个净水步骤是 。
②从爱护水资源角度分析,池水净化再利用的好处是 。
某化学兴趣小组用大理石和稀盐酸反应制取CO2,当观察不到气泡产生时发现固体仍有剩余,同学们对此进行了探究(杂质不溶于水且不与酸反应)。请你参加探究并回答相关问题:
[提出问题]不再产生气泡的原因是什么?
[猜想假设]
猜想一: ;
猜想二:生成物或杂质附着在大理石表面阻碍反应继续进行;
猜想三:剩余固体中无碳酸钙。
[实验探究一:验证猜想一]
(1)甲同学取上述反应后的溶液,测得溶液pH=2;甲同学的结论:猜想一不成立;反应前稀盐酸的pH (填“<”“>”或“=”)2。
(2)乙同学认为甲的实验设计和结论不严谨并补充了如下两个实验:
实验①配制 (填物质名称或化学式)溶液,测得该溶液pH=7; 实验②在试管中加入适量水和紫色石蕊溶液后持续通入CO2,溶液变为 色;乙同学的结论:猜想一成立,他的依据是 。
(3)丙同学认为甲、乙的实验结论均不严谨或有错误并再次改进和补充了实验:实验③向试管中加入适量水后持续通入CO2 至饱和,测得溶液pH=5.6;丙同学的结论:猜想一不成立,他的依据是 。
[实验探究二:验证猜想二]
(4)丁同学不断振荡反应容器观察到仍无任何气泡产生;丁同学的结论:猜想二 (填“成立”或“不成立”)。
[实验探究三:验证猜想三]
(5)戊同学实验后得出结论:猜想三不成立,他设计的实验是 。探究活动结束后,老师进行了点评,同时启发同学们针对此探究还可以进一步反思。
[反思拓展]
(6)该实验探究活动说明:反应物相互接触后能否反应的影响因素有 。
(7)根据所学化学知识,任写一例该因素影响化学反应的实例: 。
某化学活动小组同学发现,不同物质在发生变化时,即使实验现象相同,其变化的实质也可能存在着本质的区别。
同学们利用如图所示的装置进行了以下两个实验。
实验Ⅰ:在集气瓶底部放入一定量的硝酸铵固体,再将注射器中的水注入瓶中,振荡。
实验Ⅱ:向充满二氧化碳的集气瓶中注入一定量的氢氧化钠溶液,振荡。
[现象分析]上述两个实验过程中,U形管中液面均出现 (填“左高右低”或“左低右高”)现象,其中实验Ⅰ没有发生化学变化,实验Ⅱ发生了化学变化,其反应的化学方程式为 。
[归纳总结]相同的实验现象既可以由物理变化引起,也可以由化学变化引起。
[拓展延伸]在探究白色固体的组成时,也需考虑相同现象是否存在着本质区别。
有一包白色固体,可能含有氧化钙、氢氧化钙、碳酸钙中的一种或几种。为了探究白色固体的成分,同学们做了以下实验。
步骤1:甲同学取一定量的白色固体于试管中,加入一定量的水后振荡,触摸试管外壁,没有感觉到放热现象,说明白色固体中没有 。
试管底部有白色不溶物,甲同学认为白色固体中一定含有碳酸钙,乙同学认为上述现象不足以证明碳酸钙的存在,其理由是 。
步骤2:为进一步得出准确的结论,他们进行了下面所示实验。
实验操作 |
实验现象 |
实验现象 |
(1)将步骤1试管中物质过滤,向滤液中滴加 。 |
溶液由无色 变成红色 |
白色固体中 含有 |
(2)向滤出的固体中加入足量的 。 |
有气泡产生 |