有机物A常用于食品行业。已知9.0 g A在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重5.4 g和13.2 g,经检验剩余气体为O2。
(1)A分子的质谱图如下图所示,从图中可知其相对分子质量为 ,则A的分子式是 。

(2)A能与NaHCO3溶液发生反应,A一定含有的官能团名称是 。
(3)A分子的核磁共振氢谱有4个峰,峰面积之比是1:1:1:3,则A的结构简式是 。
(4)0.1 mol A与足量Na反应,在标准状况下产生H2的体积是 L。
(5)A在一定条件下可聚合得到一种聚酯,用于制造手术缝合线,其反应的化学方程式是 。
已知四种强电解质溶液,分别含有下列阴、阳离子中的各一种,并且互不重复:Ba2+、H+、K+、NH4+、CO32-、Cl-、OH-、SO42-.将这4种溶液分别标记为A、B、C、D,其相互关系如下:
①向A或D中滴入C,均生成白色沉淀;
②A和B混合加热产生的气体能被D吸收;
③A和D反应生成的气体能被B吸收。
请回答下列问题:
(1)A、B、C、D中电解质的化学式:
A________、B、________C、________D________。
(2)若将B和D混合,反应的离子方程式为______________________。
(3)若将③中生成的气体用过量的B吸收,则反应的离子方程式为___________________。
有A、B、C、D四种无色溶液,它们分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为::①A+D→溶液+气体,②B+C→溶液+沉淀,
③B+A→溶液+沉淀X,④D+B→溶液Y+沉淀,⑤溶液Y+沉淀X→溶液+气体.
(1)根据以上记录确定:A__________ B___________ C___________ D___________
(2)写出①、③各反应的离子方程式:
①_______________③______________
有甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、CO32-、SO42-中的不同阴、阳离子各一种组成,已知:①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成;②0.1mol/L乙溶液中c(H+)>0.1mol/L;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成。
(1)它们的化学式分别为甲_________、乙_________、丁_________。
(2)写出甲溶液和丁溶液反应的离子方程式:_________________________。
(3)检验乙中阴离子所用试剂的名称是____________________。
1mol仅含C、H、O三种元素的有机物A在稀硫酸中水解生成1molB和1molC,B分子中N(C):N(H)=4:5,135<Mr(B)<140;C与B分子中C原子数相同,且:Mr(B)=Mr(C)+2.(N代表原子个数,Mr代表相对原子质量)
(1)C的分子式为_______________,A的摩尔质量为______________;
(2)B的分子具有高度对称性,苯环上的一氯取代物只有一种.B能与金属Na反应但不能与NaOH反应.写出B的结构简式______________;
(3)C有多种同分异构体,其中属于芳香酯类的同分异构体有__________种,写出其中一种的结构简式____________;
(4)C分子中苯环上有两个取代基,且苯环上的一氯取代物有两种.写出A的结构简式______________。
由乙烯和其他无机原料合成环状酯,其合成过程如下(水及其他无机产物均已省略)
请分析后回答下列问题:
(1)写出下列反应的反应类型:①______________;②______________;
(2)D物质中的官能团名称为______________;
(3)物质X与A互为同分异构体,则X的结构简式为______________;
(4)写出下列转化的化学方程式:A→B______________;
B+D→______________。
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X的原子结构示意图为________________ Y原子核外价电子排布图 ________________。
(2)XZ2与YZ2分子的立体结构分别是________和________________,相同条件下两者在水中的溶解度较大的是__________(写分子式),理由是_________________________。
(3)Q的元素符号是__________,它的基态原子的核外电子排布式为______________,在形成化合物时它的最高化合价为__________。
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键_____________________。
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素的核外电子数和电子层数相等 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能如下: |
| I1=738 kJ·mol-1 I2=1451 kJ·mol-1 I3=7733 kJ·mol-1 I4=10540 kJ·mol-1 |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:______________________________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有__________个方向,原子轨道呈_______形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 该同学所画的电子排布图违背___________________。
该同学所画的电子排布图违背___________________。
(4)G位于________族________区,该元素的核外电子排布式为_________________。
(5)DE3中心原子的杂化方式为____________,用价层电子对互斥理论推测其空间构型为__________。
(6)检验F元素的方法是____________,请用原子结构的知识解释产生此现象的原因:_____________。
已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、H均为常见的化合物;B和乙为淡黄色固体,E的式量比D的式量大16,在一定条件下,各物质间相互转化关系如下图所示(产物中水已忽略)。
(1)写出下列物质的化学式:丙_______、B_______、D_______。
(2)写出有关反应的化学方程式:
B+H2O _______________________________________
D + 丙 ______________________________________
F+ 丙 _______________________________________
(1)下图中A为淡黄色固体,B、C为溶液,D为气体,E、F为白色沉淀。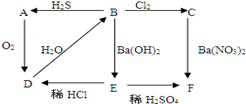
①根据如图转化关系,填写下列物质的化学式:A为______D为______E为______
②写出B→C的化学方程式_________________________
③写出B→A的化学方程式_________________________
(2)把某黑色固体单质A加热至红热,投入到一种无色溶液B中,产生由两种气体组成的混合气体X,将X做如下图所示的实验:
①由此可推断各物质的化学式为:C为___________X为___________
②写出A投入B中的化学方程式______________________
③写出D的稀溶液与F反应的离子方程式__________________
X、Y、Z、W是元素周期表前四周期中的四种常见元素,相关信息见下:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63,中子数为34 |
(1)Z位于元素周期表第__________周期第__________族,Y和Z的最高价氧化物对应的水化物的酸性较强的是_____________(写水化物的化学式)。
(2)XY2是一种常用的溶剂,XY2的分子中存在_____________个σ键.在H-Y、H-Z两种共价键中,键的极性较强的是_____________,键长较长的是__________;
(3)W的基态原子核外电子排布式是__________W2Y在空气中煅烧生成W2O化学方程式是__________。
碳酸二甲酯(DMC)是一种低毒性的绿色化学品,可用于代替高毒性的光气(COCl2)作羰基化试剂。DMC的合成路线如图.完成下列填空.

已知:RCO-OR1+R2O-H→RCO-OR2+R1O-H (称酯交换反应)
(1)写出反应类型:反应①_________________;
(2)写出结构简式:X____________________;
(3)已知物质Y与DMC互为同分异构体,Y的水溶液呈酸性,在一定条件下2molY能生成1mol分子中含六元环结构的有机物Z,则Z的结构简式为____________________;
(4)DMC与双酚( )在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:______________________________。
)在一定条件下可发生类似反应①的反应,生成芳香族聚碳酸酯,写出反应的化学方程式:______________________________。
Ⅰ.A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E是短周期中金属性最强的元素,F与G位置相邻,G是同周期元素中原子半径最小的元素.请用化学用语回答:
(1)推断B元素在元素周期表中的位置_______________________。
(2)A与D形成的18电子的化合物与FD2化合生成一种强酸,其化学方程式为_____________。
(3)用电子式表示化合物E2F的形成过程_______________________。
(4)下图为某新型发电装置示意图,其负极电极反应为_______________________。

(5)在101kPa、25℃下,16g液态C2A4在D2中完全燃烧生成气体C2,放出312kJ热量,则C2A4和D2反应的热化学方程式为_______________________。
Ⅱ.A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去)。
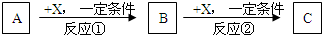
试回答:
(1)若X是强氧化性单质,则A不可能是___________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的 化 学式为___________。
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为___________。
H是一种新型香料的主要成分之一,其结构中含有三个六元环,H的合成路线如下(部分产物和部分反应条件略去):
已知:
①B中核磁共振氢谱图显示分子中有6种不同环境的氢原子.
②RCH=CH2+CH2=CHR′ CH2=CH2+RCH=CHR′
CH2=CH2+RCH=CHR′
③D和G是同系物
请回答下列问题:
(1)用系统命名法命名(CH3)2C=CH2:_________________________。
(2)A→B反应过程中涉及的反应类型有______________________。
(3)写出D分子中含有的官能团名称:_____________________。
(4)写出生成F与足量氢氧化钠溶液在加热条件下反应的化学方程式:_________________________。
(5)写出E在铜催化下与O2反应生成物的结构简式:_________________________。
(6)同时满足下列条件:①与FeCl3溶液发生显色反应;②能发生水解反应;③苯环上有两个取代基的G的同分异构体有________种(不包括立体异构),其中核磁共振氢谱为5组峰的为_________________(写结构简式)。
A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件均未列出)。
(1)若A是常见金属单质,与B的水溶液反应生成C和D,D、F是气体单质,D在F中燃烧时发出苍白色火焰.则F所对应的元素在周期表位置是____________,反应②的离子方程式为_________________。
(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属.且③④两个反应都有红棕色气体生成,则反应④的化学方程式为_________________。
(3)若A、D、F都是短周期非金属单质,且A、D所含元素同主族,A、F所含元素同周期,C是一种重要工业原料气,则1molB中含有______个共价键,分子E的结构式是__________。