工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下:
请回答下列问题:
(1)步骤①所得废渣的成分是(写化学式),操作I的名称。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是。
③中X试剂为 。
(3)④的离子方程式为。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH |
1.3 |
1.4 |
1.5 |
1.6 |
1.7 |
1.8 |
1.9 |
2.0 |
2.1 |
| 钒沉淀率% |
88.1 |
94.8 |
96.5 |
98.0 |
98.8 |
98.8 |
96.4 |
93.1 |
89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)<。〖已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39〗
(5)该工艺流程中,可以循环利用的物质有和。
[有机化学基础]
可用来制备抗凝血药,通过下列路线合成:
请回答:
(1)B→C的反应类型是____________________。
(2)下列关于化合物G的说法不正确的是_____。
A 分子式是C9H6O3 B 能与金属钠反应
C分子中含有4种官能团 D能与液溴反应
E. 1 mol G最多能和4mol氢气反应 F. 1 mol G最多能和3 molNaOH反应
(3)写出A与银氨溶液反应的化学方程式。
(4)写出D→E的化学方程式___________________________________________。
(5)写出F和过量NaOH溶液共热时反应的化学方程式_______________________。
(6)化合物E的同分异构体很多,除E外符合下列条件的共种。
①含苯环且能与氯化铁溶液显色;②苯环上有两个取代基;③含酯基。
【化学选修5——有机化学基础】
姜黄素(分子式为C21H20O6)存在姜科植物姜黄等的根茎中,具有抗基因突变和预防肿瘤的作用。其合成路线如下:
已知:
i.
ii.
(R1、R2、R3为烃基或氢原子)
iii. E的核磁共振氢谱中有两个峰
请回答下列问题:
(1)E中含有的官能团名称是。
(2)B物质的名称为;试剂X为。
(3)姜黄素的结构简式为。
(4)E →G反应的化学方程式为;其反应类型是 。
(5)下列有关香兰醛的叙述正确的是(填正确答案编号)。
a.香兰醛能与NaHCO3溶液反应
b.香兰醛能与浓溴水发生取代反应
c.能与FeCl3溶液发生显色反应
d.1 mol香兰醛最多能与3 molH2发生加成反应
(6)符合下列条件的香兰醛(K)的同分异构体有种:①属于芳香族化合物 ②与氯化铁溶液发生显色反应 ③苯环上只有两个取代基 ④存在羰基的结构。写出香兰醛(K)的同分异构体中符合下列条件的结构简式。
①苯环上的一氯取代物只有2种;
②1mol该物质与烧碱溶液反应,最多消耗3molNaOH;
③核磁共振氢谱中有4种吸收峰。
在原子序数1—18号元素中,按要求用合适的化学用语填空
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是_____________。
(4)气态氢化物最稳定的化学式是_____________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_____________。
(6)电子数为10的分子(写5个)
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下: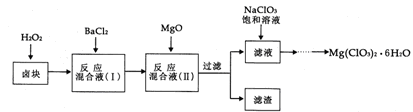

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②四种化合物的溶解度(S)随温度(T)变化曲线如图所示。
回答下列问题:
(1)加速卤块在H2O2溶液中溶解的措施有:(写出一条即可)。
(2)加入MgO的作用是;滤渣的主要成分为。
(3)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为①蒸发结晶;②;③____;④过滤、洗涤。
(4)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20.00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.l000 mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为: 。
。
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式(还原产物为Cl-):;
②产品中Mg(ClO3)2·6H2O的质量分数为(保留一位小数)。
计算题将等体积的4×10﹣3mol/L的AgNO3溶液和4×10﹣3mol/L的K2CrO4溶液混合,是否析出Ag2CrO4沉淀?[已知Ksp(Ag2CrO4)=9.0*10﹣12].
(14 分)CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值化学品是目前的研究目标。
(1)250℃时,以镍合金为催化剂,向4 L密闭容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2(g)+CH4(g) 2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
2CO(g)+2H2(g)。平衡体系中各组分体积分数如下表:
| 物质 |
CH4 |
CO2 |
CO |
H2 |
| 体积分数 |
0.1 |
0.1 |
0.4 |
0.4 |
①此温度下该反应的平衡常数K=。
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H="-890.3" kJ·mol-1
CO(g)+H2O (g)=CO2(g)+H2 (g) △H="2.8" kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H="-566.0" kJ·mol-1
反应CO2(g)+CH4(g) 2CO(g)+2H2(g) 的△H=;
2CO(g)+2H2(g) 的△H=;
③在不同温度下催化剂的催化效率与CO的生成速率如右图所示。t1~t2℃时,温度升高而CO的生成速率降低的原因是;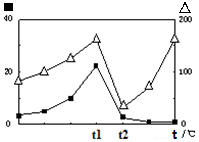 (∆代表CO的生成速率,■代表催化剂的催化效率)
(∆代表CO的生成速率,■代表催化剂的催化效率)
④为了提高该反应中CH4的转化率,可以采取的措施是;
⑤若再向容器中同时充入2.0 mol CO2、6.0 mol CH4、4.0 molCO 和8.0 molH2,则上述平衡向(填“正反应”或“逆反应”)方向移动。
(2)以CO2为原料可以合成多种物质。
①可降解二氧化碳聚合物是由CO2加聚而成,写出其结构简式:;
②以氢氧化钾水溶液作电解质进行电解,CO2在铜电极上可转化为甲烷,该电极反应方程式为。
某混合物的水溶液中,只可能含有以下离子中的若干种:K+、Mg2+、Fe3+、Al3+、NH4+、Cl-、CO32-和SO42-。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体0.672L(标准状况下),但整个过程中无沉淀生成。
③第三份加入足量BaCl2溶液后得干燥沉淀6.63g,沉淀经足量盐酸洗涤,干燥后剩余4.66g。
请回答:
(1)c(CO32-)=______ mol/L。
(2)K+是否存在?_____ (填“存在”或“不存在”);若存在,浓度范围是________ (若不存在,则不必回答第2问)。
(3)根据以上实验,不能判断哪种离子是否存在? ,若存在,这种离子如何进行检验?
已知锦纶和涤纶是常用的布料,已知涤纶的结构简式为:
①合成涤纶的单体是________、________
②合成涤纶的反应方程式和反应类型分别是__________________、______________。
某工厂采用如图工艺处理镍钴矿硫酸浸取液(含 和 )。实现镍、钴、镁元素的回收。
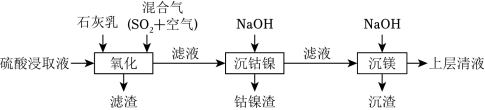
已知:
|
物质 |
Fe(OH)3 |
Co(OH)2 |
Ni(OH)2 |
Mg(OH)2 |
|
Ksp |
10﹣37.4 |
10﹣14.7 |
10﹣14.7 |
10﹣10.8 |
回答下列问题:
(1)用硫酸浸取镍钴矿时,提高浸取速率的方法为 __________(答出一条即可)。
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸( ), 中过氧键的数目为__________。
(3)“氧化”中,用石灰乳调节 , 被 氧化为 ,该反应的离子方程式为__________( 的电离第一步完全,第二步微弱);滤渣的成分为 、__________(填化学式)。
(4)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如图。 体积分数为__________时, (Ⅱ)氧化速率最大;继续增大 体积分数时, (Ⅱ)氧化速率减小的原因是__________。
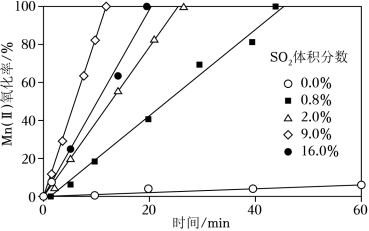
(5)“沉钴镍”中得到的 (Ⅱ)在空气中可被氧化成 ,该反应的化学方程式为__________。
(6)“沉镁”中为使 沉淀完全( ),需控制 不低于__________(精确至 )。
甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①3O2(g)═2O3(g)ㅤK1ㅤΔH1=285kJ•mol﹣1
②2CH4(g)+O2(g)═2CH3OH(l)ㅤK2ㅤΔH2=﹣329kJ•mol﹣1
反应③CH4(g)+O3(g)═CH3OH(l)+O2(g)的ΔH3= kJ•mol﹣1,平衡常数K3= (用K1、K2表示)。
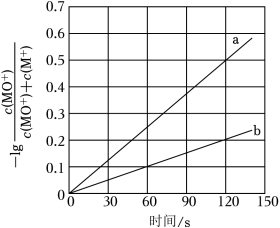
(2)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O3反应可得MO+。MO+与CH4反应能高选择性地生成甲醇。分别在300K和310K下(其他反应条件相同)进行反应MO++CH4═M++CH3OH,结果如图所示。图中300K的曲线是 (填“a”或“b”)。300K、60s时MO+的转化率为 (列出算式)。
(3)MO+分别与CH4、CD4反应,体系的能量随反应进程的变化如图所示(两者历程相似,图中以CH4示例)。
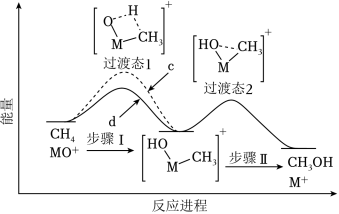
(i)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ii)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则MO+与CD4反应的能量变化应为图中曲线 (填“c”或“d”)。
(iii)MO+与CH2D2反应,氘代甲醇的产量CH2DOD CHD2OH(填“>”“=”或“<”)。若MO+与CHD3反应,生成的氘代甲醇有 种。
选择适宜的材料和试剂设计一个原电池,以便完成下列反应: 2FeCl3+Cu 2FeCl2+CuCl2。画出原电池的示意图并写出电极反应。
2FeCl2+CuCl2。画出原电池的示意图并写出电极反应。
有一包白色固体粉末,由CaCO3、Na2SO4、KCl、Ba(NO3)2、CuSO4中的几种物质组成,取样品进行如下实验(假设下列过程中,能反应的物质之间的反应恰好完全):
(1)步骤“①”所用分离方法叫做 ,要从步骤②所得“无色溶液”中提取溶剂,所用分离方法叫做 。
(2)写出实验过程中发生化学反应的离子方程式 。
(3)固体粉末中一定不存在的物质是(填化学式,下同) ;一定存在的物质是 。
(4)将固体粉末可能的组成填入下表(可以不填满,也可以再补充)
| 序号 |
化学式 |
| Ⅰ |
|
| Ⅱ |
|
| Ⅲ |
(5)设计一个实验,进一步确定混合物的组成,简述实验操作、现象和结论。
痕检是公安机关提取犯罪嫌疑人指纹的一种重要方法,硝酸银显现法就是其中的一种:人的手上有汗迹,用手拿过白纸后,手指纹线就留在纸上.如果将硝酸银溶液小心地涂到纸上,硝酸银溶液就跟汗迹中的氯化钠作用,生成氯化银,其反应的化学方程式是.反应的类型是反应,氯化银在光照条件下分解生成银粒和另一种单质,其反应的化学方程式是.反应的类型是反应,银粒呈灰褐色,随着反应的进行,银粒逐渐增多,由灰褐色逐渐变成黑色,从而显现出黑色的指纹线.
(1)臭氧可用于净化空气、饮用水消毒、处理工业废物和作为漂白剂。
①臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)===3Ag2O(s);△H =" -235.8" kJ/mol;
己知:2 Ag2O(s)===4Ag(s)+O2(g);△H = +62.2kJ/mol;
则反应 2O3(g)= 3O2(g)的△H = kJ/mol;
②科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧。臭氧在阳极周围的水中产
生,阴极附近的氧气则生成过氧化氢,阴极电极反应式为。 (2)用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)N2(g)+CO2(g)某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃) 条件下反应,反应进行到不同时间测得各物质的浓度如下:
(2)用活性炭还原法处理氮氧化物,有关反应为:C(s)+2NO(g)N2(g)+CO2(g)某研究小组向某密闭的真空容器(假设容器体积不变,固体试样体积忽略不计)中加入NO和足量的活性炭,恒温(T1℃) 条件下反应,反应进行到不同时间测得各物质的浓度如下: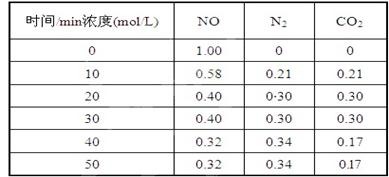
①在10 min~20 min的时间段内,以CO2表示的反应速率为;
②写出该反应的平衡常数的表达式K=;
③下列各项能作为判断该反应达到平衡状态的是(填序号字母);
| A.容器内压强保持不变 | B.2v正(NO)=v逆(N2) |
| C.容器内CO2的体积分数不变 | D.混合气体的密度保持不变 |
④30 min时改变某一条件,反应重新达到平衡,则改变的条件可能是;
⑤一定温度下,随着NO的起始浓度增大,则NO的平衡转化率 (填“增大”、“不变”或“减小”)。