现有一份含Fe2O3、Al2O3、SiO2的混合物,为测定其中铁元素的含量,进行如下实验:
①称取混合物A g,滴加过量盐酸充分反应后过滤;
②在滤液中滴加过量氢氧化钠溶液充分反应后过滤;
③洗涤②所得沉淀,烘干后称重,质量为B g。
回答下列问题:
(1)步骤①中过滤所用的玻璃仪器有 ;
(2)步骤①所得滤液中铁元素的存在形式是 (填离子符号),怎样检验它的存在(写出实验操作和现象) ;
(3)步骤②中涉及的离子方程式是 、 、 ;
(4)该混合物中铁元素的质量分数为 (用含A、B的式子表示)。
如图实验装置用于验证某些物质的性质。在试管A中装入足量的固体NaHCO3,D为固定蚊香的硬纸片。试回答下列问题:

(1)在A试管内发生反应的化学方程式是______________________。
(2)B装置的作用是____________________________________。
(3)在双球干燥管内发生反应的化学方程式为______________________。
(4)双球干燥管内观察到的实验现象是____________________________。
(5)若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是_____________________。
二氧化硫是硫的重要化合物,在生产、生活中有广泛应用。实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。

(1)如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装
置是 (填写字母),e装置中的导管作用为 。
(2)工业上制备Na2S2O3反应原理为:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2,某研究小组在实验室制备Na2S2O3·5H2O流程如下:

吸硫装置如图所示:

①装置B的作用是检验装置A中SO2的吸收效率,B中试剂是 ,表明SO2吸收效率低的实验现象是B中溶液 。
②为了使SO2尽可能吸收完全,在不改变A中溶液浓度、体积的条件下,除了及时搅拌反应物外,还可采取的合理措施是 。
③用双线桥表示下面化学反应的电子转移方向和数目:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。
④Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:准确称取0.214g KIO3固体配成溶液,加入过量KI固体和H2SO4溶液,再向其中加入Na2S2O3与之反应,消耗Na2S2O3 溶液的体积为24mL时恰好完全反应。则c(Na2S2O3)= 。
(已知:IO3-+5I-+6H+=3I2+3H2O 2S2O32-+I2=S4O62-+2I-)
如图所示,将仪器A中的浓盐酸滴加到盛有MnO2的烧瓶中,加热后产生的气体依次通过装置B和C,然后再通过加热的石英玻璃管D(放置有铁粉)。请回答:
(1)仪器A的名称是______________,烧瓶中反应的化学方程式是_____________________。
(2)装置B中盛放液体是___________,气体通过装置B的目的是____________________。
装置C中盛放的液体是_________,气体通过装置C的目的是______________________。
(3)D中反应的化学方程式是_________________。
(4)烧杯E中盛放的液体是__________,反应的离子方程式是______________________。
(5)资料表明D中产物有以下性质:①受热易升华,冷却后易凝华;②遇H2O(g)剧烈反应。为收集D中产物,在D与E之间,除增加收集装置外,还需要增加_________装置。
非金属元素及其化合物在工农业生产中应用非常广泛。请回答以下问题:
I.氯及其化合物
ClO2与Cl2的氧化性相近。在自来水消毒和果蔬保鲜等方面应用广泛,某兴趣小组通过如下图所示,对其制备、吸收、释放和应用进行了研究。

(1)A中发生反应的化学方程式: 。
(2)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是 。
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为 ,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 。
II.硫及其化合物:
(1)选择以下装置,通过实验现象依次完成以下验证:SO2具有酸性、氧化性、还原性、漂白性。其仪器的连接顺序为 。

(2)利用下图装置能证明SO2不与BaCl2溶液反应,通入X气体可排除干扰达到实验目的是

A CO2 B NH3 C O3 D N2 E NO2
C发生的离子方程式 。
(3)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

按上述方案实验,当消耗标准I2溶液25.00 mL时,滴定完毕,滴定终点的标志 ,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g·L-1。
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等。某小组模拟制备氨基甲酸铵的反应为:2NH3(g)+CO2(g) NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
NH2COONH4(s) ΔH<0。(温度对反应的影响比较灵敏)
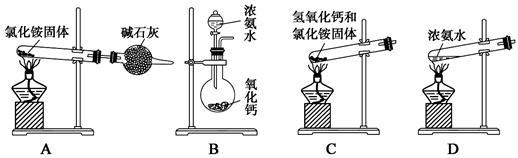
(1)如用下图装置和选用的试剂制取氨气,其中错误的是________;氨气的实验室制法的化学方程式是 。
(2)制备氨基甲酸铵的装置如下图所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中。 当悬浮物较多时,停止制备。(注:CCl4与液体石蜡均为惰性介质。)

①发生器用冰水冷却的原因是 ;
液体石蜡鼓泡瓶的作用是 ;
双通玻璃管的作用是 ;
浓硫酸的作用是 。
②从反应后的混合物中分离出产品的实验方法是 (填写操作名称)。
为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.减压40℃以下烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种。请利用下列试剂,设计实验方案,对制得的氨基甲酸铵中的杂质进行成分探究。
限选试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、稀盐酸。
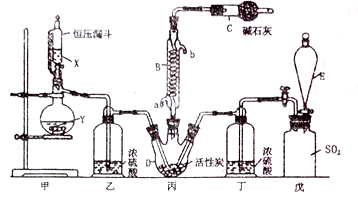
已知磺酰氯(SO2Cl2)是一种有机氯化物,也是锂电池正极活性物质,SO2Cl2是一种无色液体,熔点—54.1 ℃,沸点69.1 ℃,极易水解,遇潮湿空气会产生白雾。磺酰氯(SO2Cl2)的制备方法及装置图如下:SO2(g)+Cl2(g) SO2C12(g)
SO2C12(g)  H<0,
H<0,
(1)化合物SO2Cl2中S元素的化合价是 。
(2)仪器D的名称是 ,仪器C的作用除了吸收氯气和二氧化硫,还具有 作用。
(3)戊是贮气装置,则E中的溶液是 ;若缺少装置乙和丁,则产物变质,发生反应的化学方程式是
(4)反应结束后,将丙中混合物分离开的实验操作是 。
(5)有关该实验叙述正确的是
a、X、Y最好的席间组合是铜片和浓硫酸
b、活性炭的作用是作催化剂
c、冷凝管B也可以用作蒸馏
(6)GET公司开发的Li-SO2Cl2军用电池,其示意图如图所示,已知电池反应为: ,则电池工作时,正极的电极反应式为是
,则电池工作时,正极的电极反应式为是

现有铁、碳两种元素组成的合金,某实验小组为了研究该合金的性质并测定该合金中碳的质量分数,设计了如下实验方案和实验装置
I.探究该合金的某些性质:
(1)取a g合金粉末放人蒸馏烧瓶,并加入足量浓H2SO4,A、B中均无明显现象,原因是________________;
(2)点燃酒精灯一段时间后,A中剧烈反应,请写出此时合金中成分铁的化学反应方程式________________;
(3)反应一段时间后,将C中所吸收的气体通入以下溶液中,判断能否产生沉淀,若不能则写“否”,若能则写出相应的沉淀成分:氯水和氯化钡溶液__________,氨水和氯化钡溶液___________;
II.测定样品中碳的质量分数:
(4)装置F的作用________________________________;
(5)若将SO2气体通入含有n molNa2S的溶液中,溶液中出现黄色浑浊,试分析该溶液最多能吸收SO2气体_____________mol。
某同学查阅资料后设计了一条1-丁醇的合成路线:
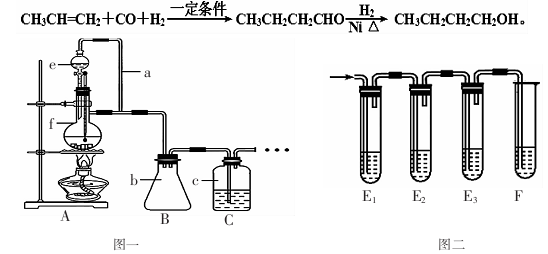
(1)利用图一装置可制备CO、丙烯等原料气体。①装置中e的名称是 ;
②a的作用 ;
(2)实验室常用浓硫酸与甲酸作用来制备CO。写出对应的化学方程式: 。
(3)制CO时,伴随的副产物还有少量S02、C02气体,某同学设计用图二装置进行检验。
①E1的作用是: ;E3的作用是: ;
②判断产物中有CO2的现象是
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是
| A.高温、常压、催化剂 | B.适当的温度、常压、催化剂 |
| C.低温、高压、催化剂 | D.适当的温度、高压、催化剂 |
(5)正丁醛经催化加氢得到含少量正丁醛的1一丁醇粗品,为提纯1-丁醇,该小组查阅文献得知:①R-CHO+NaHS03(饱和)→RCH(OH)S03Na ↓;②沸点:乙醚34℃,1-丁醇118℃。并设计出如下提纯路线:
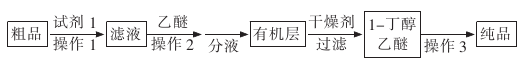
试剂1为 ,操作2为 ,操作3为
(一)如图所示,甲、乙是电化学实验装置,请回答下列问题:

若甲、乙两个烧杯中均盛放饱和NaCl溶液。
①甲中石墨棒上的电极反应式是_________________________________
②乙中总反应的离子方程式为___________________________________
③若乙中含有0.10 mol·L-1NaCl溶液400mL,当阳极产生的气体为560mL(标准状况下)时,溶液的pH=_____________(假设溶液体积变化忽略不计),转移电子的个数为____________
(二)肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景。其工作原理如上图所示,回答下列问题:
①该燃料电池中正极通入的物质是__________;
负极发生的反应式为:__________________________
②电池工作时,OH- 移向极________(“a”或“b”)
③当电池放电转移5mol电子时,至少消耗燃料肼________g
(三)全钒液流电池的结构如图所示,其电解液中含有钒的不同价态的离子、H+和SO42﹣.电池放电时,负极的电极反应为:V2+﹣e﹣=V3+.
①电池放电时的总反应方程式为___________________________
充电时,电极M应接电源的_________ 极
②若电池初始时左、右两槽内均以VOSO4和H2SO4的混合液为电解液,使用前 需先充电激活,充电过程阴极区的反应分两步完成:第一步VO2+转化为V3+;第二步V3+转化为V2+.则第一步反应过程中阴极区溶液n(H+)__________(填“增大”、“不变”或“减小”) ,阳极的电极反应式为_________________________
化学是一门以实验为基础的学科。
(1)下列实验操作的描述中,正确的是________(填序号)
①为使稀硫酸和锌制取氢气的反应速率加快,可向稀硫酸中加入用铜丝网包裹的锌粒
②粗盐提纯时,为了加快过滤速率,可用玻璃棒搅拌漏斗中的液体
③配制一定物质的量浓度的溶液时,容量瓶洗涤后不用进行干燥
④蒸馏操作中,温度计水银球部位要插入液面下且不接触蒸馏烧瓶壁
⑤可以在试管中加热氯化铵固体制备少量氨气
⑥盛放石灰水的试剂瓶内壁常有一层白色固体物质,可用稀硫酸清洗除去
(2)下列叙述中正确的是 (填序号).
| A.分液漏斗、滴定管和容量瓶使用前必须检查是否漏水 |
| B.将碘水倒入分液漏斗,再加适量乙醇,充分振荡、静置,可从碘水中萃取碘 |
| C.洁净的铁钉在食盐水中浸泡一段时间,铁钉上有气泡,说明铁发生了析氢腐蚀 |
| D.铁丝在氯气中剧烈燃烧,火星四射,生成黑色固体 |
E.酸碱中和滴定实验中,锥形瓶用蒸馏水洗净后直接使用,而滴定管用蒸馏水洗净后,必须润洗后使用
(3)用铜片与稀硝酸反应制取NO气体,如图装置中适合的是 (填图甲或图乙);装置B中的试剂最好是 ,该装置的作用是

有一混合物的水溶液,只可能含以下离子中的若干种:K+ 、Al3+ 、Fe3+ 、Mg2+ 、Ba2+ 、 NH4+、Cl- 、CO32-、SO42 -,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后得白色沉淀,沉淀经足量盐酸洗涤干燥后质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是___________,不能确定是否存在的离子是_____________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号______,浓度__________________;
离子符号______,浓度__________________;
(3)试确定K+ 是否存在________(填“是”或“否”),判断的理由是__________。
工业上常利用含硫废水生产Na2S2O3·5H2O,实验室可用如下装置(略去部分夹持仪器)模拟生产过程。

烧瓶C中发生反应如下:
Na2S(aq)+H2O(l)+SO2(g)=Na2SO3(aq)+H2S(aq)(Ⅰ)
2H2S(aq)+SO2(g)=3S(s)+2H2O(l) (Ⅱ)
S(s)+Na2SO3(aq) Na2S2O3(aq) (Ⅲ)
Na2S2O3(aq) (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若 ,则整个装置气密性良好。装置D的作用 。装置E中为 溶液。
(2)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S与Na2SO3的物质的量之比为 。
(3)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择 。
A.蒸馏水 B.饱和Na2SO3溶液
C.饱和NaHSO3溶液 D.饱和NaHCO3溶液
实验中,为使SO2缓慢进入烧瓶C,采用的操作是 。已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是 。
反应后期可用酒精灯适当加热烧瓶A,实验室用酒精灯加热时必须使用石棉网的仪器还有 。
A.烧杯 B.蒸发皿 C.试管 D.锥形瓶
(4)反应终止后,烧瓶C中的溶液经蒸发浓缩、冷却结晶即可析出Na2S2O3·5H2O,其中可能含有Na2SO3、Na2SO4等杂质。利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作、现象和结论: 。
已知Na2S2O3·5H2O遇酸易分解:S2O32—+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液
为验证卤素单质氧化性的相对强弱,某小组同学用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是 。
(2)验证氯气的氧化性强于碘的实验现象是 。
(3)B中溶液发生反应的离子方程式是 。
(4)氯、溴、碘单质的氧化性逐渐减弱的原因:从原子结构分析,同主族元素从上到下 ,得电子能力逐渐减弱。
(5)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是___________ ___。
实验室以苯、乙醛为原料,AlCl3为催化剂制备1,1–二苯乙烷,其反应原理为:

已知:AlCl3固体遇水会发生较强烈水解。
I.制取装置如右图所示。
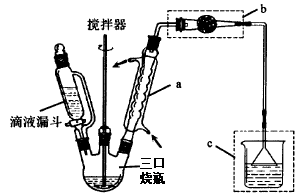
(1)该反应需控制反应温度为20℃。控制20℃的方法是 ;该反应不高于20℃的可能原因是: 。
(2)仪器a的作用是 ;装置c的作用是吸收HCl,写出产生HCl的化学方程式 ;装置b的作用是 。
Ⅱ.实验结束后,将三口烧瓶中的混合物倒入冷稀盐酸中,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,洗涤后加入少量无水硫酸镁固体,过滤、蒸馏,得到1,1–二苯乙烷。
(1)分液漏斗中,产品在 (填“上”或“下”)层;洗涤操作中,第二次水洗的目的是 ;无水硫酸镁也可用物质 代替。
(2)蒸馏提纯时,下列装置中会导致收集到的产品中混有低沸点杂质的装置是 (选填编号)。

(3)三口烧瓶中加入120mL苯(密度0.88g/mL)、19g A1C13和3.7g乙醛,20℃时充分反应,制得纯净的1,1–二苯乙烷7.8g。该实验的产率约为 。