实验题:某学生为了验证氢气还原氧化铜的产物,设计了下图所示的实验装置。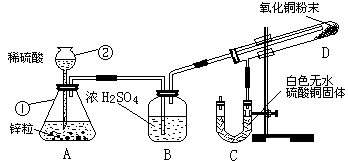
⑴ 写出编号仪器的名称: ①______________
⑵ 写出A中反应的离子方程式_____________________________
⑶ 浓H2SO4的作用是_____________________
⑷ 本实验需要加热的装置为____________(填字母编号)。
⑸ 写出装置C、D中可观察到的现象:C______ ___,D______ ___
⑹ D中反应每生成1mol水分子,转移的电子数为____________个。
(9分)某非金属单质A经如下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①A、D的化学式分别为:A D
②工业生产中大量排放的B气体被雨水吸收后形成 而污染环境。
③写出B→C反应的化学方程式:
(2)若A在常温下为气体,C是红棕色气体。
①A的电子式为 ,C的化学式为
②写出C→D反应的化学方程式:
硫酸工业尾气中二氧化硫的含量超过0.05%(体积分数)时需经处理后才能排放。某校化学兴趣小组欲测定某硫酸工厂排放尾气中二氧化硫的含量,分别采用以下方案:
[甲方案]:如右图所示,图中气体流量计B用于准确测量通过的尾气体积。将尾气通入一定体积已知浓度的碘水中测定SO2的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。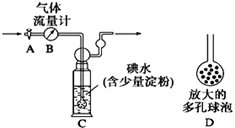
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验的准确度,其理由是___________________________________。
(2)洗气瓶C中溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量_________(填“偏高”、“偏低”或“无影响”)。
[乙方案]:实验步骤如下面流程图所示: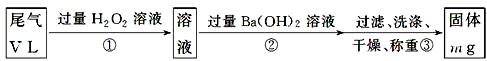
(3)步骤①中过量H2O2的作用是
(4)写出步骤②中反应的化学方程式______________________________________
(5)步骤②中Ba(OH)2是否足量的判断方法是_______________________________
___________________________________________________________________。
(6)通过的尾气体积为V L(已换算成标准状况)时,该尾气中二氧化硫的含量(体积分数)为_____________________________(用含有V、m的代数式表示)。
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是可控制气体流向,用于鼓入空气的双连打气球。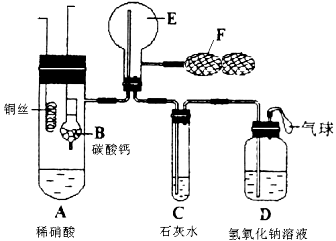
(1) 实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为
__________________________________。
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为______________________。
(3)装置E中开始时出现浅红棕色,原因是__________________________;用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是__________________________________。
(4)一段时间后,C中白色沉淀溶解,其原因是_________________________________;
。(用化学方程式表示)
(5)装置D的作用是_____________________________________________________。
一水硫酸四氨合铜(Ⅱ)(化学式为[Cu(NH3)4]SO4·H2O)是一种重要的染料及农药中间体。某学习小组以孔雀石(主要成分为Cu2(OH)2CO3,含少量Fe2O3和SiO2杂质)为原料制备该物质的流程如下: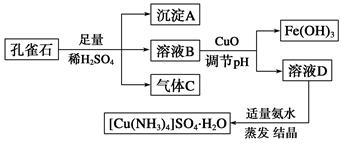
请回答:
(1)沉淀A的晶体中最小环上的原子个数为________,气体C分子中σ键和π键的个数比为________。
(2)溶液D的溶质阴离子的空间构型为__________,其中心原子的杂化轨道类型为________。
(3)MgO的熔点高于CuO的原因为______________________________________。
(4)画出一水硫酸四氨合铜(Ⅱ)中配离子([Cu(NH3)4]2+)的配位键________________。
(5)一种铜金合金晶体具有面心立方最密堆积的结构。在晶胞中,Au原子位于顶点,Cu原子位于面心,则该合金中Au原子与Cu原子个数之比为 ,若该晶胞的边长为a pm,则合金的密度为 g·cm-3(只要求列算式,不必计算出数值,阿伏伽德罗常数为NA)。
某无色透明溶液可能含有下列离子K+、Al3+、Fe3+、Ba2+、NO3—、SO42—、HCO3—、Cl-等,取该溶液进行如下实验:
①用蓝色石蕊试纸检测该溶液,试纸显红色;
②取溶液少许,加入铜片和稀硫酸共热,产生无色气体,该气体遇到空气立即变为红棕色;
③取溶液少许,加入氨水有白色沉淀生成,继续加入过量氨水,沉淀不消失;
④取溶液少许,滴入氯化钡溶液产生白色沉淀;
⑤取实验④后的澄清溶液,滴入硝酸银溶液产生白色沉淀,再加入过量的稀硝酸,沉淀不消失。
请回答下列问题:
(1)在实验①中,下图所示的操作中正确的是____ ____(填代号)。
(2)根据上述实验判断原溶液中肯定存在的离子是___ _____,
肯定不存在的离子是___ _____。
(3)写出②实验中产生无色气体的离子方程式:
________________________________________________________________________。
(4)写出③实验中的有关离子方程式:
________________________________________________________________________。
(I) 电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。用FeCl3溶液做腐蚀液与Cu反应生成CuCl2和FeCl2。
(1) 写出该反应的化学方程式 。
(2) 检验溶液中Fe3+存在的试剂是 ,证明Fe3+存在的现象是 。
(Ⅱ) 印刷电路的废腐蚀液含有大量CuCl2、FeCl2、FeCl3,任意排放会造成环境污染及资源的浪费。通过下列流程可从该废液中回收铜,并将铁的化合物全部转化为FeCl3溶液,作为腐蚀液原料循环使用。
⑴ 步骤①中发生反应的离子方程式 。
(2) 步骤②需加入的试剂A是 (填化学式)。
(3) 步骤③通入的气体B是 (填化学式),写出该反应的化学方程式 。
(4) 为测定滤渣中铜的质量分数,取50g的滤渣与足量的试剂A反应,得到5.6L气体(标准状况下),试计算滤渣中铜的质量分数。
(1)控制变量是科学研究中的重要研究方法,其基本思路是,在实验研究中人为只改变一个因素(调节变量),其他因素保持相同,观察测定因调节变量改变而改变的因素(因变量),从而分析得到研究结论。中学化学中应用控制变量的方法研究问题的例子很多。请分析或设计:
①在研究浓度对化学反应速率的影响时,教材安排了利用Na2S2O3与H2SO4反应的一组对照实验(Na2S2O3+H2SO4===Na2SO4+S↓+SO2↑+H2O)
| 烧杯 编号 |
加3% Na2S2O3溶液体积(mL) |
加H2O体积(mL) |
加(体积之比为1∶2)H2SO4溶液体积(mL) |
所需时间(s) |
| 1 |
5 |
5 |
2 |
|
| 2 |
7 |
3 |
2 |
|
| 3 |
10 |
0 |
2 |
|
在三个烧杯(底部有黑色“十”字标记)内分别加入表中所示体积的三种液体,搅拌并开始计时,到出现浑浊使烧杯底部“十”字看不见时停止计时。比较所需时间,得出浓度对化学反应速率影响的结论。实验中,温度和反应体系中硫酸浓度是保持相同的因素,调节变量是____________________,因变量是______________。
②运用控制变量原理设计实验,利用纯碱溶液探究温度对盐的水解的影响,简述实验方法:________________________________________________________________________。
(2)373 K时,H2PO3-与OH-发生如下反应:
H2PO3-+OH-HPO32-+H2O
反应结果如表所示:
| H2PO3-起始浓度(mol/L) |
0.10 |
0.50 |
0.50 |
| OH-起始浓度(mol/L) |
1.00 |
1.00 |
4.00 |
| 反应速率[mol/(L·s)] |
3.2×10-5 |
1.60×10-4 |
2.56×10-3 |
如果用v=kcm(H2PO3-)·cn(OH-)表示反应速率(k为与浓度无关的常数)
①k=________,m=________,n=________。
②若c(H2PO3-)的起始浓度为0.20 mol/L,c(OH-)的起始浓度为1.50 mol/L,则反应速率v=________。
某研究性学习小组将一定浓度的Na2CO3 溶液滴入CuSO4溶液中得到沉淀。
甲同学认为两者反应只有CuCO3一种沉淀生成;
乙同学认为这两者相互促进水解反应,生成Cu(OH) 2一种沉淀;
丙同学认为生成CuCO3和Cu(OH) 2两种沉淀。
(1)各装置连接顺序为 → → 。
(2)若甲同学的结论正确,实验现象为 。
II.若CuCO3和Cu(OH)2两者都有,可通过下列所示装置的连接,进行定量分析来测定其组成。
(1)仪器组装好后首先要进行的实验操作是 ,实验结束时要继续通入处理过的过量空气,其作用是 。
(2)若沉淀样品的质量为mg,当反应完全后,装置C质量增加了ng,则沉淀中CuCO3的质量分数为 。
III.沉淀转化在生产中也有重要应用。例如,用Na2CO3溶液可以将锅炉水垢中的CaSO4转化为较疏松瓶易清除的CaCO3,该沉淀转化达到平衡时,其平衡常数K=___________(写数值)。[已知Ksp(CaSO4)=9.1×10—6,Ksp(CaCO3)=2.8×10—9]
IV.蓝铜矿的主要成分为2CuCO3·Cu(OH)2,当它与焦炭一起加热时,可以生成铜、二氧化碳和水,写出该反应的化学方程式_____________________________________________
盐酸、硫酸和硝酸都是重要的化工原料,也是化学实验室里必备的重要试剂。请回答下列问题:
(1)常温下,可用铁、铝制的容器盛放浓硫酸,说明浓硫酸具有 性。用玻璃棒蘸取浓硫酸滴在纸上,纸逐渐变黑,说明浓硫酸具有 性。
(2)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是 (填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2 ② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu CuO
CuO Cu(NO3)2
Cu(NO3)2
(3)①在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,测得产生的气体在标准状况下的体积可能是 。
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
②若使上述反应①中剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_______________________________________________________________________。
(4)若将12.8g铜跟一定质量的浓HNO3反应,铜消耗完时,共产生气体5.6L(标准状况),则所耗HNO3的物质的量 mol。
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为 。
绿矾( )是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:
)是治疗缺铁性贫血药品的重要成分。下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生产纯净绿矾的一种方法:

已知:室温下饱和 溶液的
溶液的 约为3.9,SnS沉淀完全时溶液的
约为3.9,SnS沉淀完全时溶液的 为1.6;
为1.6; 开始沉淀时溶液的
开始沉淀时溶液的 为3.0,沉淀完全时的
为3.0,沉淀完全时的 为5.5。
为5.5。
(1)检验制得的绿矾晶体中是否含有 的实验操作是
的实验操作是
(2)操作II中,通入硫化氢至饱和的目的是 ;在溶液中用硫酸酸化至 =2的目的是 。
=2的目的是 。
(3)操作IV的顺序依次为: 、冷却结晶、 。
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;② 。
(5)测定绿矾产品中 含量的方法是:a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
含量的方法是:a.称取2.8500g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL。
①滴定时发生反应的离子方程式为: 。
②计算上述样品中 的质量分数为 (用小数表示,保留三位小数)。
的质量分数为 (用小数表示,保留三位小数)。
(每空2分,共16分)某研究性学习小组为合成1-丁醇,查阅资料得知一条合成路线:
CH3CH===CH2+CO+H2 CH3CH2CH2CHO
CH3CH2CH2CHO CH3CH2CH2CH2OH:
CH3CH2CH2CH2OH:
CO的制备原理:HCOOH CO↑+H2O,并设计出原料气的制备装置(如图)。
CO↑+H2O,并设计出原料气的制备装置(如图)。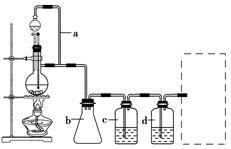
请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备丙烯。写出化学方程式: ____________________________________________________________________________。
(2)若用以上装置制备H2,在虚线框内画出收集干燥H2的装置图。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________(填序号)
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是________。
a.低温、高压、催化剂 b.适当的温度、高压、催化剂
c.常温、常压、催化剂 d.适当的温度、常压、催化剂
(5)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R—CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓ ;②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线: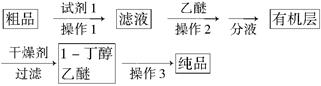
试剂1为________,操作1为________,操作2为________,操作3为________。
现有一定量含有Na2O杂质的Na2O2试样,用图K2-6-2所示的实验装置测定Na2O2试样的纯度。(可供选用的试剂只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)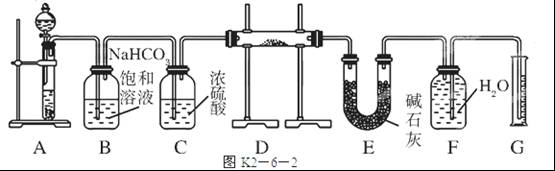 回答下列问题:
回答下列问题:
(1)装置A中液体试剂选用____________,理由是________________________________。
(2)装置B的作用是___________________________________________,装置E中碱石灰的作用是______________________________________________________________________。
(3)装置D中发生反应的化学方程式是_________________________________________。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_________________。
实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。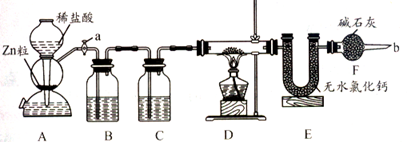
(1)如何检查装置A的气密性_________________________________________
(2)为了安全,在点燃D处的酒精灯之前,在b处必须_____________________。
(3) 装置B 的作用是_______________ ,装置C中装的液体是________________,所起的作用是_______________________。
(4)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双管中发生的化学反应方程式是________________________________________。
(5)若FeO和Fe2O3固体混合物的质量为31. 2g,反应完全后,U型管的质量增加9.9g则混合物中Fe2O3的质量为______________。
(6)U型管E右边连接干燥管F的目的是______________________,若无干燥管F,测得Fe2O3的质量将_____________(填“偏大”、“偏小”或“无影响”)
实验探究和推理都是科学研究的基本方法,请你对以下实验进行探究和推理
Ⅰ、有一瓶澄清的溶液,其中可能含有H+、NH4+、K+、Na+、Mg2+、Ba2+、Fe3+、SO42―、CO32―、Cl―和I―。取该溶液进行了以下实验:
(1)用pH试纸检验,表明溶液呈强酸性;
(2)取部分溶液,加入CCl4及数滴氯水,经振荡后CCl4层呈紫红色;
(3)另取部分溶液,加入稀NaOH 溶液使其变为碱性,溶液中无沉淀生成;
(4)取部分上述碱性溶液,加Na2CO3溶液有白色沉淀生成;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使润湿的红色石蕊试纸变蓝;
根据上述实验事实,你可知道该溶液中肯定含有的离子是① ;肯定不存在的离子是② ;还不能确定是否存在的离子是③ 。
Ⅱ、兴趣小组通过实验探究溶解铜的方法和本质。
(1)在热水浴中进行3个实验,部分实验报告如下表所示。
| 序号 |
实验操作 |
实验现象 |
| I |
稀硫酸中加入铜片 |
无明显变化 |
| II |
硝酸钠溶液中加入铜片 |
无明显变化 |
| III |
稀硫酸中加入硝酸钠溶液 |
无明显变化 |
| 再加入铜片 |
有无色气泡;溶液变蓝 |
① 实验I、II的目的是 。
② 实验III中反应的本质是(用离子方程式表示) 。