在一定温度下向饱和Na2SO4溶液中加入ag无水硫酸钠粉末,搅拌,静置后析出bgNa2SO4·10H2O晶体,(b-a)g是 ( )
| A.原饱和溶液失去的水的质量 |
| B.原饱和溶液中减少的硫酸钠的质量 |
| C.原饱和溶液中失去的水和硫酸钠的总质量 |
| D.析出的晶体含有的硫酸钠的质量 |
已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2的氧化性依次减弱。下列反应在水溶液中不可能发生的是( )
| A.3Cl2+6FeI2="==2FeCl3+4FeI3" | B.Cl2+FeI2===FeCl+I2 |
| C.Co2O2+6HCl==2CoCl2+Cl2↑+3H2O | D.2Fe2++2I-===2Fe2++I2 |
用4种溶液进行实验,下表中“操作及现象”与“ 溶液”对应关系错误的是 ( )
溶液”对应关系错误的是 ( )
| 选项 |
操作及现象 |
溶液 |
| A |
能入CO2,溶液变浑浊。再升温至65℃以上,溶液变澄清 |
C6H5ONa溶液 |
| B |
通入CO2,溶液变浑浊。继续通CO2至过量,浑浊褪去 |
NaSiO3溶液 |
| C |
通入CO2,溶液变浑浊,再加入品红溶液,红色消失。 |
Ca(ClO)2溶液 |
| D |
通入CO2,溶液变浑浊,继续通CO2至过量,浑浊消失,再加放足量NaOH溶液,又变浑浊 |
Ca(OH)2溶液 |
现有2mol/L的盐酸和硫酸溶液各100mL,分别加 入等质量的铁粉,反应结束时,所生成的气体质量比为2:3,则往酸中加入的铁粉的质量为 ( )
入等质量的铁粉,反应结束时,所生成的气体质量比为2:3,则往酸中加入的铁粉的质量为 ( )
| A.8.4g | B.5.6g | C.2.8g | D.16.8g |
下列每组中的两种物质相到反应时,无论谁过量,都可以用同一个离子方程式表示的是 ( )
| A.偏铝酸钠溶液和盐酸 | B.磷酸二氢钠溶 液和澄清和石灰水 液和澄清和石灰水 |
| C.苯酚钠溶液和二氧化碳 | D.硝酸银溶液和氨水 |
金刚烷的结构如图,它可看作是由四个等同的六元环组成的空间构型。请根据中学学过的异构现象判断由氯原子 取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物的种类( )
取代金刚烷亚甲基(-CH2-)中氢原子所形的二氯取代物的种类( )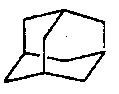
| A.4种 | B.3种 |
| C.2种 | D.6种 |
已知酸性大小:羧酸>碳酸>酚.下列含溴化合物中的溴原子,在适当条件下都能被羟其(-OH)取代(均可称之为水解反应),所得产物能跟NaHCO3溶液反应的是( )
有机物分子中原子(或原子团)间的相互影响会导致它们化学性质的改变。下列叙述能说明上述观点的是( )
| A.苯酚能与NaOH溶液反应,而乙醇不能 |
| B.四酸可发生银镜反应,而乙酸不能 |
| C.乙烯可发生加成反应,而乙烷不能 |
| D.等物质的量的甘油和乙醇分别与足量的金属钠反应,甘油产生的H2多 |
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC(以上体积均为相同条件下测得),已知VA=3VC,且VA=VB+VC,则在B的反应生成物中,该金属元素的化合价为( )
A.+1 B.+2 C.+3 D.+4
如图所示,在火棉胶袋(半透膜)内注入淀粉和食盐溶液,用线系紧密封使玻璃管内的液面刚好高出烧杯内蒸馏水的液面,过一段时间后,用碘酒和硝酸银溶液分别检验蒸馏水,整个实验过程中,所观察到的现象是( )
| A.细玻璃管内液面下降 | B.细玻璃管内液面不变 |
| C.蒸馏水遇碘酒变蓝 | D.蒸馏水遇AgON3溶液有白色沉淀生成 |
关于化学键的下列叙述中,正确的是 ( )
| A.离子化合物中只含离子键 | B.共价化合物中只含非金属元素 |
| C.离子化合物中可能含共价键 | D.离子化合物中一定含有金属离子 |
有机物种类繁多的原因的主要原因 ( )
| A.有机物分子结构十分复杂 |
| B.自然界中存在着多种形式的、大量的有机物 |
| C.烃类分子中的碳原子通过离子键和共价键跟其他原子结合 |
| D.碳原子有四个共价键,且碳原子间也可以成键,而且有同分异构现象 |
等物质的量的下列烃完全燃烧,消耗氧气最多的是 ( )
| A.CH4 | B.C5H12 | C.C3H8 | D.C2H6 |
下列有机物中,一氯取代物有2种的是 ( )
①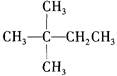 ②
②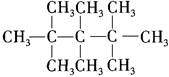
③ 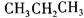 ④
④ 
| A.全部 | B.①③ | C.②④ | D.②③ |
甲烷是天然气的主要成分,是一种高效、低耗、污染小的清洁能源。下列有关甲烷的说法正确的是 ( )
| A.甲烷燃烧,火焰明亮,冒黑烟 |
| B.物质的量1∶1的甲烷与氯气发生取代反应时,生成物只有CH3Cl和HCl |
| C.0.5mol甲烷完全燃烧时消耗氧气最多为1mol |
| D.甲烷分子中的所有原子均满足最外层8电子结构 |