下列反应的离子方程式正确的是( )
| A.氯化亚铁溶液跟氯气反应:2Fe2++ Cl2 =2Fe3+ +2Cl- |
| B.向碳酸钠溶液中滴加少量的稀硝酸:CO32- +2H+=CO2↑+H2O |
| C.AgNO3溶液中加入过量氨水:Ag++ NH3·H2O ="AgOH" +NH4+ |
| D.硫化钾晶体溶于水:S2- +2H2O= 2OH - +H2S |
下列各组数据关系中,前者比后者大的是( )
| A.常温常压下,pH =10的KOH溶液和pH=" 10" 的CH3COOK溶液中,由水电离的OH -浓度 |
| B.纯水在100 0C和20℃时pH |
| C.25℃,浓度相同的硅酸钠溶液与碳酸钠溶液的pH |
| D.l0mL mol·L-1醋酸溶液稀释10倍,稀释前后的H+数目 |
在给定条件下,下列加点的物质在化学反应中能被“全消耗”的是( )
| A.用50mL 12mol.L-1盐酸与过量的二氧化锰共热制取氯气 |
| B.向100mL 3mol.L-1的硝酸中加入5. 6g铁粉 |
| C.标准状况下,将1g铝片投入20mL 18. 4mol·L-1的硫酸中 |
| D.在5 ×107 Pa、500℃和铁触媒催化的条件下,用2mol氮气和3mol氢气合成氨 |
在一种酸性溶液中存在NO3-、I-、CI-、Fe3+中一种或几种离子,向该溶液中加入溴水,溴单质被还原,由此可推断溶液中( )
①一定含有I-,不能确定是否有CI- ②一定含有NO3-
③不含有Fe3+ ④一定含有I-、NO3-和CI-
| A.① | B.②③ | C.④ | D.①③ |
高温及一定催化剂作用下,某反应达平衡,平衡常数K=  .恒容时,温度升高,H2浓度减小,下列说法正确的是( )
.恒容时,温度升高,H2浓度减小,下列说法正确的是( )
| A.将容器体积变为原来2倍,CO的平衡浓度变为原来的2倍 |
| B.恒温恒容下,增大压强,H2浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为CO2 +H2 CO+H2O ;△H>O CO+H2O ;△H>O |
下列事实得出的结论正确的是( )
| A.用一束强光照射经过煮沸的三氯化铁溶液有光的通路,说明已生成氢氧化铁胶体 |
| B.某雨水样品放置一段时间,pH由5.6变为4.3,说明水中溶解了更多的CO2 |
| C.常温下铜可溶于浓硝酸,铁不溶于浓硝酸,说明铜比铁更活泼 |
| D.二氧化硫溶于水所得的溶液可导电,说明二氧化硫是电解质 |
将0.03molCl2缓缓通人含0.02mol H2SO3和0.02mol HBr的混合溶液中,在此过程溶液的c(H+)与C12用量的关系示意图是(溶液的体积视为不变)( )
用铜锌合金制成假金元宝骗人的事件屡有发生。下列不易区别其真伪的方法是( )
| A.观察外观 | B.放入硝酸中 | C.放入盐酸中 | D.测定密度 |
浓硫酸和浓硝酸是实验室常用的酸,下列关于它们的说法错误的是( )
| A.浓硫酸和浓硝酸都不能用来直接跟锌粒反应制氢气 |
| B.浓硫酸和浓硝酸都能与金属铜反应 |
| C.浓硫酸和浓硝酸加水稀释后都能与金属铜反应 |
| D.浓硫酸和浓硝酸在常温下都能用金属铝或铁制容器盛放 |
在下列反应中,硫元素表现出氧化性的是( )
| A.稀硫酸与锌反应 | B.二氧化硫与氧气反应 |
| C.浓硫酸与铜反应 | D.三氧化硫与水反应 |
下列溶液可用无色试剂瓶装的是( )
| A.HNO3 | B.AgNO3 | C.氯水 | D.H2SO4 |
从降低成本和减少环境污染的角度考虑,制取硝酸铜最好的方法是( )
| A.铜和浓硝酸反应 | B.铜和稀硝酸反应 |
| C.氧化铜和硝酸反应 | D.氯化铜和硝酸银反应 |
下列反应中硫酸既表现出了强氧化性又表现了酸性的是( )
| A.氧化铜与硫酸反应 | B.氢氧化铝与硫酸反应 |
| C.木炭粉与浓硫酸反应 | D.铜与浓硫酸反应 |
氨水的碱性较弱,其原因是( )
| A.它能使酚酞试液变红色 |
| B.氨水极易挥发出氨 |
| C.氨与水结合生成的一水合氨(NH3·H2O)只有小部分电离成NH4+和OH— |
| D.溶于水的氨大部分以NH3分子形式存在 |
已知气体的摩尔质量越小,扩散速度越快。下图所示为气体扩散速度的实验,两种气体扩散相遇时形成白色烟环。下列关于甲、乙的判断正确的是( )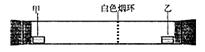
| A.甲是浓氨水,乙是浓硫酸 |
| B.甲是浓盐酸,乙是浓氨水 |
| C.甲是浓氨水,乙是浓盐酸 |
| D.甲是浓硝酸,乙是浓氨水 |