下列图示与对应的叙述相符的是



图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
| A.图Ⅰ表示t℃时冰醋酸在稀释过程中溶液导电性的变化 |
| B.图Ⅱ表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C.图Ⅲ表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大 3C(g)+D(s)的影响,乙的压强比甲的大 |
| D.据图Ⅳ,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右 |
一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时反应达到平衡,此时容器中c(NH3)=0.1mol·L-1。下列有关判断错误的是
| A.反应达平衡时N2的转化率为10% |
| B.反应进行到10 s末时,H2的平均反应速率是0.03 mol·(L·s)-1 |
| C.该反应达到平衡时,N2的平衡浓度为0.45 mol/L |
| D.该反应达到平衡时的压强是起始时压强的0.95倍 |
下列说法中正确的是
| A.将纯水加热至较高温度,Kw变大、pH变小、呈酸性 |
| B.保存FeSO4溶液时,应在其中加入稀HNO3以抑制Fe2+水解 |
| C.AlCl3溶液蒸干、灼烧至恒重,最终剩余固体是AlCl3 |
D.向0.1 mol·L-1氨水中加入少量水,pH减小, 增大 增大 |
下列离子方程式书写正确的是
| A.鸡蛋壳和醋酸溶液的反应:CaCO3+2H+=Ca2++H2O+CO2↑ |
B.明矾水解的离子方程式:Al3++3H2O Al(OH)3↓+3H+ Al(OH)3↓+3H+ |
| C.向稀硫酸加入少量Ba(OH)2溶液:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| D.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
在下列溶液中,各组离子一定能够大量共存的是
| A.常温下,c(H+)/c(OH-)=1010的溶液:Na+、NH4+、SO42-、CH3COO- |
| B.滴入酚酞试液显红色的溶液:Na+、Ba2+、NO3-、Cl- |
| C.由水电离出的c(H+)=1×10-13mol/L的溶液:NH4+、K+、CO32-、Cl- |
| D.含有大量HCO3-的溶液:K+、Al3+、Cl-、Na+ |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.1L 1mol/L醋酸溶液中含有的离子总数为2NA |
| B.25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
| C.100mL 1mol∙L-1的Na2CO3溶液中CO32-、HCO3-和H2CO3总数为0.1NA |
| D.0.1L 3mol·L-1的FeCl3溶液中含有的Fe3+数目为0.3 NA |
如图,曲线为可逆反应A(g) +2B(g)  2C(g) 正反应为吸热反应的平衡移动关系曲线,下列说法正确的是
2C(g) 正反应为吸热反应的平衡移动关系曲线,下列说法正确的是
| A.a<b,y轴指B的质量分数 |
| B.a>b,y轴指C的质量分数 |
| C.a<b,y轴指A的转化率 |
| D.a>b,y轴指A的体积分数 |
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是 ( )
| A.反应达到平衡时,X的转化率为50% |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.增大压强使平衡向生成Z的方向移动,平衡常数增大 |
| D.改变温度可以改变此反应的平衡常数 |
可逆反应:A2(?)+B2(?) 2AB(?) ΔH=-QkJ/mol,当温度和压强改变时AB物质的量的变化如下图,下列叙述正确的是
2AB(?) ΔH=-QkJ/mol,当温度和压强改变时AB物质的量的变化如下图,下列叙述正确的是 
| A.A2、B2及AB均为气体,Q>0 |
| B.AB为气体,A2、B2至少有一种为非气体,Q>0 |
| C.AB为气体,A2、B2有一种为非气体,Q<0 |
| D.AB为固体,A2、B2有一种为非气体,Q>0 |
100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:
N2O4(g)  2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2
②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变
⑥烧瓶内气体的颜色不再加深
⑦烧瓶内气体的平均相对分子质量不再变化
⑧烧瓶内气体的密度不再变化。
| A.②③⑥⑦ | B.①④⑧ | C.只有①④ | D.只有⑦⑧ |
下列说法或表示方法中正确的是( )
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B.吸热反应发生过程中要不断从外界获得能量,放热反应一定不需要吸收外界能量 |
| C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式为: 2H2(g)+O2(g)=2H2O (l)ΔH= +285.8kJ/mol |
| D.稀溶液中:H+(aq)+OH—(aq)=H2O(l)ΔH=" —53.7kJ/mol" ,若将含0.5 molH2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于53.7kJ |
某有机物的结构简式如右图,该物质不应有的化学性质是( )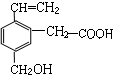
①可燃烧; ②可跟溴加成;
③可使酸性KMnO4溶液褪色;④可跟NaHCO3溶液反应;
⑤可跟NaOH溶液反应; ⑥可在碱性条件下水解
| A.①③ | B.③⑥ | C.④⑤ | D.⑥ |
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
| A.铊是易导电的银白色金属 | B.能生成+3价离子化合物 |
| C.T1(OH)3是两性氢氧化物 | D.Tl3+的氧化能力比Al3+强 |
X、Y、Z、W、R是5种短周期元素,其原子序数依次增加。X是元素周期表中原子半径最小的的元素, Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是 ( )
| A.元素Y、Z、W具有相同电子层的离子,其半径依次增大 |
| B.元素X能与元素Y形成化合物X2Y2 |
| C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY> XmR |
| D.元素W、R的最高价氧化物的水化物都是强酸 |