要配制浓度约为2mol/L NaOH溶液100mL,下列操作正确的是
| A.称取8gNaOH固体,放入100mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL |
| B.称取8gNaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀 |
| C.称取8gNaOH固体,放入100mL烧杯中,将烧杯中加满蒸馏水,同时不断搅拌至固体溶解 |
| D.用100mL量筒量取40ml 5mol/L NaOH溶液,倒入250mL烧杯中,再用同一量筒取60mL蒸馏水,不断搅拌下,慢慢倒入烧杯中 |
实验室下列物质的保存方法中,不正确的是
| A.新制的氯水保存在棕色瓶中,并放在阴凉处 |
| B.氢氧化钠溶液盛放在配有玻璃磨口塞的试剂瓶中 |
| C.少量的金属钠保存在煤油中 |
| D.硫酸亚铁溶液存放在加有少量铁粉的试剂瓶中 |
用酒精灯加热下列溶液,蒸干后灼烧,所得固体与溶质成份相同的是( )
| A.FeCl3溶液 | B.NaHCO3溶液 | C.Na2SO3溶液 | D.CH3COONa溶液 |
某学生的实验报告所列出的下列数据中合理的是
| A.用10mL量筒量取7.13mL稀盐酸 |
| B.用托盘天平称量25.20g NaCl |
| C.用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.70mL |
往溴水加入苯后,振荡,静置,溴水层颜色变浅,这是由于 ( )
| A.溴挥发出了 | B.发生了取代反应 |
| C.发生了加成反应 | D.发生了萃取 |
用pH试纸测定某无色溶液的pH值时,规
范的操作是( )。
| A.将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较 |
| B.将溶液倒在pH试纸上,跟标准比色卡比较 |
| C.用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上,跟标准比色卡比较 |
| D.在试管内放少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较 |
已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验:
(1)写出①②和③步所有反应的化学方程式:
_____________________________________;______________________________________。
_____________________________________;______________________________________。_____________________________________;______________________________________。
(2)设从③步所得固体D的质量为32 g,溶液E中只含有一种金属离子,气体F在标准状况下的体积为5.6 L,试计算取用的每份X的质量和X中FeO与CuO的质量比。
聚合硫酸铁(PPS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原成Fe2+。实验步骤如下:

(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有______________。
a.容量瓶 b.烧杯 c.烧瓶
(2)步骤Ⅱ取样分析溶液中的Fe2+、Fe3+的含量,目的是_____________________________。
a.控制溶液中Fe2+与Fe3+含量比 b.确定下一步还原所需铁的量
c.确定氧化Fe2+所需NaClO3的量 d.确保铁的氧化物酸溶完全
(3)聚合硫酸铁溶液中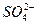 与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中
与Fe3+物质的量之比不是3∶2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中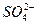 与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
与Fe3+物质的量之比。测定时所需的试剂为__________________,需要测定______________和______________的质量。(填写化合物的化学式)
a.NaOH b.FeSO4 c.BaCl2 d.NaClO3
(10分)某铝合金中含有合金元素镁、铜、硅,为了测定该合金中铝的含量,设计了如下实验,请完成有关问题:
(1)称取样品a g,称量时应该使用的主要仪器的名称是
_______________________________。
(2)将样品溶解于足量的稀盐酸,过滤。滤液中主要含有______________________________,滤渣中含有_______________________,溶解、过滤用到的玻璃仪器是__________________。
(3)滤液中加过量氢氧化钠溶液、过滤。有关的离子方程式是_______________________,____________________________________。
(4)步骤(3)的滤液中通入足量二氧化碳气体,过滤。有关的离子方程式是______________。
(5)步骤(4)过滤后的滤渣用蒸馏水洗涤数次,烘干并灼烧至恒重,冷却后称重,其质量为b g。有关的化学方程式是____________________,原样品中铝的质量分数是_________。
(6)若步骤(3)中加入氢氧化钠的量不足,则实验结果偏___________(“高”“低”或“不影响”,下同);若步骤(5)中滤渣没有洗涤,则实验结果偏___________;若滤渣灼烧不充分,则实验结果偏___________。
有人设计了如图所示实验装置,目的是做钠与水反应实验并验证:①钠的物理性质;②钠与水反应的产物是什么?
(1)当进行适当操作时还需要的仪器有_____________________________。
(2)如何进行操作?_____________________________________________。
(3)实验现象是_________________________________________________。
欲配制100 mL 1.0 mol·L-1 Na2SO4溶液,正确的方法是( )
①将14.2 g Na2SO4溶于100 mL水中 ②将32.2 g Na2SO4·10H2O溶于少量水中,再用水稀释至100 mL ③将20 mL 5.0 mol·L-1 Na2SO4溶液用水稀释至100 mL
| A.①② | B.②③ | C.①③ | D.①②③ |
有一包白色粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:
①将部分粉末加入水中,振荡有白色沉淀生成。
②向①的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生。
③取少量②的溶液,滴加稀硫酸,有白色沉淀生成。
④另取少量②的溶液,滴加AgNO3溶液,有白色沉淀生成。
请回答:
(1)根据上述实验现象,判断原白色粉末的组成成分是___________(填写名称)。
(2)写出①—④中涉及的化学方程式:
①______________________________
②_____________________________
③______________________________
④_____________________________
配制250 mL 0.10 mol·L―1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大的是( )
| A.转移溶液后未洗涤烧杯和玻璃棒就直接定容 |
| B.在容量瓶中进行定容时仰视刻度线 |
| C.在容量瓶中进行定容时俯视刻度线 |
| D.定容后把容量瓶倒置摇匀,发现液面低于刻度,再补充几滴水至刻度线 |
粗食盐中除含有钙离子、镁离子、硫酸根离子等可溶性杂质外,还含有泥沙等不溶性杂质。为了除去杂质在实验室中可将粗盐溶于水然后进行下列操作:(1)过滤;(2)加入过量的氢氧化钠溶液;(3)加入适量的盐酸;(4)加过量Na2CO3溶液;(5)加过量的BaCl2溶液。通过教材中“粗盐的提纯”及你做过的该实验回答下列问题。
(1)以上操作的正确顺序是( )
| A.(5)(4)(2)(1)(3) | B.(1)(2)(3)(4)(5) |
| C.(5)(4)(3)(2)(1) | D.(1)(5)(4)(2)(3) |
(2)实验室进行NaCl溶液蒸发时,一般有以下操作过程:①放置酒精灯;②固定铁圈位置;③放上蒸发皿(蒸发皿中盛有NaCl溶液);④加热搅拌;⑤停止加热。其正确的操作顺序为___________。
(3)如何运用最简的方法检验溶液中有无SO42―离子?______________________________。
如果有,应该如何除去SO42―离子?
___________________________________________。
(4)在粗盐经过溶解等步骤后,在过滤前的溶液中滴加饱和Na2CO3溶液,直至不再产生沉淀为止。这步操作的目的是
______________________________________________。
(5)将经过操作(4)后的溶液过滤。请问这一操作能除掉哪些杂质?
(6)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:________________________________________。过滤时:________________________________________。蒸发时:________________________________________。