Ⅰ.羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫的危害,其分子结构和CO2相似。
(1)羰基硫(COS)的电子式为:______________。
(2)羰基硫(COS)用氢氧化钠溶液处理及利用的过程如下:
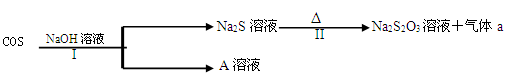
已知A是一种正盐,则A的化学式为______________;若气体a为单质,
反应II的离子方程式为________________________________________________。
Ⅱ.海水中含有丰富的镁资源。锂(Li)与镁元素性质相似。
(1)物质的量为0.10 mol的锂在只含有N2和O2混合气体的容器中燃烧,反应后容器内固体物质的质量m克,m的取值范围是 ;
(2)锂电池是新一代高能电池,目前已研究成功多种锂电池。某离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为LiCoO2+C6 CoO2+LiC6,则放电时电池的正极反应为 。
CoO2+LiC6,则放电时电池的正极反应为 。
(3)为了回收废旧锂离子电池的正极材料试样(主要含有LiCoO2及少量Al、Fe等)可通过下列实验方法回收钴、锂。
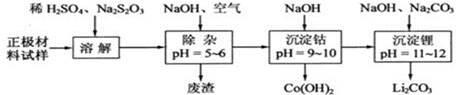
①在上述溶解过程中,S2O32-被氧化成SO42-,LiCoO2在溶解过程中的化学反应方程式为 。
②调整pH=5-6的目的是 。
按要求完成下列问题:
(1)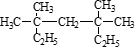 系统命名法为____________________ ,
系统命名法为____________________ ,
(2)4―甲基―1―戊烯的键线式为 __________________________ ,
(3)写出乙醛与新制氢氧化铜反应化学方程式 ____________________________________,
(4)下列有关实验的说法不正确的是_____________。
| A.制乙烯时,温度计应插入反应混合液中 |
| B.检验C2H5Cl中氯元素时,将C2H5Cl和NaOH水溶液混合加热,然后用稀硫酸酸化,再加入AgNO3溶液 |
| C.做过银镜反应的试管用氨水洗涤,做过苯酚的试管用酒精洗涤 |
| D.将一定量CuSO4和NaOH溶液混合后加入甲醛溶液,加热未产生砖红色沉淀,原因可能是NaOH量太少 |
(本题共12分)碘及其化合物可广泛用于医药和工业生产等。回答下列问题:实验室用海带提取I2时操作步骤依次为:灼烧、溶解、过滤、_______、_______及蒸馏。
灼烧海带时除需要三脚架、酒精灯、玻璃棒外,还需要的实验仪器是______________。
“过滤”后溶液中含一定量硫酸盐和碳酸盐。现要检验溶液中的I-,需选择的试剂组合及其先后顺序是_____________。(选填编号)
a.AgNO3溶液 b.Ba(NO3)2溶液 c.BaCl2溶液 d.CaCl2溶液在海带灰滤液中加入适量氯水后一定存在I2,可能存在IO3—。
请补充完整检验含I2溶液中是否含有IO3—的实验方案(可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液):
①取适量含I2溶液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出有碘单质存在;
②_____________________________________________________________________。分解水可用SO2/I2循环法。该法共涉及三步化学反应。
___________________;2H2SO4  2SO2↑+ O2↑+ 2H2O;____________________。
2SO2↑+ O2↑+ 2H2O;____________________。
与传统的分解水的方法相比,本法的优点是____________;缺点是_____________。
某工业废玻璃粉末含SiO2、Fe2O3、CeO2、FeO等。某课题小组设计如下工艺流程对资源进行回收,得到Ce(OH)4和硫酸铁铵矾。
已知:CeO2不溶于稀硫酸;酸性条件下,Ce3+易水解,Ce4+有较强氧化性。
(1)硫酸铁铵矾可净水,其原理是(写离子方程式) 。
(2)滤液A的主要成分 (填写化学式)。
(3)反应①的离子方程式是 。
(4)反应②的化学反应方程式是 。
(5)已知制硫酸铁铵矾晶体[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的产率为80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶体的质量是 。
(6)化合物HT可作为萃取剂能将铈离子从水溶液中萃取出来,过程表示为:
Ce2(SO4)3 (水层)+ 6HT(有机层) 2CeT3 (有机层)+3H2SO4(水层)
2CeT3 (有机层)+3H2SO4(水层)
分液得到CeT3 (有机层),再加入H2SO4 获得较纯的含Ce3+的水溶液。可选择硫酸作反萃取剂的原因是 (从平衡移动角度回答)。
某溶液的溶质是由下列中的几种离子构成:Na+、Fe3+、Cu2+、Ba2+、CO32-、AlO2-、SO32-、SO42-。取该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液,得到白色沉淀丙、气体丙和溶液丙。
④检验气体甲、气体乙、气体丙,都只含有一种成份,而且各不相同。
请回答下列问题:
(1)只根据实验①能得出的结论是 ;
(2)沉淀丙中一定含有 ,可能含有 。
(3)该溶液中肯定存在的离子有 。
(4)气体甲的化学式为 ;气体乙的名称为 ;气体丙的分子几何构型是 ;
(5)向溶液甲中加入NH4HCO3溶液至过量,该过程中发生的离子方程式为 ; 。
(9分)
实验室制备1,2-二溴乙烷的反应原理如下:

可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚。
用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如下图所示:

有关数据列表如下:
| 乙醇 |
1,2-二溴乙烷 |
乙醚 |
|
| 状态 |
色液体 |
无色液体 |
无色液体 |
| 密度/ |
0.79 |
2.2 |
0.71 |
| 沸点/℃ |
78.5 |
132 |
34.6 |
| 熔点/℃ |
一l30 |
9 |
-1l6 |
回答下列问题:
(1)在此制各实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是;(填正确选项前的字母)
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)在装置中应加入,其目的是吸收反应中可能生成的酸性气体:(填正确选项前的字母)
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)判断该制各反应已经结束的最简单方法是;
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在层(填"上"、"下");
(5)若产物中有少量未反应的,最好用洗涤除去;(填正确选项前的字母)
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(6)若产物中有少量副产物乙醚.可用的方法除去;
(7)反应过程中应用冷水冷却装置D,其主要目的是;但又不能过度冷却(如用冰水),其原因是。
工业上常利用低品位软锰矿浆(主要成分是MnO2)来吸收含SO2的废气,最终制得硫酸锰晶体(MnSO4·H2O),其主要流程如下:
已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子。有关金属离子形成氢氧化物沉淀时溶液的pH见下表:
| 离子 |
开始沉淀时的pH |
完全沉淀时的pH |
| Fe2+ |
7.6 |
9.7 |
| Fe3+ |
2.7 |
3.7 |
| Al3+ |
3.8 |
4.7 |
| Mn2+ |
8.3 |
9.8 |
(1)软锰矿浆中通入含SO2废气后,发生主要反应的化学方程式为____________________。
(2)浸出液中加入MnO2粉末的目的是____________;反应的离子方程式是___________________。
(3)溶液中加入石灰浆来调节pH,其作用是_________________;pH应调节的范围是__________。
(4)滤渣的主要成分是________________________________________________(用化学式表示)。
(9分) 现有A、B、C、D、E五种可溶性强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 |
H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 |
OH—、C1—、CO32—、NO3—、SO4— |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性;
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生;
③D溶液与另外四种溶液反应都能产生沉淀;C只能与D反应产生沉淀;
④上述沉淀包括难溶物和微溶物。
试回答下列问题:
(1)写出A溶液与E溶液反应的化学方程式: _________。
(2)写出E溶液与过量的B溶液反应的离子方程式: ____。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1) △H=-akJ·mol-1。请写出B与C的稀溶液反应的热化学方程式: _____________________。