海水中含有丰富的化学元素,下面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:

请回答:
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液
则加入试剂的顺序是(填编号) 。
(2)Mg(OH) 2中加入盐酸后,要获得MgCl 2•6H 2O晶体,需要进行的实验操作依次 。
A.蒸馏 B.灼烧 C.过滤 D.蒸发 E.冷却结晶
(3)目前工业上主要采用离子交换膜法电解饱和食盐水,下列关于离子交换膜电解槽的叙述错误的是 .
A.精制饱和食盐水进入阳极室 B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气 D.电解槽的阳极用金属铁网制成
(4)写出电解饱和NaCl溶液的离子方程式:
(5) 利用MgCl 2•6H 2O可制得无水氯化镁,应采取的措施是
(6) 用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
海水中蕴藏着丰富的资源。海水综合利用的流程图如下。

(1)粗盐中含Ca2+、Mg2+、Fe3+、SO42—及泥沙等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液的pH等于7;⑤溶解;⑥过滤; ⑦蒸发。正确的操作顺序是 (填写序号字母)。
| A.⑤①③②④⑥⑦ | B.⑤①②③⑥④⑦ |
| C.⑤③①②⑥④⑦ | D.⑤③②①⑥④⑦ |
(2)NaCl做原料可以得到多种产品。
①工业上由金属钠制备过氧化钠的方法是:将金属钠迅速升温至熔化,并控制温度在300–400℃,通入经处理过的空气可制得过氧化钠,处理空气的目的是 。工业生产中因温度过低而得不到纯净的过氧化钠,你认为可能含有的杂质是 (填化学式)。
② 实验室用惰性电极电解100 mL0.1 mol/LNaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为(常温下) (忽略反应前后溶液的体积变化)。
③ 电解氯化钠稀溶液可制备“84消毒液”,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式: 。
(3)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品。
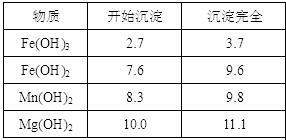
① 粗产品的溶液中含有Na+、Fe2+、Fe3+和Mn2+,需将Fe2+、Fe3+、Mn2+转化为沉淀除去。因此先向溶液中加入一种上述(1)中得到的物质NaClO,然后控制溶液的pH为 。
② 由MgCl2·6H2O晶体制备无水MgCl2的方法是 。
某学生为了测定部分变质的Na2SO3样品的纯度。按右图所示称取一定量的Na2SO3样品放入A装置的烧瓶中,滴入足量的H2SO4至完全反应;然后,将B中完全反应后的溶液与足量的BaCl2溶液反应,过滤、洗涤、干燥,得白色沉淀23.3g。回答下列问题:
(1)写出A装置中玻璃仪器的名称:酒精灯、______________、______________。
(2)实验开始时,应先点燃__________________处酒精灯(填装置字母)。
(3) 写出D中反应的化学方程式__________________________________。
(4)实验开始后,写出B中反应的离子方程式_______________________。
(5)C中的现象是____________________,E装置的作用是__________________。
(6)原样品中Na2SO3的纯度为__________(精确到0.1%)。按题给装置和操作进行实验,若装置连接和实验操作均无任何问题,该学生测得的Na2SO3的纯度_____(填“偏高”、“偏低”或“无影响”)。
用中和滴定法测定烧碱的纯度,若烧碱中不含有与酸反应的杂质,试根据实验回答:
(1)准确称取烧碱样2.50g,将样品配成250mL的待测液。
(2)滴定管使用前除洗涤外,还应 。
(3)取10.00mL待测液,用 量取注入锥形瓶中。(填仪器)
(4)用0.2000mol/L标准盐酸溶液滴定待测烧碱溶液,滴定时左手旋转酸式滴定管的玻璃活塞,右手不停地摇动锥形瓶,两眼注视 直到滴定终点。
(5)根据下列测定数据,分析得到合理数据,计算待测烧碱溶液的浓度: 。
| 滴定次数 |
待测液体积/mL |
标准盐酸体积/mL |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
10.00 |
0.50 |
10.40 |
| 第二次 |
10.00 |
4.00 |
14.10 |
| 第三次 |
10.00 |
4.20 |
15.70 |
(6)根据上述测定数据,分析得到合理数据,计算烧碱的纯度 。
有一包白色固体,可能含有CaCO3、Na2SO4、KNO3、CuSO4、BaCl2五种物质中的一种或几种。现进行如下实验:
①取少量固体粉末,加入盛有足量水的烧杯中,充分搅拌静置后,底部白色沉淀,上层为无色溶液;
②继续往烧杯中加入足量稀硝酸,白色沉淀完全消失;并有气泡产生。
③取少量②中溶液滴加Ba(NO3)2溶液,有白色沉淀生成,再加入稀硝酸,沉淀不溶解。
(1)根据以上实验现象可知,该白色固体中一定含有 ,(填化学式,下同)一定不含有 ,可能含有 。
(2)上述实验②过程中所发生反应的离子方程式为:__________________________。
某研究性学习小组的同学通过课外学习了解到:某品牌牙膏中含有摩擦剂、湿润剂、表面活性剂、黏合剂、香料、甜味剂等成分,其中的摩擦剂除了含CaCO3外,可能还含有Al(OH)3、SiO2中的一种或两种。为探究该品牌牙膏中摩擦剂的成分,该小组的同学进行了如下实验(牙膏中其他成分遇到盐酸时无气体产生):
请回答下列问题:
(1)操作Ⅰ中涉及的玻璃仪器有烧杯、________、________
(2)写出下列操作Ⅳ的离子方程式:______________________________
(3)该摩擦剂中除CaCO3外,肯定含有__________________
(4)为进一步探究摩擦剂中碳酸钙的含量,该小组同学利用如图所示装置(图中夹持仪器略去)进行实验。
请回答下列问题:
①实验过程中需持续缓缓通入空气。其作用除了可充分混合装置乙和丙中的反应物外,还有________的作用;
②丙中主要反应的化学方程式是_______________
③实验中准确称取4.00 g样品三份,进行三次测定,测得BaCO3的平均质量为1.97 g,计算样品中碳酸钙的质量分数:__________________________
④有同学认为只要测定装置丙在吸收CO2前后的质量差,不必测定装置丙中生成的BaCO3质量,一样可以确定碳酸钙的质量分数。你认为该方案是否可行?________,简述理由:________。
我国废水三级排放标准规定:废水中苯酚的含量不得超过1.00mg/L。实验室可用一定浓度的溴水测定某废水中苯酚的含量,其原理如下:

(1)请完成相应的实验步骤:
步骤1:准确量取25.00mL待测废水于250mL锥形瓶中。
步骤2:将5.0 mL 0.01mol/L溴水迅速加入到锥形瓶中,塞紧瓶塞,振荡。
步骤3:打开瓶塞,向锥形瓶中加入过量的0.1mol/L KI溶液,振荡。
步骤4: ,再用0.01 mol/L Na2S2O3标准溶液滴定至终点,消耗 Na2S2O3溶液8.50 mL。(反应原理:I2 + 2Na2S2O3 =" 2NaI" + Na2S4O6)
(2)该废水中苯酚的含量为 mg/L。
(3)步骤2塞紧瓶塞的原因是 。
(4)步骤3若振荡时间过长,则测得的废水中苯酚的含量 (填“偏高”、“偏低”或“无影响”,下同)。步骤4中若滴定至终点时滴定管尖嘴处出现气泡,而滴定前无气泡,会使测得的废水中苯酚的含量 。
某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定
操作:
A.在250 mL容量瓶中配制250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL 烧碱溶液于锥形瓶中并加几滴酚酞指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
请完成下列问题:
(1)正确的操作步骤是(填写字母)__→__→__→D→__。
(2)操作D中液面应调整到_______________;尖嘴部分应_________________。
(3)以下操作会造成所测烧碱溶液浓度偏低的是( )
A.酸式滴定管未用待装溶液润洗
B.碱式滴定管未用待装溶液润洗
C.锥形瓶未用待装溶液润洗
D.在滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
(4)该烧碱样品的纯度计算式是__________________________________________。
(1)溶液的pH除了可以通过实验得出的具体数据计算得到,在实验室中还可以用________或_________来测量得到。
(2)某研究性学习小组用pH=1的盐酸滴定25.00 mL未知物质的量浓度的NaOH溶液,从而求出该NaOH溶液的pH值(选用酚酞作为指示剂)
①实验过程中需要使用的仪器有铁架台、滴定管夹、碱式滴定管、胶头滴管、________、 ,
②右图,是某次滴定时的滴定管中的液面,其读数为 mL;

③如何判断滴定到达终点________________________
④根据下列数据:
| 滴定次数 |
待测液体积(mL)[来源 |
标准盐酸体积(mL) |
|
| 滴定前读数(mL) |
滴定后读数(mL) |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
4.00 |
24.10 |
请计算待测NaOH溶液的浓度(保留两位小数) mol/L
⑤在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有: 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用盐酸溶液润洗
C.锥形瓶水洗后未干燥
D.酸式滴定管尖嘴部分有气泡,滴定后消失
某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在250 mL容量瓶中配制250 mL烧碱溶液
B.用移液管(或碱式滴定管)量取25.00 mL 烧碱溶液于锥形瓶中,并加几滴酚酞指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol·L-1的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
请完成下列问题:
(1)正确的操作步骤是(填写字母): → → →D→ 。
(2)操作D中液面应调整到 ;开始E操作前须确保尖嘴部分 。
(3)以下操作会造成所测烧碱溶液浓度偏低的是 。
A.酸式滴定管未用待装溶液润洗
B.碱式滴定管未用待装溶液润洗
C.锥形瓶未用待装溶液润洗
D.在滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
E.在滴定前仰视,滴定后平视
F.滴定结束还有一滴挂在滴定管尖嘴外面
(4)该烧碱样品的纯度计算式是 (需化简)。
市售乙醛通常为40%左右的乙醛溶液。久置的乙醛溶液会产生分层现象,上层为无色油状液体,下层为水溶液。据测定,上层物质为乙醛的加合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基。乙醛在溶液中易被氧化,为从变质的乙醛溶液中提取乙醛(仍得到溶液),可利用如下反应原理:
(C2H4O)n nC2H4O。
nC2H4O。
(1)先把混合物分离得到(C2H4O)n:将混合物放入____中,静置,分离操作名称为______。
(2)证明是否已有部分乙醛被氧化的实验操作和现象是______________。
(3)提取乙醛的装置如图:烧瓶中放的是(C2H4O)n和6mol/LH2SO4的混合液,锥形瓶中是蒸馏水。加热至混合液沸腾,(C2H4O)n缓慢分解,生成的气体导入锥形瓶的水中。
①用冷凝管的目的是________,冷凝水的进口是_____(填“a”或“b”)。
②锥形瓶内导管口出现气泡,从下到上升至液面过程中,体积越来越小,直至完全消失,说明乙醛具有___的性质,当观察到导气管中气流很小时,必要的操作是_____,目的是__________。
维生素C是一种水溶性维生素(其水溶液呈酸性),它的分子式是C6H8O6(相对分子质量为176),人体缺乏这种维生素易得坏血症,所以维生素C又称抗坏血酸。维生素C易被空气中的氧气氧化。在新鲜的水果、蔬菜、乳制品中都富含维生素C,如新鲜橙汁中维生素C的含量在500 mg·L-1左右。校课外活动小组测定了某品牌的软包装橙汁中维生素C的含量。下面是测定实验分析报告,请填写有关空白。
(1)测定目的:测定××牌软包装橙汁维生素C含量。
(2)测定原理:C6H8O6+I2  C6H6O6+2H++2I-。
C6H6O6+2H++2I-。
(3)实验用品及试剂:
①仪器和用品(自选,略)。
②试剂:指示剂 (填名称)、浓度为7.50×10-3mol·L-1标准碘溶液、蒸馏水等。
(4)实验过程:
①洗涤仪器:检查滴定管是否漏液,润洗后装好标准碘溶液待用。
②打开橙汁包装,目测:颜色——橙黄色,澄清度——好。用 (填仪器名称)向锥形瓶中移入25.00 mL待测橙汁,滴入2滴指示剂。
③用左手控制滴定管的 (填部位的名称),右手摇动锥形瓶,眼睛注视 直到滴定终点。滴定至终点的现象是 。
(5)数据记录与处理。滴定中消耗标准碘溶液的体积见下表,请计算此橙汁中维生素C的含量是② mg·L-1。

50mL0.50 mol·L-1盐酸与50mL0.55 mol·L-1NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)右图装置名称为____,图中尚缺少的一种玻璃用品名称是_____。
(2)烧杯间填满碎纸条的作用是_______。
(3)实验中改用60mL0.50 mol·L-1盐酸与50mL0.55 mol·L-1NaOH溶液进行反应,与上述实验相比较,所放出的热量_____(填“相等”或“不相等”),中和热______(填“相等”或“不相等”),理由是______。
(4)用相同浓度和体积的氨水代替NaOH 溶液进行上述实验,测得中和热的数值与57.3kJ / mol 相比较会_____。(填“偏大”“偏小”或“无影响”)。
(5)完整地做一次这样的实验,需测定___次温度。
(6)大烧杯上如不盖硬纸板,求得的中和热数值____(填“偏大”、“偏小”或“无影响”)
有一固体粉末,其中可能含有Na2CO3、NaCl、Na2SO4、CuCl2、Ba(NO3)2、K2CO3、K2SO4中的一种或几种,现按下列步骤进行实验。
(1)将该粉末溶于水得无色溶液和白色沉淀。
(2)在滤出的沉淀中加入过量稀硝酸,有部分沉淀溶解,同时产生无色气体。
(3)取滤液做焰色反应,火焰呈黄色,透过蓝色钴玻璃观察没有明显现象。
由上述现象推断:
该混合物中一定含有 ;一定不含有 ;可能含有 ,如要检验其是否存在,应如何操作(写明操作步骤及实验结论) 。
请完成下列物质的分离提纯问题。
Ⅰ、现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:试剂X_______,沉淀B 。
(2)证明AgNO3加过量的实验方法是 。
(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________,之后若要获得固体NaNO3需进行的实验操作是___________(填操作名称)。
Ⅱ、某同学欲用CCl4萃取较高浓度的碘水中的碘,操作过程可以分解为如下几步:
| A.把盛有溶液的分液漏斗放在铁架台的铁圈中; |
| B.把50ml碘水和15mlCCl4加入分液漏斗中,并盖好玻璃塞; |
| C.检验分液漏斗活塞和上口的玻璃塞是否漏液; |
| D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正; |
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
(1)萃取过程正确操作步骤的顺序是:(填编号字母) 。
(2)设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法: 。(3)最后碘的CCl4是通过 获得(填“漏斗上口”或“漏斗下口”)。从含碘的CCl4溶液中提取碘 和回收CCl4,还需要经过蒸馏,观察下图所示实验装置指出其错误有 处。
(4)进行上述蒸馏操作时,最后晶态碘在____________(填仪器名称)里聚集。
