从樟科植物枝叶提取的精油中含有甲、乙两种成分: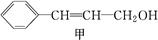
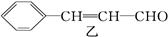
(1)①甲和乙中含氧官能团的名称分别为 和 。
②请写出甲的一种能同时满足下列3个条件的同分异构体的结构简式 。
a.苯环上有两个不同的取代基
b.能与Br2的CCl4溶液发生加成反应
c.遇FeCl3溶液呈现紫色
(2)由甲转化为乙的过程为(已略去无关产物):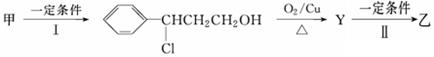
反应Ⅰ的反应类型为 ,Y的结构简式___________________________。
(3)1 mol乙最多可与________ mol H2发生加成反应。
(4)写出乙与新制Cu(OH)2悬浊液反应的化学方程式__________________________
(1)只用一种试剂(可加热)就可区别下列五种无色液体:CH3CH2CH2OH、CH3CH2CHO、HCOOH、CH3COOH、CH3COOCH2CH3,该试剂可以是 。
(2)①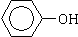 ②CH2=CH2 ③CH≡CH ④
②CH2=CH2 ③CH≡CH ④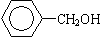
⑤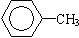 ⑥
⑥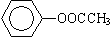 ⑦CH3CH2CH2CH2Br
⑦CH3CH2CH2CH2Br
上述有机物中(填写上述物质的序号)
①属于芳香烃的是 ;
②能与溴水发生加成反应的是 ;
③能发生消去反应的是 ;
④能与NaOH溶液反应,但不能与Na2CO3溶液反应的是 。
【化学选修——有机基础化学】某有机化合物A的结构简式如图所示,回答下列问题。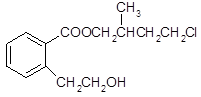
(1)A能发生消去反应的官能团名称为 。
(2)A在NaOH水溶液中加热得B和C,C是芳香族化合物。
①B的结构简式是 。
②C酸化后可得到D,D不能发生的反应是 (填选项标号)
a.取代反应 b.水解反应 c.加成反应 d.消去反应
(3)D可以发生如下转化,且E与F互为同分异构体。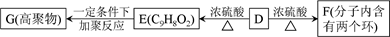
①F的结构简式是 。
②由D生成E的化学方程式 。
(4)符合下列三个条件的D的同分异构体种类有 种(不包括D)。
①只含有邻二取代苯环结构;
②与D具有相同的官能团;
③不与FeCl3溶液发生显色反应
丙烯醇( )是一种重要的有机合成原料。
)是一种重要的有机合成原料。
(1)丙烯醇中含有的官能团的化学符号是
(2)0.3mol丙烯醇与11.5g金属钠反应,能生成标准状况下的氢气_________ L。
(3)写出丙烯醇与溴水反应的化学方程式____________________________
(4)丙烯醇与CH3 CO 18OH发生酯化反应的化方程式为:_______________________
酯化反应生成的产物在一定条件下可以发生加聚反应得到高分子化合物,其结构简式为________
(5)设计方案用丙烯醇合成丙烯,在下面空格中写出方案中涉及的所有化学反应方程式:
(5分)有机物A的结构简式为 ,它可通过不同化学反应分别制得B、C、D和E四种物质。
,它可通过不同化学反应分别制得B、C、D和E四种物质。
请回答下列问题:
(1)写出有机物A中官能团的名称: 、 。
(2)在A~D四种物质中,与E互为同分异构体的是 (填代号)。
(3)写出有机物C发生加聚反应生成高分子化合物的化学方程式 。
Ⅰ.乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产。
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯C2H5OSO3H),再水解生成乙醇。写出相应反应的化学方程式:_________________________________。
(2)已知:
甲醇脱水反应 2CH3OHg) === CH3OCH3g) + H2Og) △H1="=" -23.9 kJ·mol—1
甲醇制烯烃反应 2CH3OHg) === C2H4g) + 2H2Og) △H2="=" -29.1 kJ·mol—1
乙醇异构化反应 C2H5OHg) === CH3OCH3g) △H3== + 50.7 kJ·mol—1[来源:Z_xx_k.Com]
则乙烯气相直接水合反应C2H4g) + H2Og)=== C2H5OHg)的△H == __________________________。与间接水合法相比,气相直接水合法的优点是__________________________________。
Ⅱ. 甲醇虽然毒性很强,但它是一种清洁燃料,也是一种重要的合成原料。工业甲醇的质量分数可以用下列方法测定:
①在稀硫酸中甲醇被Cr2O72-氧化成CO2和H2O,其反应为:
CH3OH + Cr2O72— + 8H+==== CO2↑+ 2Cr3++ 6H2O;
②过量的Cr2O72—可用Fe2+与之完全反应,反应如下所示:
____Cr2O72— + ____Fe2+ +____H+――― ____Cr3++____Fe3+ +____H2O
现有0.12 g工业甲醇,在稀硫酸中与25.0 mL 0.2 mol/L K2Cr2O7溶液反应,多余的K2Cr2O7恰好与9.6 mL 1.0 mol/LFeSO4溶液完全反应。
(3)请配平第②步中离子方程式配平系数依次填写在短线上)。
(4)工业甲醇的质量分数为__________。
(1)(5分)由A、B两种气态烃组成的混合气体,对H2的相对密度为17。常温常压下,取这种混合气体10mL与80mL氧气(过量)混合,当完全燃烧后恢复到原状态时,测得气体的体积为70mL。试求:
①混合气体的平均组成为(用CxHy的形式表示)___________;
②若上述两种气体按体积1:1混合时,则两种气态烃的可能组成为__________________。
(2)(5分)具有支链的化合物X的分子式为C4H8O,X既能使Br2的四氯化碳溶液褪色,又能与Na反应。①X的结构简式是 ,
②写出与X具有相同官能团的X的所有同分异构体的结构简式:______________。
某物质的分子式为C4H10O。
(1)它能被催化氧化生成相同碳原子数的醛有_________种,
它们对应的醇分别为(写结构简式)___________,___________。
(2)它能被催化氧化成相同碳原子数的酮有 种,写出结构简式并命名_________,___________。
(3)不能被催化氧化的醇的结构简式和名称___________,___________。
(4)能发生消去反应,有机产物只有一种物质的有_________种;两种的有_________种,产物的结构简式为_________和_________。
现有分子式都是C7H8O的芳香族化合物A、B、C三种物质。若各取少许分别滴加FeCl3溶液,只有C呈紫色;若投入金属钠,只有B无明显变化。
(1)写出A、B的结构简式______。
(2)C有多种同分异构体,若其一溴代物最多有两种,C的这种同分异构体的结构简式为________。
【改编】单体液晶(有机物III)是用偶联反应合成的:
反应①
反应②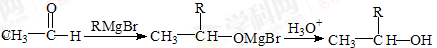
试回答以下问题:
(1)有机物Ⅲ中官能团的名称为 :有机物Ⅰ能发生的反应为 :
①加成反应 ②酯化反应 ③醇氧化为醛(或酮) ④消去反应
(2)若要通过反应②制备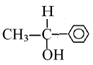 ,则需要两种有机物的结构简式分别是 。
,则需要两种有机物的结构简式分别是 。
(3)写出由有机物III制备  的反应方程式 。
的反应方程式 。
(4)符合下列条件的有机物III同分异构体有 种。
①苯环上有2个取代基;
②能发生银镜反应;
③分子中含有2个甲基。
(5)CH≡CCH2OH与CH3I能发生类似①的反应,该反应方程式是: 。
现有四种有机化合物:
试回答:
(1)甲、乙、丁都含有的官能团的名称是________。
(2)1 mol甲、乙、丁分别与足量Na反应,生成H2最多的是________(填编号,下同)。
(3)互为同分异构体的是________。
(4)等物质的量的甲、乙、丙、丁充分燃烧,消耗氧最少的是________。
(5)丁与醋酸在催化剂作用下发生取代反应生成的酯有________种。
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一。莽草酸 (A)的结构简式为: (提示:环丁烷
(提示:环丁烷 可简写成□)
可简写成□)
(1)A的分子式为___________
(2)A与溴的四氯化碳溶液反应的化学方程式为_________ __
(3)A与氢氧化钠溶液反应的化学方程式为________ ___
(4)17.4 g A与足量的碳酸氢钠溶液反应,则生成的二氧化碳的体积(标准状况)为________________
(5)A在浓硫酸作用下加热可得到B(B的结构简式为 ),其反应类型是___________
),其反应类型是___________
1mol分子组成为C3H8O的液态有机物A,与足量的金属钠作用,可生成11.2 L氢气(标准状况),则A分子中必有一个___基,若此基在碳链的一端,则A的结构简式为 。A与浓硫酸共热,分子内脱去1分子水,生成B,反应的方程式为 ;B通入溴水能发生________反应,反应的方程式为 。
下列反应原理可以用于检查司机是否酒后开车。
K2Cr2O7+C2H5OH+H2SO4—Cr2(SO4)3+CH3COOH+K2SO4+
(1)在反应中,氧化剂是 。如果在反应中生成1molCr3+,转移电子数为 。(用NA表示阿伏加德罗常数)
(2)写出上述化学方程式所缺项(填化学式) 。
(3)乙醇(C2H5OH)和乙醚(CH3CH2OCH2CH3)的沸点分别是78.5℃、34.5℃,分离二者混合物的方法是 ,乙醇比乙醚的沸点高的原因是 。
(10分,每空2分)A、B、C、D是四种短周期元素,它们的原子序数依次增大。其中A、D元素同主族且A是原子半径最小的元素,B、C元素同周期,B的最外层电子数是次外层电子数的2倍;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙为其中的三种,它们的元素组成如下表所示:
| 化合物 |
甲 |
乙 |
丙 |
| 组成元素 |
B、C |
A、C |
C、D |
常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质为固体且为离子化合物。请填写下列空白:
(1)乙的化学式为 ,丙物质的化学式为 ,其中丙中阴离子与阳离子的个数之比为 。
(2)某同学设计了一个CH3OH燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如下图:
①写出ⅰ中通入甲醇这一极的电极反应式 。
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式 。