某研究小组对铁生锈进行研究:
(1)经过较长时间后,甲同学观察到的现象是:上图中的铁钉最容易生锈的是 (填字母);
(2)根据实验条件判断,在铁钉的锈蚀过程中,正极的电极反应为: ;
(3)若为了防止铁钉生锈,该小组同学想在铁钉表面镀上一层金属,该金属最好是
A. 锡 B. 铜 C. 锌
(4)钢铁容易腐蚀,工业生产中常需对钢铁进行“发蓝”处理,以有效避免或减缓钢铁的腐蚀。所谓“发蓝”,就是在钢铁零件等进行氧化处理,使其表面形成一层致密的蓝黑色氧化膜。发蓝处理过程可表示如下:
为检验经过步骤Ⅳ处理的铁件是否合格,常往成品表面滴上5%的硫酸铜溶液,如果成品不合格(即铁件表面有微小松孔,未形成致密的氧化膜),一段时间将观察到的现象为__________________________。
下列各种镀有金属保护层的铁板,当镀层破损时相同的普通环境中,最易被腐蚀的是( )
| A.镀锌铁(白铁) | B.镀锡铁(马口铁) | C.镀银铁 | D.镀铜铁 |
下图容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是
| A.4>2>1>3 | B.2>1>3>4 | C.4>2>3>1 | D.3>2>4>1 |
下列关于金属腐蚀的叙述正确的是
| A.钢铁在潮湿空气中的腐蚀主要是化学腐蚀 |
| B.金属的化学腐蚀的实质是:M—ne-=Mn+ |
| C.金属的化学腐蚀必需在酸性条件下进行 |
| D.在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀 |
(1)反应A+3B 2C+2D在四种不同情况下的反应速率分别如下:
2C+2D在四种不同情况下的反应速率分别如下:
该反应进行的由快到慢顺序为 (填序号)
(2)铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中如下图所示,则铁被腐蚀的速率由慢到快的顺序是(填序号)_______________。
下列金属防腐的措施中,使用外加电流的阴极保护法的是
| A.水中的钢闸门连接电源的负极 |
| B.金属护栏表面涂漆 |
| C.汽车底盘喷涂高分子膜 |
| D.地下钢管连接镁块 |
钢铁在腐蚀过程中,下列变化可能发生的是
①铁元素由+2价转化为+3价 ②氧气被还原 ③产生氢气 ④Fe(OH)3失水生成Fe2O3·xH2O
⑤杂质碳被氧化而除去
| A.只有①② | B.只有③④ | C.只有①②③④ | D.①②③④⑤ |
下列说法正确的是
| A.氯碱工业中,烧碱在阳极区生成 |
| B.电解熔融氯化铝冶炼金属铝 |
| C.电镀时,用镀层金属作阳极 |
| D.将钢闸门与外电源正极相连,可防止其腐蚀 |
下列各装置中都盛有0.1 mol·L-1的NaCl溶液,放置一定时间后,装置中的四块相同锌片,腐蚀速率由快到慢的正确顺序是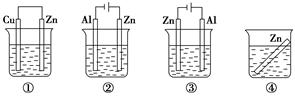
| A.③①④② | B.②①④③ | C.①②③④ | D.①②④③ |
下列与金属腐蚀有关的说法正确的是
| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
D.图d中,工作时NH  的移动方向为由里向外 的移动方向为由里向外 |
如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是
| A.④>②>①>③ | B.②>①>③>④ |
| C.④>②>③>① | D.③>②>④>① |
如图所示,甲、乙两装置电极材料都是铁棒与碳棒,请回答下列问题:
(1)若两装置中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲装置中的________棒,乙装置中的________棒。
②乙装置中阳极的电极反应式是:_______________________________。
(2)若两装置中均为饱和NaCl溶液:
①写出乙装置中总反应的离子方程式:_____________________________。
②甲装置中碳极的电极反应式是 ,乙装置碳极的电极反应属于________(填“氧化反应”或“还原反应”)。
③将湿润的淀粉KI试纸放在乙装置碳极附近,发现试纸变蓝,解释其原因: 。
家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是( )
| A.4Fe(OH)2+2H2O+O2===4Fe(OH)3↓ | B.2Fe+2H2O+O2===2Fe(OH)2↓ |
| C.2H2O+O2+4e-===4OH- | D.Fe-3e-===Fe3+ |