漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年,亚氯酸(HClO2为弱酸)不稳定可分解,反应的离子方程式为:5HClO2=4ClO2↑+H++Cl-+2H2O。向NaClO2溶液中滴加H2SO4,开始时HClO2分解反应反应缓慢,随后反应迅速,其原因是
| A.在酸性条件下,亚氯酸钠的氧化性增强 |
| B.溶液中的Cl-起催化作用 |
| C.ClO2逸出,使反应的生成物浓度降低 |
| D.溶液中的H+起催化作用 |
将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸。右边图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是
用1.0mol·L-1NaOH溶液中和某浓度硫酸溶液时,其pH和所加NaOH溶液的体积(V)关系如图所示。则原硫酸溶液的物质的量浓度和恰好完全反应后溶液的总体积分别是(设二者混合后体积为二者体积之和)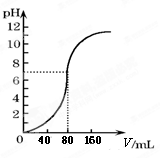
| A.0.5mol·L-1 160mL |
| B.1.0mol·L-1 160mL |
| C.0.5mol·L-1 80mL |
| D.1.0mol·L-1 80mL |
3.某溶液中可能含有OH-、CO 、AlO
、AlO 、SiO
、SiO 、SO
、SO 、Na+、Mg2+、Al3+八种离子中的几种。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸的体积的变化如下图所示。由此可知原溶液中
、Na+、Mg2+、Al3+八种离子中的几种。当向该溶液中加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸的体积的变化如下图所示。由此可知原溶液中
A.不含SO |
B.含有的阴离子一定是OH-、AlO 、SiO 、SiO |
C.含有的阴离子一定是OH-、CO 、AlO 、AlO 、SiO 、SiO |
D.含有的AlO 与SiO 与SiO 的物质的量之比为3:1 的物质的量之比为3:1 |
将溶液(或气体)X逐渐加入(或通入)到一定量Y溶液中,产生沉淀的质量与加入X的物质的量关系如下图,符合图中情况的一组物质是:
| |
A |
B |
C |
D |
| X |
Ba(HCO3)2溶液 |
Na2CO3溶液 |
KOH溶液 |
CO2气体 |
| Y |
NaOH溶液 |
CaCl2溶液 |
Mg(HSO4)2溶液 |
石灰水 |
对下列图像的描述正确的是
| A.根据图①可判断反应的ΔH <0 |
| B.根据图②,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
C.图③可表示压强(p)对反应2A(g)+2B(g)  3C(g)+D(s)的影响 3C(g)+D(s)的影响 |
| D.图④ 可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液中肯定不存在的离子组是
| A.Al3+、Mg2+、I-、SO32- | B.Mg2+、Na+、CO32-、I- |
| C.Al3+、Na+、SO32-、I- | D.Al3+、CO32-、Br-、SO32- |