如图装置,U型管中盛有Fe(OH)3胶体,以两个碳棒为电极进行电解,一段时间后,下列叙述正确的是
| A.x是阳极,y是阴极 |
| B.x极附近颜色变深,y极近颜色变浅 |
| C.x是阴极,y极附近颜色加深 |
| D.y是阴极,x极附近颜色加深 |
人工光合作用能够借助太阳能,用CO2和H2O制备化学原料.下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是 ( ) 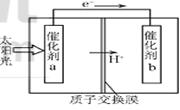
| A.该过程是将太阳能转化为化学能的过程 |
| B.催化剂a表面发生氧化反应,有O2产生 |
| C.催化剂a附近酸性减弱,催化剂b附近酸性增强 |
| D.催化剂b表面的反应是CO2 +2H++2e一=HCOOH |
用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解质溶液的pH下降的是( )
| A.CuCl2 | B.H2SO4 | C.NaCl | D.AgNO3 |
用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中正确的是 
| A.燃料电池工作时,正极反应为:O2+2H2O+4e一=40H— |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
下列说法不正确的是
| A.氢气是一种环保、可再生的能源 |
| B.电解熔融AlCl3可制金属铝 |
| C.可溶性铁盐或铝盐常用于水的净化 |
| D.二氧化硅可用于制作光导纤维 |
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9 ]。t1时刻a电极得到混合气体,其中Cl2在标准状况下为 224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是
| A.a电极与电源的负极相连 |
| B.t2时,两电极的质量相差3.84 g |
| C.电解过程中,溶液的pH不断增大 |
| D.t2时,b电极的电极反应是2H2O-4e-=2OH-+H2↑ |
下列关于电解池中形成闭合回路的叙述中,正确的是( )
| A.电解池中的闭合回路仅是由电子的定向运动形成的 |
| B.电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 |
| C.在电解质溶液中,阴离子向阴极移动,阳离子向阳极移动 |
| D.相同时间内阳离子在阴极得到的电子与阴离子在阳极失去的电子数相等 |
下列叙述正确的是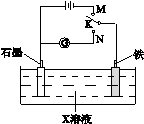
| A.K与N连接时,X为硫酸,一段时间后溶液的pH减小 |
| B.K与N连接时,X为氯化钠,石墨电极反应:2H++2e- = H2↑ |
| C.K与M连接时,X为氯化钠,石墨电极反应:4OH- -4e- =2H2O+O2↑ |
| D.K与M连接时,X为硫酸,一段时间后溶液的pH减小 |
以惰性电极电解一定浓度的CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1mol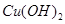 ,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
,恰好恢复到电解前的pH和浓度,则电解过程中转移的电子的物质的量为:
| A.0.1mol | B.0.2mol | C.0.3mol | D.0.4mol |
如图所示,下列有关装置的分析中正确的是( )

| 选项 |
开关控制 |
X溶液 |
装置叙述 |
| A |
接通K2, 断开K1 |
HCl |
Fe极为正极, 该极质量减小 |
| B |
接通K2, 断开K1 |
CuCl2 |
Fe极为负极, 该极质量增加 |
| C |
接通K1, 断开K2 |
CuSO4 |
Fe极为阴极, 该极有Cu析出 |
| D |
接通K1, 断开K2 |
NaCl |
Fe极为阳极, 该极逐渐溶解 |
电解CuCl2溶液时,如果阴极上有1.6g铜析出,则阳极上产生气体的体积(标准状况)约为( )
| A.0.28 L | B.0.56 L | C.0.14 L | D.11.2 L |
下列有关电化学装置完全正确的是( )
| A |
B |
C |
D |
 |
 |
 |
 |
| 铜的冶炼 |
铁上镀银 |
防止Fe被腐蚀 |
构成铜锌原电池 |
A.A B.B C.C D.D
下图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )
| A.a为阳极、b为阴极 | B.a为负极、b为正极 |
| C.电解过程中,氯离子浓度不变 | D.电解过程中,d电极质量增加 |
按图甲装置进行实验,若图乙中横坐标x表示通过电极的电子的物质的量。下列叙述正确的是( )
| A.F表示反应生成Cu的物质的量 |
| B.E表示反应实际消耗H2O的物质的量 |
| C.E表示反应生成O2的物质的量 |
| D.F表示反应生成H2SO4的物质的量 |