如图所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细,由此判断表中所列M,N,P物质,其中可以成立的是

| |
M |
N |
P |
| A |
Zn |
Cu |
稀硫酸 |
| B |
Cu |
Fe |
稀盐酸 |
| C |
Ag |
Zn |
AgNO3溶液 |
| D |
Fe |
C |
CuSO4溶液 |
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是
| 待测气体 |
部分电极反应产物 |
| NO2 |
NO |
| Cl2 |
HCl |
| CO |
CO2 |
| H2S |
H2SO4 |
A.上述气体检测时,敏感电极均作电池正极
B.检测分别含H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同
C.检测H2S时,对电极充入空气,对电极上的电极反应式为O2 + 2H2O+ 4e- = 4OH-
D.检测Cl2时,敏感电极的电极反应式为:Cl2 + 2e-= 2Cl-
某合作学习小组的同学利用下列氧化还原反应设计 原电池:2KMnO4 + 10FeSO4 + 8H2SO4=2MnSO4 + 5Fe2(SO4)3+K2SO4+8H2O,盐桥中装有饱和K2SO4溶液。下列叙述中正确的是
| A.乙烧杯中发生还原反应 |
| B.甲烧杯中溶液的pH逐渐减小 |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.外电路的电流方向是从a到b |
某电源装置如图所示,电池总反应式为:2Ag+Cl2===2AgCl。下列说法正确的是
| A.正极反应为AgCl+e-═Ag+Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01mol e-时,交换膜左则溶液中约减少0.02mol离子 |
下图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5 mol·L -1,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
| A.产生气体体积 ①=② |
| B.①中阴极质量增加,②中正极质量减小 |
| C.电极反应式:①中阳极:4OH- - 4e- = 2H2O+O2 ↑ ②中负极:2H + +2e-=H2 ↑ |
| D.溶液的pH变化:①减小,②增大 |
右图是某同学设计的验证原电池和电解池的实验装置,下列说法不正确的是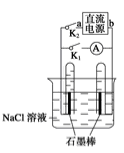
| A.若关闭K2、打开K1,一段时间后,发现左侧试管收集到的气体比右侧略多,则a为正极,b为负极 |
| B.关闭K2,打开K1,一段时间后,用拇指堵住试管移出烧杯,向试管内滴入酚酞,发现左侧试管内溶液变红色,则 a为负极,b为正极 |
| C.若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,再关闭K1,打开K2,则电路中电流方向为从右侧石墨棒沿导线到左侧石墨棒 |
| D.若直流电源a为负极,b为正极,关闭K2,打开K1,一段时间后,左侧产生的是氢气,右侧产生的是氯气,再关闭K1,打开K2,构成原电池,则左侧是正极,右侧是负极,在左侧石墨棒上发生还原反应,发生的电极反应为H2-2e-+2OH-=2H2O,正确。 |
对于右图所示的铜-锌原电池,下列说法不正确的是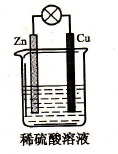
| A.铜为正极 |
| B.锌片发生氧化反应 |
| C.它是一种把化学能转换为电能的装置 |
| D.铜片向外电路提供电子,锌片从外电路获得电子 |
锂离子电池已经成为新一代实用化的蓄电池,该电池具有能量密度大、电压高的特性。锂离子电池放电时的电极反应式为:负极反应:C6Li-xe-==C6Li1-x+xLi+(C6Li表示锂原子嵌入石墨形成复合材料)
正极反应:Li1-xMO2+xLi++x e-==LiMO2(LiMO2表示含锂的过渡金属氧化物)
下列有关说法正确的是( )
| A.锂离子电池充电时电池反应为C6Li+Li1-xMO2==LiMO2+C6Li1-x |
| B.电池反应中,锂、锌、银、铅各失去1mol电子,金属锌所消耗的质量最小 |
| C.锂离子电池放电时电池内部Li+向负极移动 |
| D.锂离子电池充电时阴极反应为C6Li1-x+xLi++x e-==C6Li |
某兴趣小组同学利用氧化还原反应:
2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液.下列说法正确的是
| A.a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.b电极上发生还原反应 |
下列用来表示物质变化的化学用语中,错误的是
| A.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+ |
| B.粗铜精炼时,与电源负极相连的是纯铜,电极反应式为:Cu2+ +2e- =Cu |
C.用Pt电极电解氯化铝溶液:2Cl-+2 H2O  Cl2↑+H2+2OH- Cl2↑+H2+2OH- |
| D.由Mg、Al、NaOH溶液组成原电池,其负极反应式为:Al-3e-+4OH-=AlO2-+2H2O |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的
| A.放电时负极反应为:Zn+2OH-→Zn(OH)2+2e- |
| B.充电时阳极反应为:Fe(OH)3+5OH-→FeO42-+4H2O+3e- |
| C.放电时每转移3 mol 电子,正极有1 mol K2FeO4被氧化 |
| D.放电时正极附近溶液的碱性增强 |
下图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间,下列有关描述错误的是( )

| A.生铁块中的碳是原电池的正极 |
| B.红墨水柱两边的液面变为左低右高 |
| C.两试管中相同的电极反应式是:Fe-2e-=Fe2+ |
| D.a试管中发生了吸氧腐蚀,b试管中发生了析氢腐蚀 |
某兴趣小组同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO4=2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,盐桥中装有饱和溶液。下列说法正确的是( )

| A.a电极上发生的反应为:MnO4-+8H++5e-═Mn2++4H2O |
| B.外电路电子的流向是从a到b |
| C.电池工作时,盐桥中的SO42-移向甲烧杯 |
| D.b电极上发生还原反应 |