根据右图,下列判断中正确的是( )
| A.烧杯a中的溶液pH升高 |
| B.反应一段时间后,烧杯a底部有白色沉淀 |
| C.盐桥中阳离子向b烧杯方向运动 |
| D.铁电极为原电池负极 |
将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘少。下列说法正确的是( )
| A.液滴中的Cl―由a区向b区迁移 |
B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e- 4OH- 4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe 2+由a区向b区迁移,与b区的OH―形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e- Cu2+ Cu2+ |
有关原电池的判断正确的是( )
| A.比较活泼的金属一定做负极,活泼性较弱的金属一定做正极 |
| B.原电池的正、负极材料不一定都参与反应 |
| C.原电池的正极在放电后质量一定增加 |
| D.原电池的正极是电子流 |
已知反应AsO43-+2I-+2H+ AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
AsO33-+I2+H2O是可逆反应。设计如图装置(C1、C2均为石墨电极),分别进行下述操作。
Ⅰ.向B烧杯中逐滴加入浓盐酸
Ⅱ.向B烧杯中逐滴加入40% NaOH溶液
结果发现电流计指针均发生偏转.据此,下列判断正确的是
| A.操作Ⅰ过程中,C1为正极 |
| B.操作Ⅱ过程中,盐桥中的K+移向B烧杯溶液 |
| C.Ⅰ操作过程中,C2棒上发生的反应为:AsO43-+2H++2e - = AsO33-+H2O |
| D.Ⅱ操作过程中,C1棒上发生的反应为:2I- - 2e- = I2 |
将分别盛有熔融的氯化钾、氯化镁、氧化铝的三个电解槽串联,在一定条件下通电一段时间后, 析出钾、镁、铝的物质的量之比为
| A.1:2:3 | B.3:2:1 | C.6:3:1 | D.6:3:2 |
一种新的酒后驾车人员体内酒精含量的检测装置如右图所示,下列说法不正确的是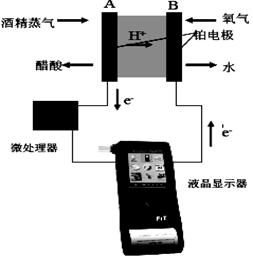
| A.该检测装置实现了将化学能转化了电能,且单位时间内通过电量越大,酒精含量越高 |
| B.电极A 的反应: H2O + C2H5OH-4e- = CH3COOH + 4H+ |
| C.电极B 是正极,且反应后该电极区pH 值减小 |
| D.电池总反应:O2 + C2H5OH = CH3COOH + H2O |
下列有关电化学知识的描述正确的是
| A.CaO+H2O="=" Ca(OH)2可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag装置中的盐桥中可以是装有含琼胶的KCl饱和溶液 |
| C.因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D.理论上说,任何能自发进行的氧化还原反应都可设计成原电池 |
下面关于原电池的说法,正确的是
| A.在正极上发生氧化反应 | B.化学性质较活泼的一极为负极 |
| C.在外电路中电子流出的极为正极 | D.原电池是将电能转化为化学能的装置 |
为了便于酒驾测试,生产了一种基于酸性燃料电池原理设计的酒精检测仪,
电池总反应式为:CH3CHO+O2=CH3COOH+H2O。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.负极上的反应为CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
| D.正极上发生的反应是:O2+4e-+2H2O=4OH- |
下列装置图或曲线图与对应的叙述相符的是
| A.图1:负极反应是Fe-2e-=Fe2+ |
| B.图2:酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
| C.图3:可表示乙酸溶液中通入氨气至过量过程中溶液导电性(I )的变化 |
D.图4:可表示在恒容密闭容器中反应“2SO2(g) +O2(g) 2SO3(g) ΔH<0”的平衡常数K正、K 2SO3(g) ΔH<0”的平衡常数K正、K |
随温度的变化
某原电池装置如下图所示。下列有关叙述中,正确的是
| A.Fe作正极,发生氧化反应 |
| B.负极反应:2H++2e-===H2↑ |
| C.工作一段时间后,两烧杯中溶液pH均不变 |
| D.工作一段时间后,NaCl溶液中c(Cl-)增大 |