恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应: N2(g)+3H2(g) 2NH3(g)(注:要求每步均要写出计算过程)
2NH3(g)(注:要求每步均要写出计算过程)
(1)若反应进行到某时刻t时,nt(N2)="6.5" mol,nt(NH3)="3" mol,计算a的值。
(2)反应达平衡时,混合气体的体积为358.4 L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量。
(3)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)等于多少?
在一容积为2L的密闭容器中加入2molA和6molB,保持温度为20℃,在催化剂存在的条件下进行下列反应:A(g)+2B(g)  2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
2C(g),达平衡后生成1.2mol C,平衡混合气体中C的体积分数为ω。
⑴求20℃时,该反应的平衡常数K(保留三位有效数字)
⑵20℃时,若在同一容器中加入1molA、 mol B和 mol C,则平衡混合气中C的体积分数仍为ω。
把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应:3A(g)+B(g) 2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算
2C(g)+xD(g),经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算
(1)x (2) B的转化率
(3) 平衡时A的浓度 (4) 恒温达平衡时容器内的压强与开始时压强比
在一定条件下,在容积为2L的密闭容器中,将2mol气体M和3mol气体N混合,发生如下反应:2M(g)+ 3N(g)  x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
x Q(g)+3R(g),经2min达平衡,生成2.4molR,并测得Q的浓度为0.4mol/L。求:
(1)用气体M来表示该反应的化学反应速率是多少?
(2)反应前后的压强比是多少?
(3)N的转化率是多少?
(4)平衡时气体Q所占的体积分数为多少?
以白云石(化学式表示为MgCO3·CaCO3)为原料制备Mg(OH)2的工艺流程如下图所示。
(1)研磨的作用是 。
(2)该工艺中可循环使用的物质是 、 (写化学式)。
(3)白云石轻烧的主要产物是MgO·CaCO3,而传统工艺是将白云石加热分解为MgO和CaO后提取,白云石轻烧的优点是 。
(4)加热反应的离子方程式为 。
(5)①加热反应时,在323k和353k溶液中c(NH4+)与反应时间的关系如下图所示,请在下图画出373k的曲线。
②由图可知,随着温度升高: 。
.已知一氧化碳与水蒸气的反应为CO+H2O CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
CO2+H2;在827℃时的平衡常数是100,如果反应开始时,一氧化碳和水蒸气的浓度都是0.011mol/L,计算:一氧化碳在此反应条件下的平衡转化率。
在一定温度下,10L密闭容器中加入5.0molSO2、4.5molO2,经10min后反应达平衡,此时O2的浓度为0.30mol/L。请计算(写出计算过程):
(1)10min内SO2的转化率;
(2)容器内反应前与平衡时的压强之比(最简整数比) ;
(3)平衡常数K。
在一定温度下,向10 L密闭容器中充入5.2 mol NO2,达到平衡时, c(N2O4)="0.16" mol·L-1。
请计算该温度下此反应的平衡常数K(请用三段式的方法写出计算过程)。
在体积固定的密闭容器中N2与H2发生反应:N2(g)+3 H2 2 NH3
2 NH3
达到平衡时c (N2)=3.5 mol·L-1,c (H2)=1 mol·L-1,c (NH3)=5 mol·L-1,求:
(1)N2和H2的起始浓度
(2)N2的转化率(要求有解题过程)
PCl5的热分解反应如下:PCl5(g)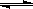 PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
(1)写出反应的平衡常数表达式;
(2)已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。计算该温度下的平衡常数。
已知一氧化碳与水蒸气的反应为:CO(g)+H2O (g) CO2(g)+H2(g) ,800℃时,在容积为2.0L的密闭容器中充入2.0mol CO(g)和3.0mol H2O(g),保持温度不变,4 min后反应达到平衡,测得CO的转化率为60%。
CO2(g)+H2(g) ,800℃时,在容积为2.0L的密闭容器中充入2.0mol CO(g)和3.0mol H2O(g),保持温度不变,4 min后反应达到平衡,测得CO的转化率为60%。
(1)求4 min内H2的平均化学反应速率。
(2)计算800℃时该反应的平衡常数。
(3)427℃时该反应的化学平衡常数为9.4,请结合(2)中的计算结果判断该反应的ΔH 0(填“>”、“<”或“=” )。
在密闭容器中将NO2加热到某温度时,进行如下的反应:2NO2 2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
2NO+O2,反应5分钟后达平衡,测得平衡时各组分的浓度分别为:c(NO2)=0.06 mol/L,c(NO)=0.24 mol/L。试求:
(1)NO2的转化率为多少?
(2)反应前后的压 强比为多少?
强比为多少?
(3)在这5分钟内,用O2来表示的平均反应速率是多少?
在5 L的密闭容器中充入2 mol A气体和1 mol B气体,在一定条件下发生反应:2A(g)+B(g) 2C(g),10min后达平衡时,在相同温度
2C(g),10min后达平衡时,在相同温度 下测得容器内混合气体的物质的量是反应前的5/6,试计算
下测得容器内混合气体的物质的量是反应前的5/6,试计算
①A的转化率
②平衡常数K
③10min内生成物C的反应速率
将N2和H2按一定比例混合,在相同状况下其密度是H2的3.6倍,取0.5mol该混合气体通入密闭容器内,使之发生反应,并在一定条件下达到平衡,已知反应达到平衡后容器内压强是相同条件下反应前压强的0.76倍。试求:
(1)反应前混合气体中N2和H2的体积比;
(2)达平衡时混合气体中氨的物质的量;
(3)平衡时N2的转化率。
已知CO(g)+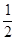 O2(g)=CO2(g),△H ="-283" kJ/mol;H2(g)+
O2(g)=CO2(g),△H ="-283" kJ/mol;H2(g)+ 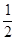 O2(g)=H2O(l),△H ="-285.8" kJ/mol;取CO和H2组成的混合气体0.5mol完全燃烧共放出142.34KJ的热量。若将此0.5mol混合气体充入密闭容器中置于900℃下发生 CO(g)+2 H2(g)
O2(g)=H2O(l),△H ="-285.8" kJ/mol;取CO和H2组成的混合气体0.5mol完全燃烧共放出142.34KJ的热量。若将此0.5mol混合气体充入密闭容器中置于900℃下发生 CO(g)+2 H2(g) CH3OH(g),在一定条件下达到平衡。平衡后容器内压强是相同条件下反应前压强的0.8倍,求:
CH3OH(g),在一定条件下达到平衡。平衡后容器内压强是相同条件下反应前压强的0.8倍,求:
(1)反应前混合气体中CO和H2的体积比;
(2)平衡混合气体中CH3OH和H2的物质的量;
(3)达到平衡时CO的转化率。