化学平衡常数K的数值大小是衡量化学反应进行程度的标志,在常温下,下列反应的平衡常数的数值如下:
2NO(g)  N2(g)+O2(g) K1=1×1030
N2(g)+O2(g) K1=1×1030
2H2(g)+O2(g)  2H2O(g) K2=2×1081
2H2O(g) K2=2×1081
2CO2(g)  2CO(g)+O2(g) K3=4×10-92
2CO(g)+O2(g) K3=4×10-92
以下说法正确的是
| A.常温下,NO分解产生O2的反应的平衡常数表达式为K1=c(N2)·c(O2) |
| B.常温下,水分解产生O2,此时平衡常数的数值约为5×10-80 |
| C.常温下,NO、H2O、CO2三种物质分解放出O2的倾向由大到小的顺序为 NO>H2O>CO2 |
| D.以上说法都不正确 |
COCl2(g)  CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是
CO(g)+Cl2(g) △H>0,当反应达到平衡时,下列措施能提高COCl2转化率的是
| A.恒容通入惰性气体 | B.恒压时通入惰性气体 |
| C.恒容通入COCl2气体 | D.加催化剂 |
右图是温度和压强对X + Y  2Z 反应影响的示意图图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )。
2Z 反应影响的示意图图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是( )。
| A.上述可逆反应的正反应为放热反应 |
| B.X、Y、Z均为气态 |
| C.X和Y中只有一种是气态,Z为气态 |
| D.上述反应的逆反应的△H>0 |
可逆反应∶2NO2 2NO+O2在密闭容器中反应,达到平衡状态的标志是:
2NO+O2在密闭容器中反应,达到平衡状态的标志是:
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时,生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ |
| C.①③④ | D.①②③④⑤⑥ |
已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应2HI(g)
2HI(g)的K=50,由此推测在450℃时,反应2HI(g)  H2(g)+I2(g)的化学平衡常 数为
H2(g)+I2(g)的化学平衡常 数为
| A.0.02 | B.50 | C.100 | D.无法确定 |
下列图示与对应的叙述相符的是
图6 图7 图8 图9
A.图6表示已达平衡的某反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件可能是加入催化剂,也可能是改变压强
B.图7表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A
C.图8表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是吸热反应
D.图9表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化
下列措施或事实不能用勒夏特列原理解释的是 ( )
| A.新制的氯水在光照下颜色变浅 |
| B.Fe(SCN)3溶液中加入6mol/L NaOH溶液后颜色变浅 |
| C.在合成氨的反应中,降温或加压有利于氨的合成 |
| D.H2、I2、HI平衡混合气加压后颜色变深 |
在恒温时,一固定容积的容器内发生如下反应:2NO2(g)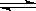 N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( )
N2O4(g) 达到平衡时,再向容器内通入一定量的NO2(g),重新达到平衡后,与第一次平衡时相比,NO2的体积分数 ( )
| A.不变 | B.增大 | C.减小 | D.无法判断 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) ΔH<0
2N2(g)+3H2O(g) ΔH<0
在恒容的密闭容器中,下列有关说法正确的是 ( )
| A.平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B.单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡 |
| C.平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| D.其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 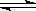 2c(g) △H1<0; x(g)+3y(g)
2c(g) △H1<0; x(g)+3y(g) 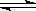 2z (g) △H2>0
2z (g) △H2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是 ( )
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+(aq)+ SCN-(aq) Fe(SCN)2+(aq)。已知平衡时,物质的量浓度[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( )
Fe(SCN)2+(aq)。已知平衡时,物质的量浓度[Fe(SCN)2+]与温度T的关系如图所示,则下列说法正确的是( ) 
| A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN-(aq)====Fe(SCN)2+(aq)ΔH>0 |
| B.温度为T1、T2时,反应的平衡常数分别为K1、K2,则K1< K2 |
| C.反应处于D点时,一定有v(正)>v(逆) |
| D.A点与B点相比,A点的[Fe3+]大 |
可逆反应a A(s)+b B(g) c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
| A.达平衡后,加入催化剂则C%增大 |
| B.达平衡后,若升温,平衡左移 |
| C.化学方程式中b >c +d |
| D.达平衡后,增加A的量有利于平衡向右移动 |
可逆反应:2NO2(g)  2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡
状态的标志是
①单位时间内生成nmol O2的同时生成2nmol NO2②单位时间内生成nmol O2的同时生成2nmol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态
| A.①④ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
已知:N2(g)+3H2(g) 2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是: ( )
2NH3(g);△H=-Q kJ·mol-1(Q>0)。现有甲乙两个相同的密闭容器,向甲容器中充入1mol N2(g)和3mol H2(g),在一定条件下达到平衡时放出的热量为Q1 kJ;在相同条件下向乙容器中充入2mol NH3(g),达到平衡时吸收的热量为Q2 kJ。已知Q2=3Q1,下列叙述中正确的是: ( )
A.Q1= Q Q |
| B.达到平衡时,甲容器中H2的转化率为25% |
C.平衡时甲容器中气体的压强为开始时压强的 |
| D.平衡时甲容器中NH3(g)的体积分数比乙容器中的小 |