实验室中所用少量氯气是用下列方法制取的,4HCl(浓)+MnO2 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O
试回答下列问题:
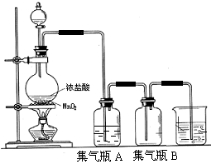
(1)实验室中可采用 溶液来吸收有毒的氯气,写出该反应的离子方程式 。
(2)实验取质量分数为36.5%,密度为1.19g·cm-3,浓盐酸100mL,反应结束后测得盐酸的浓度变为1.9mol/L,(忽略体积的变化)请你计算出实验过程生成标况下的Cl2多少L(写出计算过程)
钛白粉(主要成分是TiO2),广泛用于油漆、塑料、造纸等行业,还可用作乙醇脱水、脱氢的催化剂。下图是以钛铁矿(主要成分FeTiO3,钛酸亚铁)为主要原料生产钛白粉并获得副产品FeSO4·7H2O的工艺流程图。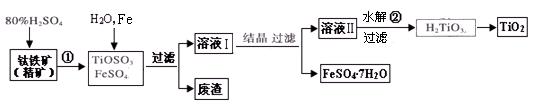
(1)钛铁矿与硫酸发生反应①的化学方程式为 ;在TiOSO4和FeSO4溶液中加入Fe的目的是 。
(2)溶液Ⅱ中TiOSO4在加热条件下发生水解反应②的离子方程式为 ;可回收利用的物质是 。
(3)为测定溶液Ⅱ中TiOSO4的含量,首先取待测钛液10 mL用水稀释至100 mL,加过量铝粉,充分振荡,使其完全反应:3TiO2+ +Al+6H+=3Ti3++Al3++3H2O。过滤后,取出滤液20.00 mL,向其中滴加2~3滴KSCN溶液作指示剂,用 (填一种玻璃仪器的名称)滴加0.1000mol·L-1 FeCl3溶液,当溶液出现红色达到滴定终点,用去了30.00mL FeC13溶液。待测钛液中TiOSO4的物质的量浓度是 。
实验室要用4 mol·L-1的浓硫酸配制500 mL 0.2 mol·L-1的稀H2SO4溶液。
(1).实验中所需用到的主要玻璃仪器有:量筒、烧杯、玻璃棒、 、 等。
(2).需用浓度为4mol/L的浓硫酸的体积为多少mL?
(3).取20 mL该稀溶液,然后加入足量的锌粒,求生成的气体体积(标况下)。
(15分)淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去):实验过程如下:①将1∶1的淀粉水乳液与少许硫酸(98%)加入烧杯中,水浴加热至85℃~90℃,保持30 min,然后逐渐将温度降至60℃左右;②将一定量的淀粉水解液加入三颈烧瓶中;③控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3、98%H2SO4的质量比为2:1.5)溶液;④反应3h左右,冷却,减压过滤后再重结晶得草酸晶体。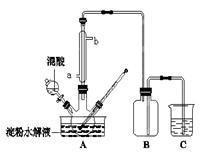
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑+3NO↑+9H2O
C6H12O6+8HNO3→6CO2+8NO↑+10H2O 3H2C2O4+2HNO3→6CO2+2NO↑+4H2O
请回答下列问题:
(1)实验①加入98%硫酸少许的目的是: 。
(2)冷凝水的进口是 (填a或b);实验中若混酸滴加过快,将导致草酸产量下降,其
原因是 。
(3)检验淀粉是否水解完全所用的试剂为 。
(4)草酸重结晶的减压过滤操作中,除烧杯,玻璃棒外,还必须使用属于硅酸盐材料的仪器有
(5)当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NOx全部吸收,发生的化学反应方程式为: 。
(6) 将产品在恒温箱内约90℃以下烘干至恒重,得到二水合草酸。用KMnO4标准溶液滴定,该反应的离子方程式为:2MnO4- + 5H2C2O4 + 6H+ = 2Mn2+ + 10CO2↑+ 8H2O
称取该样品0.12 g,加适量水完全溶解,然后用0.020 mol·L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),此时滴定终点的现象为 。滴定前后滴定管中的液面读数如图所示,则该草酸晶体样品中二水合草酸的质量分数为 。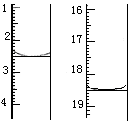
为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
① ② ③ ④ ⑤
称取粗盐
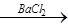
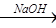
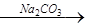
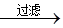 滤液
滤液
⑥ ⑦
 精盐
精盐
(1)判断BaCl2已过量的方法是
(2)第④步中,相关的离子方程式是
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
(4)为检验精盐纯度,特配制150 mL 0.2 mol·L—1 NaCl溶液,下图是该同学转移溶液的示意图,图中的错误是 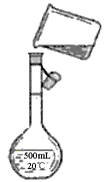
(5)提纯过程中步骤①⑤⑦都用到相同的仪器,名称:
这三个步骤中还需要用到的属于硅酸盐材料的仪器有 (填写仪器名称)
某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。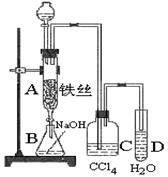
(1) 写出A中反应的化学方程式______________________
(2) 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡;
目的是______ ___,写出有关的化学方程式:_______________ ____
(3) C中盛放CCl4的作用是 。
(4)能证明苯和液溴发生的是取代反应,而不是加成反应,可向
试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验
证的方法是向试管D中加入______ ___,现象是 。
(12分)实验室用浓盐酸与二氧化锰共热制取氯气,其反应方程式为:MnO +4HCl(浓)
+4HCl(浓) MnCl
MnCl +2H
+2H O+Cl
O+Cl ↑。现将4.35 g MnO
↑。现将4.35 g MnO 跟足量36%的盐酸充分反应后,生成的氯气为多少克?
跟足量36%的盐酸充分反应后,生成的氯气为多少克?