自然界存在的碳酸盐类铜矿(如孔雀石、石青等)的化学组成为:aCuCO3·bCu(OH)2(a、b为正整数,且a≤2,b≤2)。
(1)将孔雀石、石青矿样分别加盐酸至完全溶解,耗用HCl物质的量与产生CO2物质的量之比:孔雀石为4∶1;石青为3∶1。则它们的化学组成为:
孔雀石:_________,石青:_________。
(2)今有一份碳酸盐类铜矿样品,将其等分为A、B两份。然后,加盐酸使A样品完全溶解,产生CO2 3.36 L(标准状况),加热B样品,使其完全分解,得到20 g CuO。试计算并确定该矿石的化学组成。
(3)某碳酸盐类铜矿样加酸完全溶解后,产生CO2 6.72 L(标准状况),这份矿样中CuO含量不低于_________g。
(4)设某碳酸盐类铜矿样的质量为A g,所含CuO质量为G g,加酸完全溶解后,产生的CO2的体积(标准状况)为V L,则含铜矿样的A、V、G之间的关系式为:_________。
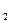 +4HCl(浓)
+4HCl(浓) MnCl
MnCl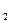 +2H
+2H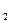 O+Cl
O+Cl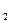 ↑。现将4.35 g MnO
↑。现将4.35 g MnO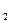 跟足量36%的盐酸充分反应后,生成的氯气为多少克?
跟足量36%的盐酸充分反应后,生成的氯气为多少克?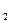 +4HCl(浓)
+4HCl(浓) MnCl
MnCl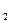 +2H
+2H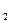 O+Cl
O+Cl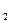 ↑。现将4.35 g MnO
↑。现将4.35 g MnO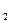 跟足量36%的盐酸充分反应后,生成的氯气为多少克?
跟足量36%的盐酸充分反应后,生成的氯气为多少克?