实验室在制备气体时,对某些气体来说,收集方法即可采用排水法,又可采用排空气法收集。下列气体中,能同时采用上述两种收集方法的是( )
| A.NH3 | B.NO | C.NO2 | D.H2 |
下列实验操作均要用玻璃棒,其中玻璃棒的作用及其目的相同的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体
| A.①和② | B.①和③ | C.③和④ | D.①和④ |
下列制取气体的方法在实验室不可取的是
| A.铜和稀硝酸反应,排水法收集NO | B.锌和稀硝酸反应制氢气 |
| C.氮气和氧气反应制NO | D.加热氯化铵制取氨气 |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法不能达到实验目的的是( )
| |
混合物 |
试剂 |
分离方法 |
| A |
苯(苯酚) |
氢氧化钠溶液 |
分液 |
| B |
甲烷(乙烯) |
酸性高锰酸钾溶液 |
洗气 |
| C |
乙酸乙酯(乙酸) |
氢氧化钠溶液 |
蒸馏 |
| D |
乙炔(硫化氢) |
硫酸铜 |
洗气 |
无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )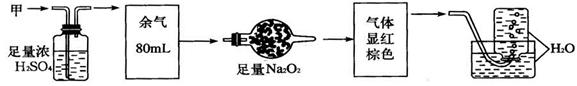
| A.NH3、NO2、N2 | B.NH3、NO、CO2 |
| C.NH3、NO2、CO2 | D.NO、CO2、N2 |
工业上制取硫酸铜不是直接用浓硫酸与铜反应,而是将铜丝浸入稀硫酸中并不断地从容器下部吹入细小的空气泡,这样做的优点不包括
| A.节省能源 | B.不产生污染大气的SO2 |
| C.提高了Cu的利用率 | D.提高了H2SO4的利用率 |
为了得到比较纯净的物质,使用的方法恰当的是( )
| A.向Na2CO3饱和溶液中,通入过量的CO2后,在减压、加热条件下,蒸发得到NaOH晶体 |
B.加热蒸发 饱和溶液得纯净的 饱和溶液得纯净的 晶体 晶体 |
C.向 溶液中加入过量的氯水,加热蒸发得 溶液中加入过量的氯水,加热蒸发得 晶体 晶体 |
D.向Fe2(SO4)3溶液加入足量 溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得 溶液,经过过滤、洗涤沉淀,再充分灼烧沉淀得 |
为制备干燥、纯净的CO2,将大理石和盐酸反应生成的气体先后通过装有下列物质的两个吸收装置,两个装置中应依次装入
| A.饱和Na2CO3溶液;无水CaCl2固体 | B.饱和NaHCO3溶液;浓H2SO4 |
| C.浓H2SO4;饱和Na2CO3溶液 | D.饱和Na2CO3溶液;稀H2SO4 |
利用下列装置可以完成的实验组合是 ( ) 
| 选项 |
制气装置 |
洗气瓶中试剂 |
瓶中气体 |
| A |
氯酸钾 MnO2 |
浓硫酸 |
O2 |
| B |
石灰石 稀盐酸 |
NaHCO3溶液 |
CO2 |
| C |
Zn 稀硫酸 |
浓硫酸 |
H2 |
| D |
MnO2 浓盐酸 |
浓硫酸 |
Cl2 |
用右下图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是
| |
气体 |
a |
b |
c |
 |
| A |
NO2 |
浓硝酸 |
铜片 |
NaOH溶液 |
|
| B |
SO2 |
浓硫酸 |
Cu |
浓硫酸 |
|
| C |
O2 |
双氧水 |
二氧化锰 |
碱石灰 |
|
| D |
CO2 |
稀盐酸 |
CaCO3 |
饱和NaHCO3溶液 |
四支试管分别充满O2、NO2、C12、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满C12的试管是 
A B C D
下列实验操作中正确的是
| A.制取溴苯:将铁屑、溴水、苯混合加热 |
| B.实验室制取硝基苯:先加入浓硫酸,再加苯,最后滴入浓硝酸 |
| C.鉴别甲苯和苯:向甲苯和苯中分别滴入酸性KMnO4溶液,振荡,观察是否褪色 |
| D.检验卤代烃中的卤原子:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀的颜色 |
下列各组物质在一定条件下反应,可以制得较纯净的1,2-二氯乙烷的是
| A.乙烷与氯气混合 | B.乙烯与氯化氢气体混合 |
| C.乙烯与氯气混合 | D.乙烯通入浓盐酸 |
下列气体只能用排水法收集的是
| A.NO | B.SO2 | C.NH3 | D.Cl2 |
用氢氧化钠固体配制0.10mol/L的氢氧化钠溶液,下列说法错误的是
| A.定容时俯视,会造成浓度偏高 | B.转移时不慎将转移液溅出,会造成浓度偏低 |
| C.称量时托盘上要垫上干净的称量纸 | D.定容摇匀后发现液面下降,不应继续加水 |