常温下,浓度均为0.1 mol/L的三种溶液:①CH3COOH溶液;②NaOH溶液;③CH3COONa溶液。下列说法不正确的是( )
| A.溶液的pH:②>③>① |
| B.水电离出的c(OH-):③>①>② |
| C.②和③等体积混合后的溶液:c(Na+)+c(H+)=c(OH-)+c(CH3COO-) |
| D.①和②等体积混合后的溶液:c(CH3COOH)+c(CH3COO-)="0.1" mol/L |
下列液体均处于25 ℃,有关叙述正确的是 ( )。
| A.某物质溶液的pH>7,则该物质一定是碱或强碱弱酸盐 |
| B.pH=6.5的牛奶中c(H+)是pH=4.5的H2SO4溶液中c(H+)的100倍 |
| C.pH=3的醋酸与pH=11的NaOH溶液等体积混合后溶液中: c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
| D.AgCl在等浓度的CaCl2溶液和NaCl溶液中的溶解度相同 |
下列叙述正确的是( )
| A.在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变 |
| B.Na2CO3溶液加水稀释后再恢复至原温度, pH和KW均减小 |
| C.室温下pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,水电离出的c(H+)之比104:1 |
| D.25℃,若测知氨水与NH4Cl混合溶液的pH>7,则溶液中c(NH4+)>c(Cl—) |
归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:(均在常温下)
①pH =1的强酸溶液,加水稀释后,溶液中所有离子的浓度均降低。
②pH=2的盐酸和pH=1的醋酸,c(H+)之比为2∶1。
③在Na2CO3和NaHCO3溶液中均存在下列关系c(Na+)+c(H+)=c(OH-)+c(HCO3‑)+2c(CO32-)
④反应2A (s) + B (g)=2C (g) + D (g) 不能自发进行,则该反应△H一定大于0
⑤已知醋酸电离平衡常数为Ka;醋酸根水解常数为Kh;水的离子积为Kw;
则三者关系为:Ka·Kh=Kw
⑥反应A(g) 2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能
2B(g);△H,若正反应的活化能为EakJ·mol-1,逆反应的活化能
为EbkJ·mol-1,则△H =(Ea-Eb)kJ·mol-1。其归纳正确的是
| A.①②③⑥ | B.③④⑤⑥ | C.②④⑤⑥ | D.①③④⑤ |
下列说法正确的是
| A.常温下,将pH=11的氨水稀释到原体积的10倍后,溶液的pH=10 |
| B.为确定某酸.H2A是强酸还是弱酸,可测NaHA溶液的pH,若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| C.用0.2000 mol/L NaOH标准溶液滴定HCl与CH3COOH的混合溶液(混合液中两种酸的浓度均约为0.1mol/L),至中性时,溶液中的酸未被完全中和 |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1 mol/L盐酸 ③0.1 mol/L氯化镁溶液④0.1 mol/L硝酸银溶液中,则Ag+浓度:①>④=②>③ |
下列有关实验的原理、方法和结论都正确的是
| A.将等体积、等pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH变化大 |
| B.用CH3COOH溶液作导电性实验,灯光较暗,说明CH3COOH是弱电解质 |
| C.向滴有酚酞的Na2CO3溶液中逐滴加入Ba(NO3)2,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |
| D.沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
下列说法正确的是
| A.NaHCO3和Na2CO3混合溶液中,一定有 c(Na+)+c(H+)=c(OH-)+c(HCO3-) +c(CO32-) |
| B.浓度均为0.1 mol·L-1的下列溶液,pH由大到小排列顺序为 NaOH>Na2CO3>NaHSO4>(NH4)2SO4 |
| C.向冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 |
| D.pH=3的硫酸与醋酸溶液,c(SO42-)与c(CH3COO-)之比为1∶2 |
(1)常温下,已知0.1 mol·L-1一元酸HA溶液中c(OH-) / c(H+)=1×10-8。
①常温下,0.1 mol·L-1 HA溶液的pH= ;写出该酸(HA)与NaOH溶液反应的离子方程式: ;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是: 。
(2)常温下,向pH=a的氨水中加入等体积盐酸时,溶液呈中性,则此盐酸的pH 14-a(>、<、=)
(3)向物质的量浓度均为0.01 mol·L-1的MnCl2和BaCl2混合溶液中,滴加Na2CO3溶液,先沉淀的离子是 ,当两种难溶电解质共存时,溶液中c(Ba2+)/c(Mn2+)= 。(此温度下,Ksp(BaCO3)=8.1×10-9、Ksp(MnCO3)=1.8×10-11)
下列有关说法中正确的是( )
| A.常温下,将1 L pH=12的氨水加水稀释为10 L后溶液的pH=11 |
| B.有甲、乙两醋酸溶液,测得甲的pH=a,乙的pH=a+1,若用于中和等物质的量浓度等体积的NaOH溶液,需甲、乙两酸的体积V (乙)>10V(甲) |
C.向浓度均为0.1 mol·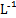 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] 的MgCl2、CuCl2混合溶液中逐滴加入氨水,先生成蓝色沉淀,说明Ksp[Cu(OH)2]>Ksp[Mg(OH)2] |
| D.水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 |
对于(NH4)2SO4溶液,下列说法正确的是
A.溶液中存在电离平衡:(NH4)2SO4 2NH4+ + SO42- 2NH4+ + SO42- |
| B.向溶液中滴加少量浓硫酸,c(NH4+)与c(SO42-)均增大 |
| C.加水稀释,溶液中所有离子的浓度均减小 |
| D.溶液中:c(SO42-)=2c(NH4+) + 2c(NH3·H2O) |
常温下,0.1 mol·L-1某一元酸HA溶液中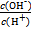 =1×10-12,下列说法中正确的是( )
=1×10-12,下列说法中正确的是( )
| A.溶液中由水电离出的c(H+)=1×10-10 mol·L-1 |
B.溶液中存在HA H++A- H++A- |
| C.与0.1 mol·L-1 NaOH溶液等体积混合后所得溶液为中性 |
| D.原溶液中加入一定量NaA晶体或加水稀释,溶液中c(OH-)均增大 |
下列说法正确的是
| A.中和等体积、等物质的量浓度盐酸和醋酸溶液,盐酸所需NaOH溶液多于醋酸 |
| B.常温下,20 LpH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
C.向0.1 mol/LCH3COOH溶液中加入少量CH3COONa固 体,溶液中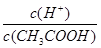 增大 增大 |
| D.一定温度下,10mL 0.50mol·L—1 NH4Cl溶液与20mL 0.25mol·L—1 NH4C1溶液含NH4+物质的量相同 |
下列说法符合事实的是
| A.常温下由水电离产生的c(H+)=10-12mol/L的溶液中加入铝粉都能够产生氢气 |
| B.已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12。在含Cl—、CrO42—浓度相同的溶液中滴加几滴稀AgNO3溶液时,则先生成AgCl沉淀 |
| C.电解硫酸铜溶液一段时间后,加入氧化铜固体不可能使溶液恢复到原来的浓度 |
| D.在NaAlO2和Na2CO3的混合溶液中逐滴滴加盐酸直至过量,开始没有沉淀,随后产生沉淀,最后沉淀消失 |
下列有关结论中,正确的是
| A.浓度为0.lmol/LCuSO4溶液,温度升高,溶液的pH降低 |
| B.—元酸与—元碱恰好完全反应后的溶液中—定存在c(H+)=c(OH-) |
C.浓度相同的AlCl3、NH3 H2O、Ba(OH2)三物质的溶液,等体积混合时没有沉淀生成 H2O、Ba(OH2)三物质的溶液,等体积混合时没有沉淀生成 |
| D.在所有能够溶解Al(OH)3的溶液中Cu2+、ClO-、Cl-、 Ca2+一定能够大量共存 |