A、B、C、D、E五种化合物,均含有某种短周期常见元素,它们的转化关系如图所示,其中A为澄清溶液,C为难溶的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
(1)写出化学式:
A________,C________,D________。
(2)写出下列反应的离子方程式。
A→B____________________________________________________________;
F→E_____________________________________________________________
A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断: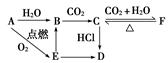
(1)A、D的化学式:
A.____________, D.____________。
(2)写出有关反应的化学方程式(是离子反应的直接写离子方程式)
B→C:________________________________________________________________________;
E→B:________________________________________________________________________;
F→C:________________________________________________________________________。
短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素,D单质燃烧时呈现黄色火焰,D的单质在高温下与C的单质充分反应,可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称:A________;B________;C________;D________。
(2)E的原子结构示意图: _______________________。
E的周期表中的位置: __________________。
(3)F离子的符号: ________________。
F离子结构示意图: __________________。
(4)A、B组成的最简单化合物的名称是:________。
(5)写出BC2与过量氢氧化钠反应的离子方程式:________________________________。
(6)C单质与D单质发生反应的产物有:________(填化学式)。C、D组成的一种化合物与水发生化合反应垢化学方程式为: ___________________________________________________________。
(7)能说明E的非金属性比F的非金属性________(填“强”或“弱”)的事实是:______________________________________________________________________________________________________________________________(举一例)
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。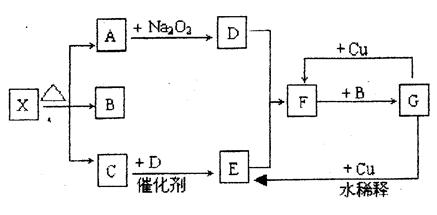
(1)写出下列各物质的化学式:
X: ;B: ;F: ;G: 。
(2)写出下列变化的反应方程式:
A→D: ;
G→E: 。
(3)实验室里,常用加热 的混合物的方法制取气体C,常采用 法来收集。
金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G,它们都是中学阶段常见的化学物质,它们之间存在下图所示的转化关系(图中有些反应的产物和反应的条件没有全部标出):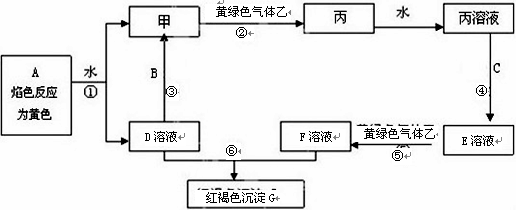
请根据以上信息回答下列问题:
(1)写出下列物质的化学式:丙 ,G 。
(2)反应③的化学方程式为 。
(3)反应⑤的离子方程式为 。
胃酸过多是常见的胃病。甲、乙两种中学课本中用以治疗胃酸过多的常见胃药,以下是它们的说明摘要。
甲:(1)白色结晶状粉末,可缓缓分解;(2)能溶于水,水溶液呈弱碱性;(3)遇酸及酸性药物则产生二氧化碳;(4)胃酸过多患者服用多见胃胀气,甚至有引起胃溃疡穿孔的危险。
乙:(1)与胃酸是中和作用缓慢而持久,可维持3~4小时。(2)凝胶本身覆盖于溃疡面上,具有保护作 用。(3)可溶于稀酸或氢氧化钠溶液中。
(1)请你推测,甲中含有的主要化学成份是 (填化学式);乙中含有的主要化学成份是 (填化学式)。
(2)试写出甲中含有的主要化学成份引起胃胀气反应的离子方程式: 。
(3)试写出乙中含有的主要化学成份分别与稀盐酸和氢氧化钠溶液反应的离子方程式:
; 。
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出),大部分反应在工业生产中得到实际应用。已知Ⅰ、G是单质,且Ⅰ是一种既能与酸反应又能与碱反应生成氢气的金属,L是一种无色气体,K是一种红棕色气体,E是一种红褐色沉淀。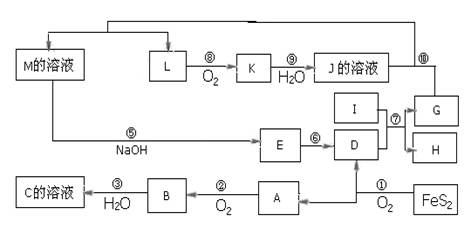
请填写下列空白:
(1)写出下列物质的化学式:C: ;J: 。
(2)写出下列反应的化学反应方程式:
反应⑦: 。
反应⑩: 。
(3)写工业上NH3与O2在一定条件下制取L的化学方程式: 。
下列中学化学中常见物质的转化关系图中,反应条件及部分反应物和产物未全部注明,已知A、D为金属单质,其它为化合物,其中C为两性氧化物。试推断:
(友情提示:金属Al可在高温下将一些金属从其氧化物中置换出来)
(1)写出物质的化学式:
A: B: C: H:
(2)写出下列反应的方程式:
A→D反应的化学方程式
C→F反应的离子方程式
D→G反应的离子方程式
工业上用铝土矿(主要成分为Al2O3,还含有Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过程如下:
(可供选择的试剂:稀盐酸、NaOH溶液、稀氨水,CO2等)
请写出你所设计的方案中以下各步反应涉及的化学方程式.
①____________________________________________________________________
②____________________________________________________________________
④___________________________________________
已知A、B、C、D、E为中学化学中常见的化合物,其中A是淡黄色固体,B是无色液体,甲、乙、丙为非金属单质,丁为地壳中含量最多的金属元素所组成的单质,C的焰色反应呈黄色,丙是黄绿色气体,它们之间的转化关系如图所示(有的反应部分产物已经略去):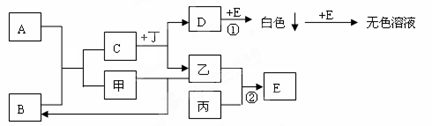
(1)实验室制取丙的化学方程式为 ,描述反应②的反应条件及现象
(2)反应①的化学方程式为:
(3)写出C与丙反应的离子方程式 ,列举这个反应的一种用途 。
已知某物质A有如下转化关系:
根据上图关系及实验现象,回答下列问题:
(1)A是 ,B是 ,G是 ,X是 (均填化学式)。
(2)写出反应Ⅱ的化学方程式 。
(3)写出反应Ⅲ的离子方程式 。
如图A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料,常温下H为无色液体。
根据图示回答问题:
(1)写出下列物质的化学式:B________,E________,I________;
(2)写出反应A+B→E+D的一种用途__________________;
(3)反应①的离子方程式是_________________________________________;
反应②的化学方程式是__________________________________________;
(4)J与盐酸反应的化学方程式是__________________ _________________;
反应后的溶液与D反应的离子方程式是___________________________________。
已知X、Y、Z都是中学化学中的常见三种气体,X为黄绿色,向X的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液颜色无明显变化;向Y的水溶液中滴入品红试液,品红褪色,将溶液加热后,溶液又呈红色;向Z的水溶液中滴入红色石蕊试液,溶液呈蓝色。据此回答下列问题:
(1)试写出下列物质的化学式:Y______________、Z________________;
(2)将X通入Y的水溶液中发生反应的离子方程式是 ;
(3)实验室制取Y的化学方程式是 。
已知A、B、C、D、E、F、G、H、I九种物质,A、B、D、E焰色反应均为紫色(透过蓝色钴玻璃),G是一种单质,I是一种化合物,H是一种淡黄色固体,它们的转化关系如图所示。请回答下列问题: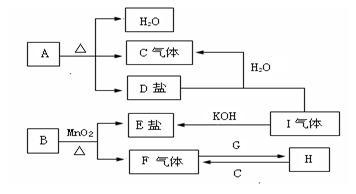
⑴B、D、I的化学式是B D I
⑵写出H的一种用途
⑶写出A受热分解的化学方程式
⑷若H与C反应固体增重4.2g,则参加反应的C气体在标准状况下的体积为 L
已知A~O各代表一种物质,除O外其余物质均由短周期元素组成,它们之间的转化关系如下图所示(反应条件略)。A、B、H分别是单质。B与冷水缓慢反应,与沸水迅速反应,放出氢气。D是一种离子化合物,其阴阳离子的个数比 为2︰3,且能与水反就应得到两种碱。C为淡黄色固体化合物,O能与G的水溶液反应生成蓝色沉 淀。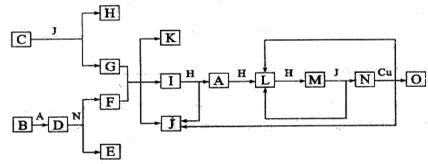
请回答下列问题:(1)组成B单质的元素位于周期表第 周期,第 族。化合物C和D的电子式为 ___ 、_____________。
(2)J的沸点比硒化氢(H2Se)的沸点高,其原因是 。
(3)写出I与H在点燃条件下反应生成A和J的化学方程式:
(4)写出D与足量的N反应生成E和F的化学方程式: 。
写出G与F加热反应生成K、I和J的化学方程式: 。
(5)上图中在同一反应里一种物质作氧化剂,又作还原剂,这样的反应共有 个。