下列框图中的字母分别代表一种常见的物质或其溶液,相互之间的转化关系如下图所示(部分产物及反应条件已略去)。已知A、B为气态单质,F是地壳中含量最多的金属元素的单质;E、H、I为氧化物,E为黑色固体,I为红棕色气体;M为红褐色沉淀。
请回答下列问题:
(1)A在B中燃烧的现象是 。
(2)D+E→B的反应中,被氧化与被还原的物质的物质的量比是 。
(3)G+J→M的离子方程式是 。
(4)Y受热分解的化学方程式是 。
现有原子序数依次增大的W、T、X、Y、Z、R六种前四周期元素.TW3能使湿润的红色石蕊试纸变蓝色.X、Y位于同一主族且Y的原子序数是X的2倍.Z、R是生活中常见金属,Z、R的器皿在潮湿空气中分别生成红褐色锈和绿色锈.
请回答下列问题:
(1)TW3的电子式为 .
(2)由W、T、X、Y中的元索组成一种离子化合物M,能发生如图转化关系:
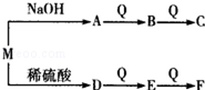
F与E的相对分子质量之差为16.则M的化学式可能为 .
C与水反应的化学方程式为 .
(3)(TW4)2Y2X8能和ZYX4在水溶液中反应生成Z2+和YX42﹣,写出离子方程式 .
(4)常温下,在WTX3浓溶液中以Z、R为电板构成原电池,负极材料是 ,
正极反应式为 .
A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如图所示转化关系。
试回答下列问题:
(1)A是___________,C是_________________。
(2)C的溶液与NaOH溶液混合后产生的现象是______________________________。
(3)反应①的反应类型是___________________。
(4)从A、B、C三种物质中任选一种,从它们所含共同元素的价态上预测所选物质具有氧化性或还原性,并设计实验验证。
预测性质___________________________________________
主要操作___________________________________________
可能的现象__________________________________________
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物,已知:

①反应C+G  B+H能放出大量的热,G是红综色固体粉末;
B+H能放出大量的热,G是红综色固体粉末;
②I是一种常见的温室气体,它和E可以发生反应:2E+I  2F+D,F中的E元素的质量分数为60%.
2F+D,F中的E元素的质量分数为60%.
回答问题:
(1)①中反应的化学方程式为______________________________;
(2)1.6g G 溶于盐酸,得到的溶液与铜粉完全反应,至少需要铜粉__________克;
(3)C与过量NaOH溶液反应的离子方程式为________________________________,
反应后的溶液与过量的化合物I反应的离子方程式为_______________________;
(4)E与I反应的化学方程式为______________________________;
(5)写出H物质在工业上的一种用途___________________;
(6)将一定量的B完全溶于过量盐酸中,然后通入0.005mol Cl2,再加入0.01mol重铬酸钾晶体(K2Cr2O7),恰好使溶液中B2+全部转化为B3+,铬元素本身被还原为+3价铬离子。通过计算确定原B的物质的量为______。
A.0.01mol B.0.03mol C.0.04mol D.0.07mol
X、Y、Z、W是中学化学中常见的四种气体。已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,通常状况下是黄绿色,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应;W气体的水溶液滴入酚酞变红色。
请回答下列问题:
(1)X、Y两种气体按物质的量之比1:1在水溶液中能发生反应,化学方程式为 。
(2)科学家发现,Z在催化剂条件下能与W反应,反应产物中的单质应是(填化学式) ;该反应是氧化还原反应,则其中的氧化剂是(填化学式) 。
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为 。
(4)检验W气体的方法是 。
常见的纯净物A、B、C、X,它们之间有如图转化关系(副产物已略去)。

试回答:
(1)若X是强氧化性单质,则A不可能是________。
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则B的化学式为__ ______;C溶液在储存时应加入少量X,理由是_________________(用必要的文字和离子方程式表示)。
(3)若A、B、C为含金属元素的无机化合物,X为强电解质溶液,A溶液与C溶液反应生成B,则B的化学式为________,X的化学式可能为________或________(写出不同类物质),反应①的离子方程式为_____________或__________。
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下图的反应(图中有些反应的产物和反应的条件没有全部标出)。
请根据以上信息回答下列问题:
(1)写出下列物质化学式:B 、F 、H 、乙 。
(2)写出下列反应的化学方程式
反应① 。
反应③ 。
(3)检验物质G中阳离子的方法 。
A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素的离子不含电子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与 E同周期;E元素原子的最外层电子数是其次外层电子数的 3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)E元素在元素周期表中的位置是_______________。
(2)由A、B、C三种元素形成的离子化合物的化学式为_________________。
(3)A可分别与C、E形成甲、乙两种三原子分子,且甲有18个电子、乙有10个电子,甲与乙比较,沸点较高的是(填化学式)_______________。
(4)F含有的化学键类型是___________和_____________,其水溶液呈酸性,请用相关的离子方程式解释其原因___________。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该过程的化学方程式为______。
已知B为黑色粉末,用D、E、G做焰色反应实验,隔蓝色钴玻璃观察,焰色均呈紫色,F为深红棕色液体,H能使淀粉变蓝,它们之间的相互转化关系如图所示。
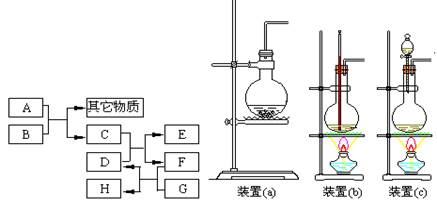
(1)请根据以上关系进行判断,指出下列物质的化学式:
A ,C ,D ,G .
(2)写出下列反应的化学方程式:
C+D: ;
A+B: 。
在A和B的反应中,A显示出来的性质是 (填写序号,多选倒扣)。
①只有还原性;②还原性和酸性;③只有氧化性;④氧化性和酸性
当A和B进行反应时,应选择上图所示装置中的 较为合适。
(3)C还能由以下反应制得:KClO3+6HCl=KCl+3Cl2↑+3H2O,在该反应中,被氧化的氯元素与被还原的氯元素的物质的量之比为 。
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下它们之间的相互转化关系如图所示(部分反应中的H2O已略去)。
请回答下列问题:
(1)若A可用于自来水消毒,D是生产、生活中用量最大、用途最广的金属单质,则反应②的离子方程式是________________________。
(2)若A是一种碱性气体,常用作制冷剂,B是汽车尾气之一,遇空气会变色,则反应①的化学方程式为________________________________。
(3)若A、C、D都是常见气体,C是导致酸雨的主要气体,则反应③的化学方程式为______________。某同学将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:________________。
已知A、B、C、D是中学化学的常见物质,且A、B、C均含有同一种元素。在一定条件下,它们之间的相互转化关系如图所示(反应中生成的H2O已略去)。请回答下列问题: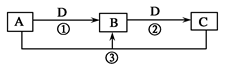
(1)若A是一种可用于自来水消毒的黄绿色气体,D是生活中常用的金属单质,则C的化学式为__________;写出A与C反应的离子方程式________________________。
(2)若A是一种常见的强碱,C常用于糕点发酵,则反应①的离子方程式是________________。
(3)若A是一种碱性气体,常用作制冷剂,B、D是空气中的主要成分,则C的化学式为_________。
(4)若A是一种无色、有臭鸡蛋气味的气体,C是导致酸雨的主要气体,则反应③的方程式为________。
中学化学中几种常见物质的转化关系如下图(部分产物未列出)。A是一种生活中常见金属单质之一,D是淡黄色固体单质。
请回答下列问题:
(1)A、G的化学式分别为A________,G________;
(2)用物理方法洗去试管内壁的D,应选择的试剂是_______________;
(3)F的浓溶液与A反应过程中,F体现的性质与下列反应中H2SO4体现的性质完全相同的是________(填字母);
A.C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
B.Fe+H2SO4===FeSO4+H2↑
C.Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D.FeO+H2SO4===FeSO4+H2O
(4)写出反应E+H2O2→F的离子反应方程式:______________________________;
(5)写出B→C的离子反应方程式:_______________________________________;
(6)若足量A与少量F在加热条件下反应,得到E和另一种气体,其体积比为1:1,则参加反应的A与F的物质的量之比为_______________。
下图中A~J均代表无机物或其水溶液,其中B、D、G是单质,B是地壳中含量最高的金属元素,G是气体,J是磁性材料。

根据图示回答问题:
(1)按要求写出下列化学用语:若B原子中子数比质子数多1,则B的原子符号为 ;C的电子式为 ,若D最外层只有两个电子,则D的原子结构示意图 ;
(2)写出反应①的化学方程式是 ;写出反应②的化学方程式并标出电子转移的方向和数目__________________
(3)J与稀硝酸反应的离子方程式是 ;用排水法收集满该反应的还原产物后,将试管倒扣在水槽中并通入O2使试管刚好全部充满水,假设液体不外溢,则所得溶液的物质的量浓度为 。
A、B、C三种物质中均含有同一种元素,它们之间有如右图所示的转化关系(部分反应物质已略去)。
Ⅰ.(1)若A是一种两性氧化物,B的水溶液呈酸性,请写出反应④的离子方程式:______________,B溶液显酸性的原因(用离子方程式表示)_____________。
(2)若反应①为置换反应,反应④为化合反应,C物质大量存在于海水中,是人体生理活动不可缺少的物质。工业上可以用C来制取A或B,保存少量单质A的方法 是__________,A在氧气中燃烧产物所含的化学键有_______________;用C来制取B反应的化学方程式为______________________。
(3)若反应①②③均为化合反应,反应④为置换反应。当A为一种金属单质时,请写出反应③可能的离子方程式________________________。若只用一种试剂鉴别B、C,可以选的试剂是_____________。