以下物质间的每步转化通过一步反应能实现的是( )
| A.Al-Al2O3-Al(OH)3-NaAlO2 |
| B.Fe-FeO-Fe(OH)2-Fe(OH)3 |
| C.Si-SiO2-H2SiO3-Na2SiO3 |
| D.Na-Na2O2-Na2CO3-NaOH |
类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列说法正确的是( )
| A.Fe能置换硫酸铜溶液的铜;则Na也能置换硫酸铜溶液的铜 |
| B.CaC2能水解:CaC2+2H2O==Ca(OH)2+C2H2↑;则Al4C3也能水解:Al4C3+12H2O ==4Al(OH)3↓+3CH4↑ |
| C.工业上电解熔融MgCl2的制取金属镁;则也可以用电解熔融AlCl3的制取金属铝 |
| D.CO2与Na2O2反应生成Na2CO3和O2;则SO2与Na2O2反应生成Na2SO3和O2 |
下列各组试剂中,只用试管和胶头滴管,不用其他试剂就可以鉴别的是( )
| A.NaHSO4溶液和Na2CO3溶液 | B.稀盐酸和AgNO3溶液 |
| C.AlCl3溶液和NH3·H2O溶液 | D.Ba(OH)2溶液和NaHCO3溶液 |
X、Y、Z、W有如右图所示的转化关系,则X、Y、Z可能是
① N2、NO、NO2 ② AlCl3、Al(OH)3 、NaAlO2
③S、SO2 、SO3 ④ NaOH、Na2CO3、NaHCO3
| A.①②③④ | B.①② | C.②④ | D.③④ |
锥形瓶内盛有气体X,滴管内盛有液体y。若挤压滴管胶头,使液体y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来。气体X和液体y不可能是( )
| |
X |
y |
| A |
NH3 |
H2O |
| B |
SO2 |
KOH溶液 |
| C |
CO2 |
6mol∕L H2SO4溶液 |
| D |
HCl |
6mol∕L NaNO3溶液 |
下列各组物质中,不能满足右图物质一步转化关系的选项是
| 选项 |
X |
Y |
Z |
| A |
Na |
NaOH |
NaCl |
| B |
Fe |
FeCl3 |
FeCl2 |
| C |
SiO2 |
Na2SiO3 |
H2SiO3 |
| D |
Al |
NaAlO2 |
Al(OH)3 |
(10分) A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生成的A是大气的主要成分,写出该反应的化学方程式:__________________________________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应的主要气体。判断单质A的元素在周期表中的位置:__________________。
(3)若A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中钠、氧外的元素为同一主族,且溶液均显碱性。写出②反应的化学方程式:__________________________________。
(4)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶液用于蚀刻印刷铜电路板,写出该反应的离子方程式:__________________________。
(5)若A为淡黄色固体,C、D是氧化物,且C是造成酸雨的主要物质. B与C可反应生成A。请写出B的电子式______________。
向一无色透明的溶液中滴加稀硫酸时有沉淀生成,且所得沉淀量与所加硫酸的关系如下图所示,则原溶液可能是 
| A.Na2SiO3与Na2CO3的混合溶液 |
| B.Na2S和Na2SO3的混合溶液 |
| C.NaAlO2与Na2SiO3的混合溶液 |
| D.Na2SO3与Na2SiO3的混合溶液 |
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
| 物质 编号 |
物质转化关系 |
甲 |
乙 |
丙 |
丁 |
| ① |
 |
Cu |
CuO |
CuSO4 |
Cu(NO3)2 |
| ② |
Na2CO3 |
NaOH |
NaHCO3 |
CO2 |
|
| ③ |
(NH4)2SO3 |
CaSO3 |
SO2 |
NH4HSO3 |
|
| ④ |
CH3CH2Cl |
C2H5OH |
CH2=CH2 |
CH3CH3 |
A.①②③④ B.①②③ C.①③④ D.②④
非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是________;
②在工业生产中B气体的大量排放被雨水吸收后形成了________而污染了环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是:A________;C________.
②D的浓溶液在常温下可与铜反应并生成C气体,请写出该反应的化学方程式___________________________。该反应________(填“属于”或“不属于”)氧化还原反应。
下列叙述正确的是
| A.SO2具有还原性,故可作漂白剂 |
| B.Na的金属活动性比Mg强,故可用Na与MgCl2溶液反应制Mg |
| C.浓硫酸具有吸水性,因此浓硫酸可以干燥某些气体 |
| D.Fe在Cl2中燃烧生成FeCl3,故在与其他非金属反应的产物中的Fe也显+3价 |
下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
| |
a |
b |
c |
| A |
Al |
AlCl3 |
Al(OH)3 |
| B |
NO |
NO2 |
HNO3 |
| C |
Si |
SiO2 |
H2SiO3 |
| D |
S |
SO2 |
H2SO4 |
A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去)。

(1)若A是一种黄色单质固体,则B→C的化学方程式为 。
(2)若A是一种活泼金属,C是淡黄色固体,则C的名称为 。将C长期露置于空气中,最后将变成物质D。现有D和NaHCO3的固体混合物10g,加热至质量不再改变,剩余固体质量为9.38 g,D的质量分数为 。
(3)若C是红棕色气体,A可能是一种能用下图装置制取的气体,请结合所学知识,回答下列问题:

①写出实验室制取A的化学方程式 。
②收集A的方法是 ,验证A是否已经收集满的方法是:
(任写一种)。
③若有5.35g氯化铵参加反应,则产生的A气体在标准状况下的体积为 L。
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题: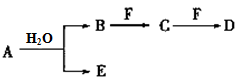
(1)若常温下A为有色气体。
①当F是一种金属单质时,请写出一定浓度的B溶液和适量F反应生成C与气体E的离子方程式:________________。
②当C是一种产生温室效应的气体分子时,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为_________;D中所含化学键的类型______________。
(2)若A为淡黄色固体,D为白色难溶于水的物质,且A和D的式量相等。
①用离子方程式表示F的水溶液呈酸性的原因__________________。
②A可由对应的单质直接化合生成,生成39gA时,放出255.5kJ的热量,写出该反应的热化学方程式_____________。
(3)若A中一种元素原子的最外层电子数为内层电子总数的1/5 ,将B和D分别溶于水,所得溶液按恰当比例混合,可得一种不含金属元素的盐溶液,请写出A与H2O反应的化学方程式:____;B转化为C的化学方程式为_______________。