(1)现有0.1 mol·L-1的纯碱溶液,试用pH试纸测定溶液的pH,其正确的操作是___________________;纯碱溶液呈碱性的原因是_________________(用离子方程式表示)。
(2)为探究纯碱溶液呈碱性是由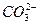 引起的,请你设计—个简单的实验方案:___________。
引起的,请你设计—个简单的实验方案:___________。
(3)为证明盐的水解是吸热反应,四位学生分别设计如下方案,其中正确的是( )
| A.甲学生:在醋酸钠溶液中滴入2滴酚酞,加热后红色加深,说明盐类水解是吸热反应 |
| B.乙学生:在盐酸中加入氨水,混合液温度上升,说明盐类水解是吸热反应 |
| C.丙学生:将硝酸铵晶体溶于水,水温下降,说明盐类水解是吸热反应 |
| D.丁学生:在氨水中加入氯化铵固体,溶液的pH变小,说明盐类水解是吸热反应 |
草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,向10 mL 0.01 mol·L-1 NaHC2O4溶液中滴加0.01 mol·L-1 NaOH溶液,随着NaOH溶液体积的增加,溶液中离子浓度关系正确的是( )
| A.V(NaOH)=0时,c(H+)=1×10-2 mol·L-1 |
B.V(NaOH)<10 mL时,不可能存在c(Na+)=2c(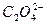 )+c( )+c( ) ) |
| C.V(NaOH)="10" mL时,c(H+)=1×10-7 mol·L-1 |
D.V(NaOH)>10 mL时,c(Na+)>c(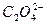 )>c( )>c( ) ) |
醋酸钡晶体[(CH3COO)2Ba·H2O]是一种媒染剂,下列有关0.1 mol·L-1醋酸钡溶液中粒子浓度的比较中错误的是( )
| A.c(Ba2+)>c(CH3COO-)>c(OH-)>c(H+) |
| B.c(H+)+2c(Ba2+)=c(CH3COO-)+c(OH-) |
| C.c(H+)=c(OH-)-c(CH3COOH) |
| D.2c(Ba2+)=c(CH3COO-)+c(CH3COOH) |
常温下,下列各溶液的叙述中正确的是( )
| A.0.1 mol·L-1的醋酸钠溶液20 mL与0.1 mol·L-1盐酸10 mL混合后溶液显酸性 c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)>c(CH3COOH) |
| B.pH=7的醋酸钠和醋酸混合液中:c(Na+)=c(CH3COO-) |
| C.0.1 mol·L-1的醋酸的pH=a,0.01 mol·L-1的醋酸的pH=b,则a+1<b |
| D.已知酸性HF>CH3COOH,pH相等的NaF与CH3COOK溶液中,c(Na+)-c(F-)<c(K+)-c(CH3COO-) |
为了配制 的浓度与Cl-的浓度比为1∶1的溶液,可在NH4Cl的溶液中加入( )
的浓度与Cl-的浓度比为1∶1的溶液,可在NH4Cl的溶液中加入( )
①适量的HCl ②适量的NaCl ③适量的氨水 ④适量的NaOH
| A.①② | B.③ | C.③④ | D.④ |
下列反应不属于水解反应或水解方程式不正确的是( )
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O====Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液: +H2O
+H2O
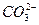 +H3O+
+H3O+
⑤NH4Cl溶于D2O中: +D2O
+D2O NH3·D2O+H+
NH3·D2O+H+
| A.①②③④ | B.①②③ |
| C.②③⑤ | D.全部 |
实验室在配制硫酸铁溶液时,先把硫酸铁晶体溶解在稀硫酸中,再加水稀释到所需的浓度,这样操作的目的是( )
| A.提高硫酸铁的溶解度 | B.防止硫酸铁分解 |
| C.降低溶液的pH | D.抑制硫酸铁水解 |
把0.2 mol·L-1NH4Cl溶液与0.1 mol·L-1NaOH溶液等体积混合后溶液中下列微粒的物质的量浓度的关系正确的是( )
A.c( )=c(Na+)=c(OH-)>c(NH3·H2O) )=c(Na+)=c(OH-)>c(NH3·H2O) |
B.c( )=c(Na+)>c(NH3·H2O)>c(OH-) )=c(Na+)>c(NH3·H2O)>c(OH-) |
C.c( )>c(Na+)>c(OH-)>c(NH3·H2O) )>c(Na+)>c(OH-)>c(NH3·H2O) |
D.c( )>c(Na+)>c(NH3·H2O)>c(OH-) )>c(Na+)>c(NH3·H2O)>c(OH-) |
在0.1 mol·L-1Na2CO3溶液中,各种微粒之间存在下列关系,其中不正确的是( )
A.c(Na+)+c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
B.c(Na+)=2[c( )+c( )+c( )+c(H2CO3)] )+c(H2CO3)] |
C.c(OH-)=c(H+)+c( )+2c(H2CO3) )+2c(H2CO3) |
D.c(Na+)=c( )=c(OH-)=c(H+) )=c(OH-)=c(H+) |
已知某溶液中只存在OH-、H+、 、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序可能有如下四种关系:
①c(Cl-)>c( )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
②c( )>c(OH-)>c(Cl-)>c(H+)
)>c(OH-)>c(Cl-)>c(H+)
③c( )>c(Cl-)>c(OH-)>c(H+)
)>c(Cl-)>c(OH-)>c(H+)
④c(Cl-)>c(H+)>c( )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解一种溶质,则该溶质是__________,上述四种离子浓度的大小顺序为__________(填序号)。
(2)若四种离子的关系符合③,则溶质为__________;若四种离子的关系符合④,则溶质为__________ 。
(3)将pH相同的NH4Cl溶液和HCl溶液稀释相同的倍数,下面图象正确的是__________(填图象符号)。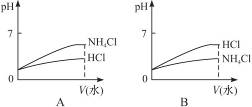

(4)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)___________c(NH3·H2O)(填“大于”“小于”或“等于”,下同);混合前酸中c(H+)和碱中c(OH-)的关系为c(H+)________c(OH-)。
(5)如右图所示,烧杯中盛放的溶液为盐酸,接通电流表G后,指针发生偏转,则负极材料是___________,正极反应式是______________。
25 ℃时,在浓度均为1 mol·L-1的(NH4)2SO4、(NH4)2SO3、(NH4)2Fe(SO4)2三种溶液中,若测得其中c( )分别为a、b、c(单位为mol·L-1),则下列判断正确的是( )
)分别为a、b、c(单位为mol·L-1),则下列判断正确的是( )
| A.a="b=c" | B.c>a>b | C.b>a>c | D.a>c>b |
常温下某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合溶液的pH如下表:
| 实验编号 |
HA的浓度(mol·L-1) |
NaOH的浓度(mol·L-1) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
c |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
(1)不考虑其他组的实验情况,单从甲组分析如何用a来分析HA属于强酸还是弱酸:_____。
(2)不考虑其他组的实验情况,单从乙组分析c是否一定等于0.2?________。混合溶液中离子浓度c(A-)与c(Na+)的大小关系为________。
(3)从丙组结果分析HA是________酸,该混合溶液中离子浓度大小关系为________。
(4)丁组实验混合溶液中由水电离的c(OH-)=_____________mol·L-1。