关于盐类水解反应的说法正确的是()
| A.溶液呈中性的盐一定是强酸与强碱生成的盐 |
| B.含有弱酸根离子的盐的水溶液一定呈碱性 |
| C.盐溶液的酸碱性主要决定于形成盐的酸碱性的相对强弱 |
| D.同浓度的NH4Cl和NaClpH之和大于14 |
已知ROH为强碱,HM为弱酸,使其完全反应后的RM溶液中,各种离子浓度由小到大的顺序是()
| A.c(OH-)<c(H+)<c(M-)<c(R+) | B.c(H+)<c(M-)<c(R+)<c(OH-) |
| C.c(H+)<c(OH-)<c(M-)<c(R+) | D.c(R+)<c(M-)<c(H+)<c(OH-) |
在盐类发生水解反应的过程中正确的说法是()
| A.盐的电离平衡被破坏 | B.水的电离程度逐渐增大 |
| C.溶液的pH发生变化 | D.没有中和反应发生 |
某盐的化学式XmYn为最简结构(m≠n),将一定量的盐溶于足量水时:
(1)若测得溶液的pH为5,则该盐与水反应的离子方程式可能为:__________________。
(2)若测得该盐溶液的pH为9,则该盐与水反应的离子方程式可能为:_______________。
(3)若X、Y为同周期的短周期元素,XmYn溶于水时,有白色沉淀产生,又有无色气体放出,则XmYn溶于水的化学方程式为:______________________________。
已知某溶液中只存在OH-、H+、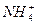 、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(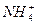 )>c(H+)>c(OH-)②c(Cl-)>c(
)>c(H+)>c(OH-)②c(Cl-)>c(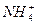 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
③c(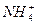 )>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(
)>c(Cl-)>c(OH-)>c(H+)④c(Cl-)>c(H+)>c(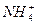 )>c(OH-)
)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶液是_______________,上述四种离子的浓度的大小顺序为_______________(填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为_______________;若上述关系中④是正确的,则溶液中的溶质是_______________。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好成中性,则混合前c(HCl)_________c(NH3·H2O)(填“大小”“小于”或“等于”)。
等体积的下列溶液中,阳离子总数最多的是()
| A.0.1mol·L-1的FeCl3溶液 | B.0.1mol·L-1的AlCl3溶液 |
| C.0.05mol·L-1的Na2S溶液 | D.0.05mol·L-1的Al2(SO4)3溶液 |
下列离子因水解相互促进而不能共存的是()
A. 、Na+、Cl-、OH- 、Na+、Cl-、OH- |
B.Al3+、Na+、 、 、 |
C.H+、Fe2+、 、Cl- 、Cl- |
D. 、K+、 、K+、 、Al3+ 、Al3+ |
向氨水中逐滴加入稀盐酸,使溶液呈中性,则此时()
A.c( )=c(Cl-) )=c(Cl-) |
B.c( )>c(Cl-) )>c(Cl-) |
C.c( )<c(Cl-) )<c(Cl-) |
D.c( )与c(Cl-)关系不定 )与c(Cl-)关系不定 |
为了使Na2S溶液中c(Na+)/c(S2-)的比值变小,可以加入的物质是()
| A.适量盐酸 | B.适量NaOH溶液 | C.适量KOH溶液 | D.适量KHS溶液 |
某同学想把AlCl3溶液和Na2S溶液混合制取Al2S3,但最后得到一种白色絮状沉淀,并且混合液中有臭鸡蛋气味的气体放出。试解释造成此结果的原因,写出反应的离子方程式,并指出制取硫化铝的正确方法。
四种盐都是一元酸和一元碱反应生成的,实验测得盐AX和BY的水溶液pH都等于7,AY的水溶液pH>7,BX水溶液pH<7,下列结论正确的是()
| A.盐AX和BY没有发生水解,盐AY和BX发生了水解 |
| B.酸性HX>HY,碱性AOH>BOH |
| C.等物质的量的AY和BX的混合物溶于水,溶液呈中性 |
| D.等物质的量浓度的HX溶液和HY溶液的pH前者大于后者 |
c(N0048 )相同的下列溶液①NH4Cl②(NH4)2SO4③NH4HSO4④NH4HCO3,其物质的量浓度由大到小的顺序是()
)相同的下列溶液①NH4Cl②(NH4)2SO4③NH4HSO4④NH4HCO3,其物质的量浓度由大到小的顺序是()
| A.②④①③ |
| B.②③①④ |
| C.①④③② |
| D.④①③② |
已知同温同浓度时①H2CO3比H2S电离度大,②H2S比HCO 电离度大,则下列反应不正确的是()
电离度大,则下列反应不正确的是()
A.Na2CO3+H2S NaHCO3+NaHS NaHCO3+NaHS |
B.Na2S+H2O+CO2 NaHS+NaHCO3 NaHS+NaHCO3 |
C.2NaHCO3+H2S Na2S+2H2O+2CO2↑ Na2S+2H2O+2CO2↑ |
D.2NaHS+H2O+CO2 Na2CO3+2H2S Na2CO3+2H2S |