常温下,0.1mol/L的氯化铵溶液中,离子浓度最大的是
| A.Cl- | B.OH- | C.H+ | D.NH4+ |
下列有关说法错误的是
| A.室温下的某NaF溶液中,c(H+)=1×10-10 mol∙L-1,说明NaF使水的电离减弱 |
| B.Mg在空气中燃烧时发出耀眼的白光,一部分化学能转化为光能 |
| C.纯碱溶于热水中去污效果增强,说明纯碱的水解是吸热反应 |
| D.反应 N2(g)+3H2(g)=2NH3(g)(△H<0)达平衡后,降低温度,正、逆反应速率都减小,平衡向正反应方向移动 |
欲使0.1mol∙L-1的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3¯)都减少,其方法是
| A.通入二氧化碳气体 | B.加水稀释 |
| C.通入氯化氢气体 | D.加入饱和石灰水溶液 |
相同物质的量浓度的NaCN和NaClO溶液相比,前者的pH较大,则下列有关同温、同体积和同浓度的HCN和HClO叙述中,正确的是
| A.酸性:HCN>HClO |
| B.pH:HClO>HCN |
| C.浓度:c(CN-)<c(ClO-) |
| D.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
下列溶液均处于 25℃,有关叙述正确的是
| A.AgCl 在同浓度的CaCl2 和NaCl溶液中的溶解度相同 |
| B.0.1 mol∙L-1的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C.含有 NH4+、Cl-、H+、OH-的溶液中,其离子浓度一定是:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D.pH=4.5的番茄汁中 c(H+) 是 pH=6.5 的牛奶中 c(H+)的 100 倍 |
下列做法与盐类水解知识无关的是
| A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞 |
| B.施肥时,草木灰(有效成分为 K2CO3)不能与碳酸氢铵混合使用 |
| C.Al2S3不能用复分解反应的方法在溶液中制取,而只能用干法制备。 |
| D.配制 FeCl2溶液时常常要在溶液中加入少量铁粉 |
在蒸发皿中加热蒸干并灼烧(低于 300℃)下列物质的溶液,可以得到该固体溶质的是
| A.氯化铝 | B.亚硫酸钠 | C.硫酸镁 | D.碳酸氢钠 |
在盐类的水解过程中,下列各种情况必定发生的是
| A.盐的电离平衡被破坏 | B.水的电离平衡被破坏 |
| C.25℃,溶液的pH不是7 | D.溶液温度升高 |
常温下,物质的量浓度相同的下列溶液,NH4+浓度最大的是( )
| A.NH4Cl | B.NH4HCO3 | C.NH4HSO4 | D.CH3COONH4 |
下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2O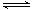 HCOO-+H3O+ HCOO-+H3O+ |
B.HS-+H2O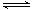 S2-+H3O+ S2-+H3O+ |
C.CO32-+H2O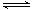 HCO3-+OH- HCO3-+OH- |
D.HCO3-+H2O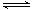 CO32-+H3O+ CO32-+H3O+ |
常温下pH=3的二元弱酸H2R溶液与a L pH=11的NaOH溶液混合后,混合液的pH刚好等于7(假设反应前后体积不变),则对反应后混合液的叙述正确的是
| A.c(R2-)+c(OH-)=c(Na+)+c(H+) |
| B.c(R2-)>c(Na+)>c(H+)=c(OH-) |
| C.2c(R2-)+c(HR-)=c(Na+) |
| D.混合后溶液的体积为2a L |
下列实验现象以及结论均合理的是
| A.在一块镀锡铁板刻一划痕,滴加酸化的食盐水浸泡及KSCN溶液,溶液颜色没有变化,判断其具有好的耐腐蚀性 |
| B.测定一定物质的量浓度的某NaA溶液的pH,pH>7,可以说明HA是弱酸 |
| C.在氯化银的悬浊液中加入碘化钠溶液,沉淀颜色不变,说明氯化银的溶解度比碘化银大 |
| D.在酸碱中和滴定中,用标准氢氧化钠溶液测定醋酸溶液的浓度时,用甲基橙做指示剂对滴定终点的判断比用酚酞的更准确 |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
| 选项 |
现象或事实 |
解释 |
| A |
碱性锌锰电池比普通锌锰电池性能好 |
锌在碱性介质中被氧化成更高价态 |
| B |
配制FeCl2溶液时加入少量铁粉 |
抑制Fe2+的水解 |
| C |
施肥时,草木灰(有效成分为K2CO3)不能与铵盐氮肥混合使用 |
它们反应生成氨气会降低肥效 |
| D |
纯水和干木头都不导电,但木头用水浸湿后却可以导电 |
水和干木头的某些成分发生化学反应 |
关于浓度均为0.1mol/L的四种溶液:①NH3·H2O、②HCl、③NH4Cl 、④(NH4)2CO3,下列说法正确的是
| A.由水电离出的c(H+):④>③>①>② |
| B.①、②和③等体积混合后的溶液:pH=7 |
| C.c(NH4+):③>④>① |
| D.①和②等体积混合后的溶液:c(NH4+)+c(NH3·H2O)=0.1mol/L |