化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置。
(1)把化学能转化为电能的装置是 (填“甲”或“乙”);
(2)④电极上的电极反应式为
(3)①电极上的电极反应式为 ,
检验该电极反应产物的方法是
(4)写出装置甲的反应总化学方程式 。
航天飞机常采用新型燃料电池作为电能来源,燃料电池一般指采用H2、CH4、CO、C2H5OH等可燃物质与O2一起构成的电池装置,它可直接将化学能转化为电能。我国发射的“神舟五号”载人飞船是采用先进的甲烷电池为电能来源的,该电池以KOH溶液为电解质,其总反应的化学方程式为:CH4+2O2+2OH-===CO32-+3H2O。
(1)电极反应 正极__________ _________负极____________ __________。
(2)消耗标准状况下的5.6 L O2时,有________mol电子发生转移。
(3)开始放电时,正极附近溶液的pH________(填“增大”“减小”或“不变”)。
(10分)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2===2H2O.试回答下列问题:
(1)若电解质溶液为KOH溶液,构成燃料电池,则:
①负极反应式为________________,
②工作一段时间后,溶液pH________(填“增大”或“减小”或“不变”).
(2)如把KOH改为稀H2SO4作电解质,则:
①正极反应式为________________,
②工作一段时间后,溶液pH________(填“增大”或“减小”或“不变”).
(3)如把H2改为甲烷,KOH作电解质,则正极反应式为____________________.
燃煤烟气中含有大量的氮氧化合物(NOx)、二氧化硫和二氧化碳等,不宜直接排放到空气中,可采用以下措施对燃煤烟气进行处理。
(1)脱硝:选择性催化还原法的脱硝原理是在催化剂存在下,通入甲烷使氮氧化合物(NOx)转化为无害气体,发生如下反应:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H1=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H2=-1160 kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为 。
(2)脱硫:①石灰石—石膏湿法烟气脱硫的工作原理是烟气中的二氧化硫与浆液中的碳酸钙以及鼓入的空气反应生成石膏(CaSO4·2H2O)。某电厂用煤400吨(煤中含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,用石膏湿法烟气脱硫中有96%的硫转化为石膏,则可生产石膏 吨。
② 新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由该铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中酸性氧化物分解除去,转化流程如图所示:
新型纳米材料氧缺位铁酸盐(ZnFe2Ox),由该铁酸盐(ZnFe2O4)经高温还原制得,常温下,它能使工业废气中酸性氧化物分解除去,转化流程如图所示: 若2molZnFe2Ox与足量SO2可生成1.0molS,
若2molZnFe2Ox与足量SO2可生成1.0molS,
则x= 。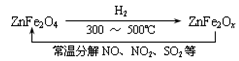
(3)脱碳:从脱硝、脱硫后的烟气中获取二氧化碳,用二氧化碳合成甲醇是碳减排的新方向。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)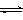 CH3OH(g)+H2O(g) △H3
CH3OH(g)+H2O(g) △H3
①取五份等体体积CO2和H2的的混合气体(物质的量之比均为1:3),
分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如图11所示,则上述CO2转化为甲醇反应的△H3 0(填“>”、“<”或“=”)。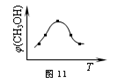
②在容积为1L的恒温密闭容器中充入1 mol CO2和3 mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图12所示。若在上述平衡体系中再充0.5 mol CO2和1.5 mol H2O(g)(保持温度不变),则此平衡将 移动(填“向正反应方向”、“不”或“逆反应方向”)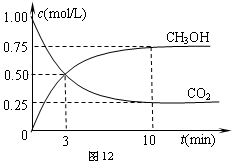
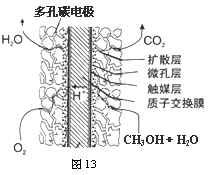
③直接甲醇燃料电池结构如上图13所示。其工作时负极电极反应式可表示为 。
氢氧燃料电池是将H2通入负极,O2通入正极而发生电池反应的,其能量转换率高。
(1)若电解质溶液为KOH溶液,其正极反应为 ,负极反应为 ;
(2)若电解质溶液为硫酸,其正极反应为 ,负极反应为 ;
若反应过程中转移了2mol电子,可产生水的质量为 g。
(3)若用氢氧燃料电池电解由NaCl和CuSO4组成的混合溶液,其中c(Na+)=3c(Cu2+)
=0.3mol·L—1,取该混合液100mL用石墨做电极进行电解,通电一段时间后,在阴极收集到0.112L(标准状况)气体。此时氢氧燃料电池外电路中转移电子数为 ,消耗H2的质量为 。
全矾液流电池是一种新型电能储存和高效转化装置,其电解质溶液为VOSO4溶液,该电解质溶液可通过下列方法制取:将18.2gV2O5和30mL浓H2SO4加入到40mL水中,并在充分搅拌下在水浴上加热20min。向溶液中加水稀释至375mL,通SO2至悬浮液变成深蓝色溶液。将此溶液蒸发浓缩至原体积的五分之一,通入足量的CO2。再将溶液煮沸后,用稀释至1000mL,全矾液流电池的工作原理为VO2++H2O+V2+  +V2++2H+。
+V2++2H+。
(1)通入SO2发生反应的化学方程式为 。
(2)通入SO2的目的是 。
(3)全矾液流电池充电时,阳极的电极反应式为 。
(4)某溶液中含有VO2+、Cr2O32—,现向此溶液中滴入29.00mL0.1mol/L的FeSO4溶液,恰好使VO2+ →VO2+,Cr2O32—→ Cr3+。再滴入2.00mL,0.020mol/LKMnO2溶液,又恰好使VO2+ →VO2+,而Cr3+不变,试求溶液中Cr的质量(mg).
氢氧碱性燃料电池是一种高效、环境友好的新型电池,在航空航天、潜艇和汽车等领域得到了广泛的应用。
⑴写出该电池两极的电极反应式。
负极: ,
正极: 。
⑵ 用该燃料电池做电源,以石墨为电极电解足量的饱和食盐水,请回答下列问题:
①写出电解饱和食盐水发生反应的化学方程式: 。
②每生成 0.1 mol 阳极产物,燃料电池中消耗氢气的物质的量为 。
,(1)以甲烷为燃料制作新型燃料电池,电解质为氢氧化钾溶液。电池负反应式为 ;放电时钾离子移向电池的 (填“正”或“负”) 极
(2)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,达到平衡时,溶液pH=5.60,c(H2CO3)=1.5×10-5 mol·L-1。若忽略水的电离及H2CO3的第二级电离,
则H2CO3  HCO3-+H+的平衡常数K1= (已知10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= (已知10-5.60=2.5×10-6)
(3)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中
c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是
(用离子方程式和必要的文字说明)。
美国阿波罗宇宙飞船上使用的氢氧燃料电池是一种新型的化学电池,其构造如图所示;两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电。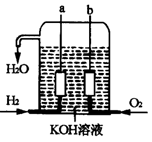
(1)a极是 极,b极是 极,
电极反应式分别为 , 。
(2)氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料,往往是某些碳氢化合物,如甲烷(天然气)、汽油等。请写出将图中H2换成CH4时所构成的甲烷燃料电池中a极的电极反应式: 。此时电池内总的反应方程式为 。
我国发射上天的宇宙飞船——“神舟”六号上使用氢氧燃料电池,其电池总反应为:2H2+O2====2H2O,电解质溶液溶质为KOH,溶剂是水,反应保持在较高温度下进行,使生成的水不断蒸发,经过一定的处理后供宇航员使用,该电池放电时负极反应为:_______________________,正极反应为:______________________
23.已知:铅蓄电池总的化学方程式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
负极反应为:Cd+2OH--2e-=Cd(OH)2
铅蓄电池使用(放电)一段时间后,其内阻明显增大,电压却几乎不变,此时只有充电才能继续使用。镍镉碱性充电电池使用(放电)到后期,当电压明显下降时,其内阻却几乎不变,此时充电后也能继续使用。回答下列问题:
⑴铅蓄电池在放电时的负极反应为 ,其在充电时阳极反应为 ;
⑵镍镉碱性充电电池在充电时的总反应的化学方程式为 ;
⑶上述两种电池使用一段时间后,一个内阻明显增大,而另一个内阻却几乎不变的主要原因可能是 ;
⑷如果铅蓄电池在放电时回路中有2mol电子转移时,消耗H2SO4 mol。
人们已经研制出以丙烷为燃料的新型燃料电池,电解质为熔融酸盐,电池

(2)该电池的正极通入O2和CO2,负极通入丙烷,则正极的电极反应式为__________________________________,电池工作时CO32—移向_____________极。
(3)用该电池电解1L 1 mol·L—1的AgNO3溶 液,此电解池反应的化学方程式为_________________________________________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
液,此电解池反应的化学方程式为_________________________________________________;当该电池消耗0.005molC3H8时,所得溶液的pH为__________(溶液体积变化忽略不计)
甲醇是一种可再生能源,具有广泛的开发和应用前景。
⑴工业上一般采用下列反应合 成甲醇:CO(g)+2H2(g)
成甲醇:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
①下列数据是在不同温度下的化学平衡常数(K)。
| 250℃: K1=__________ |
300℃: K2=0.270 |
350℃: K3=0.012 |
由表中数据判断ΔH 0(填“>”、“=”或“<”=。)
②250℃,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得:
CO剩余0.4mol,求K1。
⑵已知在常温常压下:①CH3OH(l)+O2(g)=CO(g)+2H2O(l);△H=-442.8KJ/mol
②2CO(g)+O2(g)=2CO2(g);ΔH2 =-566.0kJ/mol
写出甲醇燃烧热的热化学方程式____________________________________________,
⑶某实验小组依据甲醇燃烧的反应原理,设计如图(A)所示的燃料电池装置。则:
①该燃料电池负极的电极反应为:___________________________ ,
,
②用该甲醇燃料电池对B池进行电解,己知c、d是质量相同的铜棒,电解2min后,取出c、d,洗净、烘干、称量,质量差为0.64g,在通电过程中,电路中通过的电子为_________mol。
汽车的启动电源常用铅蓄电池,电池反应为:Pb+PbO2+4H++2SO2-4 2PbSO4+2H2O;据此判断:
2PbSO4+2H2O;据此判断:
(1)放电时,铅蓄电池的负极材料是________;电极反应为__________________________
(2)放电时,电解质溶液中阴离子移向________极。
(3)若用该铅蓄电池作电源电解足量的食盐水,阳极产生0.05molCl2时,理论上H2SO4的
物质的量减小_______mol。
(4)铅蓄电池上有两个接线柱,一个接线柱旁标有“+”,另一个接线柱旁标有“—”。
关于标有“—”的接线柱,下列说法中正确的是___________
A.充电时作阳极,放电时作负极 |
B.充电时作阳极,放电时作正极 |
C.充电时作阴极,放电时作负极 |
D.充电时作阴极,放电时作正极 |
(5)充电时的阳极反应式是____________________________________。
铅蓄电池是典型的可充型电池,它的正负极是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题:
(1)、放电时:正极的电极反应式是________________;正极区PH值将________(填“变大”“变小”“不变”);电解液中H2SO4的浓度将变________;当外电路通过1mol电子时,理论上负极板的质量增加________g。
(2)、在完全放电耗尽PbO2和Pb时,若按图连接,电解一段时间后,则在A电极上生成________,B电极上生成________,此时铅蓄电池的正负极的极性将________。
(3)、某同学用碳棒、铜棒和稀硫酸为原材料,实现了在通常条件下不能发生的反应:
Cu+H2SO4(稀)=CuSO4+H2↑。
请在方框中画出能够实现这一反应的装置图。
-