铅蓄电池是最常见的二次电池,其电池总反应可以表示为:
Pb(s)+PbO2(s)+2H2SO4(aq)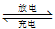 2PbSO4(s)+2H2O(l),下列说法不正确的是
2PbSO4(s)+2H2O(l),下列说法不正确的是
| A.电池的电解液为酸性溶液,正极为PbO2、负极为Pb |
| B.电池放电时,正极反应为PbO2+2 e-+SO42-+4H+=PbSO4+2H2O |
| C.电池充电过程中,阳极附近溶液的pH升高 |
| D.电池充电时,阴极反应为PbSO4+2e-=Pb+SO42- |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
3Zn(OH)2+2Fe(OH)3+4KOH。下列叙述不正确的是
| A.放电时负极反应为:3Zn-6e-+6OH-==3Zn(OH)2 |
B.充电时阳极反应为:Fe(OH)3-3e-+5OH- FeO42- +4H2O FeO42- +4H2O |
| C.放电时每转移3 mol电子,正极有1 mol K2FeO4被还原 |
| D.充电时阴极溶液的碱性减弱 |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电。其电池反应为:2CH3OH + 3O2+ 4OH- 2CO32- + 6H2O,则下列说法错误的是
2CO32- + 6H2O,则下列说法错误的是
| A.充电时每生成1 mol CH3OH转移6 mol电子 |
| B.充电时电解质溶液的pH逐渐增大 |
| C.放电时负极的电极反应为:CH3OH-6e-+8OH- = CO32- + 6H2O |
| D.放电时CH3OH参与反应的电极为正极 |
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是
| A.两个装置之间没有盐桥,故不能形成电流 |
| B.a电极的电极反应式 C2H5OH+16OH--12e-==2CO32-+11H2O |
| C.一段时间后,乙池d电极周围的溶液呈现棕褐色 |
| D.乙池在反应前后溶液的pH不变 |
如图为氢氧燃料电池原理示意图,下列叙述不正确的是
| A.a电极是负极 |
| B.b电极上发生氧化反应 |
| C.该电池工作时化学能转化为电能 |
| D.该电池的总反应为2H2 + O2 =2H2O |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法不正确的是( )
| A.检测时,电解质溶液中的H+向正极移动 |
| B.若溶液中有0.4 mol电子通过,则在标准状况下消耗4.48 L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2==CH3COOH+H2O |
| D.正极上发生的反应为:O2+4e-+4H+=2H2O |
氢氧燃料电池是将H2和O2通入电池,穿过浸入20%—40%的KOH溶液的多孔碳电极,其电极反应式分别为:2H2+4OH--4e-= 4H2O和O2+2H2O+4e-= 4OH-,下列不正确的是
| A.氢氧燃料电池属于环境友好电池 |
| B.通O2的极是正极,通入H2的极是负极 |
| C.工作一段时间后KOH溶液的溶质质量分数增大 |
| D.工作时溶液中的OH-向负极作定向移动 |
用酸性氢氧燃料电池为电源电解CuSO4溶液的实验装置如下图所示。下列说法中正确的是( )
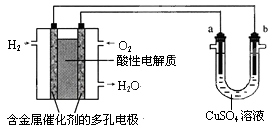
| A.燃料电池工作时,正极反应为:O2+2H2O+4e-=4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的 材料,电池反应为: 。下列说法错误的是( )
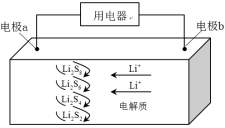
| A. |
电池工作时,正极可发生反应: |
| B. |
电池工作时,外电路中流过 电子,负极材料减重 |
| C. |
石墨烯的作用主要是提高电极a的导电性 |
| D. |
电池充电时间越长,电池中 的量越多 |
一种可充电锂-空气电池如图所示。当电池放电时,
与
在多孔碳材料电极处生成
。下列说法正确的是( )
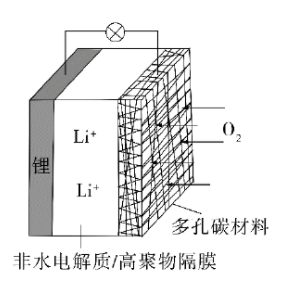
| A. | 放电时,多孔碳材料电极为负极 |
B. | 放电时,外电路电子由多孔碳材料电极流向锂电极 |
| C. | 充电时,电解质溶液中 向多孔碳材料区迁移 |
D. | 充电时,电池总反应为 |
某燃料电池主要构成要素如图所示,下列说法正确的是( )

A.电池可用于乙醛的制备
B.b电极为正极
C.电池工作时,a电极附近pH降低
D.a电极的反应式为O 2+4e ﹣﹣4H +═2H 2O
根据下图所示的装置,判断下列说法正确的是
| A.该装置中a极为负极 |
| B.该装置中b极的电极反应式是:2H++2e-= H2↑ |
| C.一段时间后,左边装置中溶液pH增大 |
| D.CuSO4溶液浓度保持不变 |
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:CH3CH2OH-4e-+H2O=CH3COOH+4H+。下列有关说法正确的是( )
| A.检测时,电解质溶液中的H+向负极移动 |
| B.若有0.4 mol电子转移,则在标准状况下消耗4.48L氧气 |
| C.电池反应的化学方程式为:CH3CH2OH+O2=CH3COOH+H2O |
| D.正极上发生的反应为:O2+4e-+2H2O=4OH- |
一种三室微生物燃料电池可用于污水净化、海水淡化,其工作原理如图所示。以下说法不正确的是( )

| A.中间室Cl—移向左室 |
| B.X气体为CO2 |
| C.处理后的含硝酸根废水pH降低 |
| D.电路中每通过1 mol电子,产生标准状况下氮气的体积为2.24L |