最新研制的一种由甲醇和氧气以及强碱作电解质溶液的新型手机电池。下列有关此电池的叙述错误的是( )
| A.正极电极反应:O2+2H2O+4e-====4OH- |
B.负极电极反应:CH3OH+8OH--6e-==== +6H2O +6H2O |
| C.电池在使用过程中电解质溶液的pH升高 |
| D.当外电路通过0.6 mol电子时,理论上消耗甲醇3.2 g |
镍镉可充电电池,电极材料是Cd和NiO(OH),电解质是KOH,放电时的电极反应式是Cd+2OH--2e- Cd(OH)2,2NiO(OH)+2H2O+2e-
Cd(OH)2,2NiO(OH)+2H2O+2e- 2Ni(OH)2+2OH-。下列说法不正确的是( )
2Ni(OH)2+2OH-。下列说法不正确的是( )
A.电池的总反应式是Cd+2NiO(OH)+2H2O 2Ni(OH)2+Cd(OH)2 2Ni(OH)2+Cd(OH)2 |
| B.电池充电时,镉元素被还原 |
| C.电池放电时,电池负极周围溶液的pH不断增大 |
| D.电池充电时,电池的负极和电源的正极连接 |
甲醇广泛用作燃料电池的燃料,可出天然气来合成,已知:
①2CH4(g)+O2(g)=2CO(g)+4H2(g) △H=-71kJ/mol
②CO(g)+2H2(g)=CH3OH(l) △H=-90.5kJ/mol
③CH4(g)+2O2(g)=CO2+2H2O(g) △H=-890kJ/mol
下列说法不能得出的结论是
| A.反应②在任何温度下均能自发进行 |
| B.CO(g)+2H2(g)=CH3OH(g)△H>-90.5kJ/mol |
| C.甲醇的燃烧热为764kJ/mol |
| D.若CO的燃烧热为282.5kJ/mol,则H2的燃烧热为286kJ/mol |
镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应:Mg+2H++H2O2= Mg2++2H2O。关于该电池说法正确的是
| A.镁合金为电源负极,发生氧化反应 | B.放电时H+在正极反应得电子 |
| C.正极方程式为:H2O2+2e-=2OH- | D.放电时正极的pH降低 |
甲醇燃料电池(DMFC)可用于笔记本电脑、汽车等,该燃料电池是以甲醇为燃料,氧气为氧化剂,电解质可以是质子交换膜(可传导氢离子),也可以是固体氧化物(可传导氧离子),甲醇和氧气分别在多孔金属电极上发生反应,从而将化学能直接转化为电能。下列叙述中错误的是
A.电池放电时,甲醇在负极发生氧化反应
B.以固体氧化物为电解质的电池放电时,氧离子由负极移向正极
C.以质子交换膜为电解质的电池放电时,正极的反应为:O2+4H++4e— 2H2O
D.电池的总反应是:2CH3OH+3O2 2CO2+4H2O
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:

①CH3OH(g)+H2O(g)=CO2(g)+3H2(g) △H1=" +" 49.0 kJ·mol -1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g) △H2=-192.9 kJ·mol -1
下列说法正确的是
| A.根据②推知:在25℃,101 kPa时,1mol CH3OH(g)燃烧生成 CO2和H2O(l)放出的热量应大于192.9 kJ |
| B.反应②中的能量变化如右图所示,则△H2= E1- E3 |
| C.H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收能量 |
| D.CH3OH的燃烧热△H=-192.9 kJ·mol -1 |
下列说法正确的是( )
| A.碱性锌锰干电池是二次电池 |
| B.铅蓄电池是一次电池 |
| C.二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生 |
| D.燃料电池的活性物质没有储存在电池内部 |
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆—氧化钇为电解质,这种电解质在高温下允许氧离子(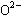 )在期间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
)在期间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是( )
O2
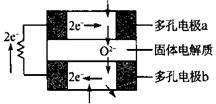
H2
| A.有O2放电的a极为电池的负极 |
| B.有H2放电的b极为电池的正极 |
C.a极对应的电极反应式为: O2 + 2H2O + 4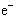 → 4 → 4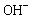 |
D.该电池的总反应方程式为:2 H2 + O2 2H2O 2H2O |
(08济南针对性训练,12)固体氧化物燃料电池,以固体氧化物(能传导O2—)作
为电解质,其工作原理如下图所示。下列关于固体氧化物燃料电池的有关说法中,正确的是( )

| A.外电路中电子由电极b流向电极a |
| B.固体氧化物的作用是让电子在电池内通过 |
| C.若H2作为燃料气,接触面发生的反应为H2+2OH—→2H2O+4e— |
| D.若C2H4作为燃料气,接触面上发生的反应为C2H4+6O2—→2CO2+2H2O+12e— |
镁及其化合物一般无毒(或低毒)、无污染,镁电池放电时电压高而平稳,因而越来越成为人们研制绿色原电池所关注的重点。有一种镁原电池的反应为:xMg+Mo3S4
MgxMo3S4。在镁原电池放电时,下列说法错误的是
| A.Mg2+向正极迁移 | B.正极反应为:Mo3S4+ 2xe- = Mo3S42x— |
| C.Mo3S4发生氧化反应 | D.负极反应为:xMg-2xe-=xMg2+ |
(08浙江金华十校模拟,9)一组镍氢电池能使一台试运行的混合动力公交车两年内跑10万公里。大功率镍氢动力电池及其管理模块,是国家“十五”863计划电动汽车重点专项中的一项重要课题。我国镍氢电池生产技术居世界先进水平。常见的镍氢电池的某极是镍氢合金LaNi5H6(LaNi5H6中各元素化合价均为0 ),电池反应通常表示为:LaNi5H6+6NiO(OH) LaNi5+6Ni(OH)2。。下列说法正确的是( )
LaNi5+6Ni(OH)2。。下列说法正确的是( )
| A.放电时储氢合金作正极 |
| B.充电时储氢合金作阳极 |
| C.充电时阳极周围c(OH-)增大 |
| D.放电时负极反应是LaNi5H6+6OH--6e-===LaNi5+6H2O |
如右图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极。接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中有气体生成。一段时间后(两玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,说明此时该装置形成了原电池,关于该原电池的叙述正确的是
| A.C(I)的电极反应式是2H++2e- = H2↑ |
| B.C(II)的电极反应式是Cl2+2e-=2Cl- |
| C.C(I)的电极名称是阴极 |
| D.C(II)的电极名称是负极 |
电动自行车由于灵活、快捷、方便,已成为上班族的主要代步工具,其电源常用铅蓄电池,反应原理为:PbO2+Pb+2H2SO4 2PbSO4+2H2O 下列叙述正确的是( )
2PbSO4+2H2O 下列叙述正确的是( )
| A.放电时PbO2是电池的负极,电解质溶液的密度逐渐减小 |
| B.放电时负极的电极反应式为:Pb+SO42--2e-=PbSO4↓ |
| C.电池充电时,PbO2得电子被氧化 |
| D.电池充电时,阴极电极反应式为:PbSO4+2H2O-2e-=PbO2+SO42-+4H- |